【改编】下列离子方程式正确的是
| A.将铁和铜用导线连接后同时插入硝酸银溶液中,铜上的电极反应为:Cu-2e-=Cu2+ |
| B.FeBr2溶液中通入少量的Cl2:Cl2+2Fe2+= 2Fe3++2Cl- |
| C.将金属钠放入硫酸铜溶液中:2Na+Cu2+-=2Na++Cu |
| D.酸性氢氧燃料电池的正极反应:H2-2e-= 2H+ |
某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。下列说法正确的是
| A.正极反应为Ag-e-=Ag+ |
| B.放电时,交换膜右侧溶液中有大量白色沉淀生成 |
| C.当电路中转移0.1mol e-时,通过交换膜的阳离子为0.2mol |
| D.用KCl溶液代替盐酸,则电池总反应不改变 |
下列关于电化学的说法中错误的是
| A.原电池的负极、电解池的阳极均发生氧化反应 |
| B.原电池将化学能转化为电能,电解池将电能转化为化学能 |
| C.电解水制取H2和O2时,为了增强导电性,可加入NaOH、NaCl、H2SO4 |
| D.利用原电池原理可制备化学电源,利用电解池原理可制备化学物质 |
已知反应AsO43-+2I-+2H+ AsO33-+I2+H2O是可逆反应。设计如图装置(C1、C2均为石墨电极),分别进行下述操作:Ⅰ.向B烧杯中逐滴加入浓盐酸;Ⅱ.向B烧杯中逐滴加入40%NaOH溶液结果发现电流表指针均发生偏转。据此,下列判断正确的是
AsO33-+I2+H2O是可逆反应。设计如图装置(C1、C2均为石墨电极),分别进行下述操作:Ⅰ.向B烧杯中逐滴加入浓盐酸;Ⅱ.向B烧杯中逐滴加入40%NaOH溶液结果发现电流表指针均发生偏转。据此,下列判断正确的是
| A.操作Ⅰ过程中,C1为正极 |
| B.操作Ⅱ过程中,盐桥中的K+移向B烧杯溶液 |
| C.Ⅰ操作过程中,C2棒上发生的反应为AsO43-+2H++2e-=AsO33-+H2O |
| D.Ⅱ操作过程中,C1棒上发生的反应为2I--2e-=I2 |
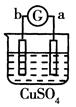
有a、b、c、d四个金属电极,有关的反应装置及部分反应现象如下:
| 实验 装置 |
 |
 |
 |
 |
| 部分实验现象 |
a极质量减小b极质量增加 |
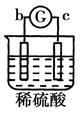
溶液中的SO42-向b极移动 |
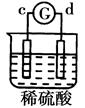
d极溶解c极有气体产生 |
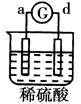
电流从a极流向d极 |
由此可判断这四种金属的活动性顺序是
A. a>b>c>d B. b>c>d>a C. d>a>b>c D. a>b>d>c
以熔融Li2CO3和K2CO3为电解质,天然气经重整催化作用提供反应气的燃料电池如右图。下列说法正确的是
| A.以此电池为电源电解精炼铜,当有0.1 mol e- 转移时,有3.2 g铜溶解 |
| B.若以甲烷为燃料气时负极电极反应式:CH4+5O2--8e-=CO32-+2H2O |
| C.该电池使用过程中需补充Li2CO3和K2CO3 |
| D.空气极发生的电极反应式为O2+4e-+2CO2===2CO |
蓄电池放电时是起原电池的作用,在充电时起电解池的作用。下式是爱迪生蓄电池分别在充电、放电时的反应: Fe + NiO2 + 2H2O  Fe(OH)2 + Ni(OH)2下列有关爱迪生电池的各种推断中不正确的是
Fe(OH)2 + Ni(OH)2下列有关爱迪生电池的各种推断中不正确的是
| A.放电时铁做负极,NiO2做正极 |
B.充电时阴极上的电极反应为: |
| C.放电时,电解质溶液中的阴离子是向正极方向移动 |
| D.蓄电池的两个电极必须浸入在碱性溶液中 |
如图是利用一种微生物将废水中的有机物(假设是淀粉)的化学能直接转化为电能,并利用此电能在铁上镀铜,下列说法中正确的是
| A.质子透过离子交换膜由右向左移动 |
| B.铜电极应与X相连接 |
| C.M电极反应式:(C6H10O5)n + 7nH2O-24ne-= 6nCO2↑+ 24nH+ |
| D.当N电极消耗0.25 mol气体时,则铁电极增重16 g |
有人设计将两根铂丝做电极插入到KOH溶液中,然后在两极上分别通入甲烷和氧气而构成燃料电池。该电池中反应的化学方程式为CH4+2O2+2KOH K2CO3+3H2O,则关于此燃料电池的下列说法中错误的是 (已知1个电子所带电量为1.6×10-19C)
K2CO3+3H2O,则关于此燃料电池的下列说法中错误的是 (已知1个电子所带电量为1.6×10-19C)
A.通入甲烷的电极为电池的负极,通入氧气的电极为正极
B.在标准状况下,每消耗5.6 L O2,可向外提供2.4×104 C的电量
C.通入甲烷电极的电极反应为:CH4+10OH--8e- CO32-+7H2O
CO32-+7H2O
D.放电一段时间后,溶液的pH减小
原电池是将化学能转变为电能的装置。关于如图所示,原电池的说法正确的是
| A.Cu为负极,Zn为正极 |
| B.电子由铜片通过导线流向锌片 |
| C.溶液中H+由正极流向负极 |
| D.原电池的反应本质是氧化还原反应 |
锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是
| A.铜电极上发生氧化反应 |
| B.电池工作一段时间后,甲池的c(SO42-)减小 |
| C.电池工作一段时间后,乙池溶液的总质量增加 |
| D.阴阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡 |
某同学为研究电化学原理,使用KC1盐桥设计如图所示实验装置。下列分析不合理的是
| A.闭合K2断开K1,左侧烧杯中的Fe2+向铁电极移动 |
| B.无论闭合K1断开K2,还是断开K1闭合K2,石墨电极上发生的反应都是Fe3++e-= Fe2+ |
| C.闭合K1断开K2,电流从石墨电极经过K1流向铁电极 |
| D.闭合K1断开K2,左侧烧杯中的溶液pH将逐渐降低 |
图Ⅰ的目的是精练铜,图Ⅱ的目的是保护钢闸门。下列说法不正确的是
| A.图Ⅰ中a为纯铜 |
| B.图Ⅰ中SO42-向b极移动 |
| C.图Ⅱ中如果a、b间连接电源,则a连接电源负极 |
| D.图Ⅱ中如果a、b间用导线连接,则X可以是铜 |
糕点(如月饼)包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。下列分析正确的是
| A.脱氧过程是吸热反应,可降低温度,延长糕点保质期 |
| B.脱氧过程中铁作原电池正极,电极反应为:Fe—3e— =Fe3+ |
| C.脱氧过程中碳做原电池负极,电极反应为:2H2O + O2 + 4e—= 4OH— |
| D.含有1.12g铁粉的脱氧剂,理论上最多能吸收氧气336mL(标准状况) |
试题篮
()