(1)家用液化石油气的主要成分之一是丁烷(C4H10),当10 kg丁烷完全燃烧并生成二氧化碳气体和液态水时,放出的热量为5×105 kJ。试写出丁烷燃烧的热化学方程式: 。已知1mol液态水汽化时需要吸收44 kJ热量,则反应C4H10(g)+6.5O2(g) ===4CO2(g)+5H2O(g)的ΔH= 。
(2)有同学用丁烷与空气为原料制作一燃烧电池,若以稀硫酸为电解质溶液时,其负极反应式为 。
(3)已知拆开1 mol H-H键,1 molN-H键,1 molN≡N键分别需要的能量是akJ、bkJ、ckJ,则N2与H2反应生成NH3的热化学方程式为 。
(1)在298K时,1molCH4在氧气中完全燃烧生成二氧化碳和液态水,放出热量890.0 kJ。写出该反应的热化学方程式 。现有CH4和CO的混合气体0.75mol,完全燃烧后,生成CO2气体和18g液态水,并放出515kJ热量,则CH4的物质的量为 。
(2)利用该反应设计一个燃料电池:用氢氧化钾溶液作电解质溶液,多孔石墨做电极,在电极上分别通入甲烷和氧气。通入甲烷气体的电极应为 极(填写“正”或“负”),该电极上发生的电极反应式为 。
(3)在下图所示实验装置中总反应的方程式为 ;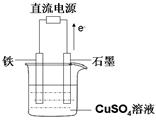
如果起始时盛有1000mL pH=5的硫酸铜溶液(25℃,CuSO4足量),一段时间后溶液的pH变为1,此时可观察到的现象是 ;
若要使溶液恢复到起始浓度(温度不变,忽略溶液体积的变化),可向溶液中加入 (填物质名称),其质量约为 。
(共7分)硫—碘循环分解水制氢主要涉及下列反应:
ⅠSO2+2H2O+I2===H2SO4+2HI
Ⅱ2HI H2+I2
H2+I2
Ⅲ2H2SO4===2SO2+O2+2H2O
(1)分析上述反应,下列判断正确的是________。
a.反应Ⅲ易在常温下进行
b.反应Ⅰ中SO2氧化性比HI强
c.循环过程中需补充H2O
d.循环过程产生1 mol O2的同时产生1 mol H2
(2)一定温度下,向1 L密闭容器中加入1 mol HI(g),发生反应Ⅱ,H2物质的量随时间的变化如图所示。
0~2 min内的平均反应速率v(HI)=________。该温度下,H2(g)+I2(g) 2HI(g)的平衡常数K=________。
2HI(g)的平衡常数K=________。
相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则________是原来的2倍。
a.平衡常数 b.HI的平衡浓度
c.达到平衡的时间 d.平衡时H2的体积分数
(3)实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡________移动(填“向左”、“向右”或“不”);若加入少量下列试剂中的________,产生H2的速率将增大。
a.NaNO3 b.CuSO4 c.Na2SO4 d.NaHSO3
(4)以H2为燃料可制作氢氧燃料电池。已知2H2(g)+O2(g)===2H2O(l) ΔH=-572 kJ·mol-1某氢氧燃料电池释放228.8 kJ电能时,生成1 mol液态水,该电池的能量转化率为________。
现有如下两个反应:
A、NaOH + HCl =" NaCl" + H2O
B、2FeCl3+Cu =2FeCl2+CuCl2
根据两反应本质,判断能否设计成原电池:A、_________,B、__________(选择“能”或“不能”);
(2)如果不能,说明其原因________________________________________________________;
(3)如果可以,则写出正、负极材料及其电极反应式,电解质溶液:
负极材料________,电极反应式_______________,电解质溶液____________;
正极材料________,电极反应式_______________。
下图是一个化学过程的示意图。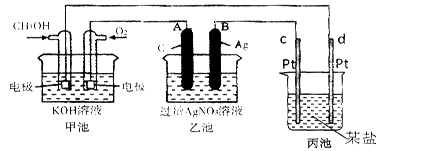
(1)图中乙池是 装置。
(2)c(Pt)电极的名称是 。
(3)写出通入CH3OH电极的电极反应式是 。
(4)乙池中反应的离子方程式为 。
(5)当乙池中B(Ag)极的质量增加5.40g时,甲池中理论上消耗O2 mL(标准状况下);此时丙池某电极析出1.6g某金属,则丙中的某盐溶液可能是 (填序号)
| A.MgSO4 | B.CuSO4 | C.NaCL | D.AgNO3 |
如图所示,甲、乙两装置电极材料都是铁棒与碳棒,请回答下列问题: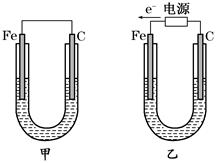
(1)若两装置中均为CuSO4溶液,反应一段时间后:
①有红色物质析出的是甲装置中的________棒,乙装置中的________棒。
②乙装置中阳极的电极反应式是:_______________________________。
(2)若两装置中均为饱和NaCl溶液:
①写出乙装置中总反应的离子方程式:__________________________________。
②甲装置中碳极的电极反应式是___________ _______,乙装置碳极的电极反应属于________(填“氧化反应”或“还原反应”)。
③将湿润的淀粉KI试纸放在乙装置碳极附近,发现试纸变蓝,解释其原因:
_______________________________________________________________________。
(6分)(1)甲醇可作为燃料电池的原料。以CH4和H2O为原料,通过下列反应来制备甲醇。
Ⅰ:CH4(g)+H2O(g) CO(g)+3H2(g)ΔH="+206.0" kJ·mol-1
CO(g)+3H2(g)ΔH="+206.0" kJ·mol-1
Ⅱ:CO(g)+2H2(g) CH3OH(g)ΔH="-129.0" kJ·mol-1
CH3OH(g)ΔH="-129.0" kJ·mol-1
CH4(g)与H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为 _____________。
(2)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后,将Co2+ 氧化成Co3+,然后以Co3+ 作氧化剂把水中的甲醇氧化成CO2而净化。实验室用如图装置模拟上述过程:
①写出阳极电极反应式 _______ 。
②写出Co3+除去甲醇的离子方程式 。
熔融盐燃料电池具有较高的发电效率,因而受到重视。某燃料电池以熔融的K2CO3(其中不含O2-和HCO-3)为电解质,以丁烷为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极。该燃料电池负极电极反应式为:2C4H10+26 CO32--52e-===34CO2+10H2O。
试回答下列问题:
(1)该燃料电池中发生氧化反应的物质是 。
(2)该燃料电池的化学反应方程式为 ;
(3)某学生想用该燃料电池电解饱和食盐水,写出反应的离子方程式 。
(4)当电路中通过0.26NA的电子时,消耗的氧气的体积(标况)为 ;此时电解饱和食盐水生成的氯气的物质的量是 ;若此时溶液体积为200ml,则生成的NaOH的物质的量浓度为 。
依据氧化还原反应:2Ag+(aq)+Cu(s)===Cu2+(aq)+2Ag(s)设计的原电池,如图所示。
请回答下列问题:
(1)电极X的材料是________;电解质溶液Y是________溶液。(填名称)
(2)银电极为电池的________极,发生的电极反应为____________________________;X电极上发生的电极反应为____________________________。
(3)外电路中的电子是从________极流向______极(填电极材料)。外电路中每通过0.1 mol电子,银电极的质量理论上增加 g。
(4)原电池工作时,盐桥(装有琼脂-KCl的U型管)里的Cl-移向 电极。
如下图是一个乙醇燃料电池工作示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题:
(1)M电极材料是 , N的电极反应式为 ,加入乙醇的铂电极的电极反应式为 。
(2)若在常温常压下,1g C2H5OH燃烧生成CO2和液态H2O时放出约为30kJ热量,表示乙醇燃烧热的热化学方程式为 。
(3)若M、N均为石墨电极,将乙池改为电解500mL含KNO3和Cu(NO3)2的混合液一段时间后,在两极上均生成11.2L(标准状况)气体。则M极产生的气体是H2,原混合液中Cu2+的物质的量浓度是 mol/L。
(14分)
(1)某课外兴趣小组用下图装置进行实验,
试回答:
①若开始时开关K与a连接,则A电极反应式为____________________。
②若开始时开关K与b连接,则A电极反应式为____________________。
③若开始时开关K与b连接,电路中通过0.2 NA个电子时,两极共产生 ____________mol气体
④若开关K与b连接,铁和石墨棒互换位置,描述U型管中观察到的现象:_____ _ 。
(2)如下图所示的装置,C、D、E、F都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。试回答以下问题:
①B是电源的 _极
②甲装置中D电极的电极反应式: _____________________________ 。
③欲用丙装置给铜镀银,G应该是 _ (填“银”或“铜”),电镀液的主要成分是(填化学式) 。
现有A、B、C、D和Cu五种金属片,将其分别用导线连接后浸入稀硫酸中(如下图),
每次实验时,通过灵敏电流计测出电子流动方向如下:
根据上述情况,回答下列问题:
(1)上述五种金属的活动性顺序是_____________________________。
(2)在①中,Cu片上观察到的现象是:_____________________________;
(3)在②中,溶液中H+向金属片________移动;
(4)在④中,两金属片上均无气泡放出。此时两金属片上的电极反应式分别为:
Cu:____________________________;B:_____________________________;
(5)如果实验⑤用B、D,则导线中电流方向为:_________(填B→D或D→B);
(6)已知反应:Cu+2Fe3+==Cu2++2Fe2+。请用下列试剂和材料,用上图所示装置,将此反应设计成原电池并检验正极产物。
试剂:CuCl2溶液、FeCl3溶液、FeCl2溶液、KSCN溶液、K3[Fe(CN)6]溶液、双氧水、NaOH溶液
材料:Cu片、Fe片、石墨棒
a、设计电池应选用的试剂和材料是:__________________________________;
b、检验正极产物选用的试剂是_______________________,
检验反应的离子方程式:________________________________________________。
按下图装置进行实验,并回答下列问题: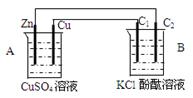
(1)判断装置的名称:A池为 B池为
(2)铜极的电极反应式为 石墨棒C2附近发生的实验现象为
(3)当C2极析出224mL气体(标准状况)时,锌的质量减少 g。
(1)家用液化石油气的主要成分之一是丁烷(C4H10),当10 kg丁烷完全燃烧并生成二氧化碳气体和液态水时,放出的热量为5×105 kJ。试写出丁烷燃烧的热化学方程式:
。
已知1mol液态水汽化时需要吸收44 kJ热量,则1mol丁烷完全燃烧生成二氧化碳气体和气态水时,放出的热量为 kJ。
(2)有同学制作一氢氧燃烧电池,通入H2的一极为 极。若以稀硫酸为电解质溶液时,其正极反应式为 。
(10分)为探究原电池和电解池的工作原理,某研究性小组分别用如图所示装置进行实验。
(1)甲装置中,a电极的反应式为________________________________________。
(2)乙装置中,阴极区产物为_________________________。
(3)丙装置是一种家用环保型消毒液发生器。外接电源a为_______(填“正”或“负”)极,该装置内发生反应的化学方程式为________________________________________________________。
(4)若甲装置作为乙装置的电源,一段时间后,甲中消耗气体与乙中产生气体的物质的量之比为____________(不考虑气体的溶解)。
试题篮
()