下图为一个原电池,完成下列问题:
(1)负极材料________,正极材料________,电解质溶液是________。
(2)写出电极反应式:负极:__________________________;
正极:___________________________。
(6分)按如图所示,两个烧杯中分别盛有足量的稀硫酸溶液和氯化铜溶液: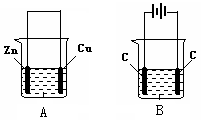
(1)A, B两个装置中,属于原电池的是 (填标号,下同)。
(2)B池中,右边C是 极,电极反应式为: ;
(3)A池中溶解了6.5g锌时,转移了 mol电子。
在Zn、Cu、稀硫酸组成的原电池中负极是 .正极反应式: , 电池总反应式:__ ___(离子方程式),电流从_ __极到__ 极,溶液中H+ 移向 _ _极,电池工作一段时间后电解质溶液PH值会变_ _
根据所学知识回答下列问题,在如图所示装置中 ,
,
(1)若烧杯中溶液为稀硫酸,则观察到的现象为 ,正极反应式为 ,负极反应式为 ,
该装置中的能量变化形式为 。
(2)若烧杯中溶液为氢氧化钠溶液,则负极为 。
请根据氧化还原反应Fe+2H+=Fe2++H2↑设计成原电池:
(1)负极材料为: 发生的电极反应是: ,电流 (填“流出”或“流入”)
(2)正极发生的电极反应是: 该反应为 (填“氧化反应”或“还原反应”)
(3)若电路中转移6.02×1022个e-,则产生标况下H2的体积为_ _。
原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)现有如下两个反应:A.NaOH+HCl=NaCl+H2O;B.Zn+H2SO4=ZnSO4+H2↑判断能否设计成原电池A. ,B. 。(填“能”或“不能”)
(2)将纯锌片和纯铜片按图方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题: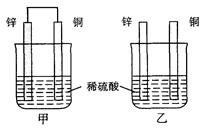
①下列说法正确的是 。
a.甲、乙均为化学能转变为电能的装置
b.乙中铜片上没有明显变化
c.甲中铜片质量减少、乙中锌片质量减少
d.两烧杯中溶液中的H+均减小
②在相同时间内,两烧杯中产生气泡的速度:甲 乙(填“>”、“<“或“=”)
③请写出图中构成原电池的负极电极反应式 。
电池工作时,溶液中SO42-向 极移动电池工作完成后,溶液中SO42-浓度 (填增大或减小或不变)。
原电池是一种 装置。电子的流动方向是从 极到 极;电流方向是从
极到 极,电工操作中规定,不能把铜线和铝线拧在一起连接线路,这是因为在潮湿的空气中,铜与铝接触形成 ,其中铝做 ,很快被腐蚀。
(13分)(1)A、B、C三个烧杯中分别盛有相同物质的量浓度的稀盐酸。
①B中Fe极的电极反应式为 。
②C中总反应化学方程式为 。
③比较A、B、C中铁被腐蚀的速率,由快到慢的顺序 。
(2)如图是甲醇燃料电池原理示意图,回答下列问题:
①电池的负极是________(填“a”或“b”),该极的电极反应是:_____________。
②电池工作一段时间后电解质溶液的碱性________(填“增大”、“减小”或“不变”)。
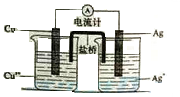
银是一种贵金属,古代常用于制造钱币及装饰器皿,现代在电池和照明器材等领域亦有广泛应用。回答下列问题。
(1)久存的银制器皿表面会变黑,失去银白色的光泽,原因是 。
(2)已知Ksp(AgCl)=1.8×10-10,若向50mL0.018mol·L-1的AgNO3溶液中加入50mL0.020mol·L-1的盐酸,混合后溶液中的Ag+的浓度为 mol·L-1,pH为 。
(3)AgNO3溶液光照易分解,生成Ag和红棕色气体等物质,其光照分解的化学方程式为 。
(4)下图所示原电池正极的反应式为 。
由A、B、C、D四种金属按下表中装置进行实验。
| 装置 |
 |
 |
 |
| 现象 |
二价金属A不断溶解 |
C的质量增加 |
A上有气体产生 |
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是______________________________________。
(2)装置乙中正极的电极反应式是_______________________________________。
(3)装置丙中溶液的pH________(填“变大”、“变小”或“不变”)。
(4)四种金属活动性由强到弱的顺序是___________________________________。
(8分)分别按下图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中G为电流计。请回答下列问题:
(1)以下叙述中,正确的是______。
| A.甲中锌片是负极,乙中铜片是正极 |
| B.两烧杯中铜片表面均有气泡产生 |
| C.两烧杯中溶液pH均增大 |
| D.产生气泡的速度甲中比乙中慢 |
E.乙的外电路中电流方向Zn→Cu
(2)变化过程中能量转化的形式主要是:乙为__________。
(3)在乙实验中,某同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是_________。
(4)在乙实验中,如果把硫酸换成硫酸铜溶液,请写出铜电极的电极反应方程式________________。
I.已知拆开1mol H—H键,1mol N三N键分别需要吸收的能量为436kJ,946kJ;形成1mol N—H键,会放出能量391kJ,在反应N2 + 3H2="=" 2NH3中,每生成2mol NH3 ___ _热量(填:吸收或放出)_____ kJ。
II.(6分)我国经济发展对能源的需求与日俱增。一种新型燃料电池是将两根特制电极插入氢氧化钾溶液中,然后从两极分别通入甲烷和氧气,其电极反应式为:
X极:CH4+10OH- -8e- ="=" CO32-+7H2O Y极:4H2O+2O2+8e- ==8OH-
(1)指出该电池的正极__________(X或Y)极
(2)在标准状况下,通入5.6L甲烷气体,完全反应后有__________mol电子转移;
(3)该电池的电解质溶液的PH变化是_______ ___(填升高、降低、不变)
III.(6分)利用Cu + 2FeCl3 = CuCl2 + 2FeCl2反应,设计一个原电池。
(1)画出装置图(在图中标出电极材料、正负极、电解质溶液)。
(2)写出电极反应方程式
负极: 正极:
某课外活动小组用如图装置进行实验,试回答下列问题。
(1)若开始时开关K与a连接,则B极的电极反应式为__________。
(2)若开始时开关K与b连接,则B极的电极反应式为____________,总反应的离子方程式为_________________________________。
(3)若开关K与b连接,下列说法正确的是(填序号)______________。
①溶液中Na+向A极移动
②从A极处逸出的气体能使湿润的KI淀粉试纸变蓝
③反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
④若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子
(4)如果模拟工业上离子交换膜法制烧碱的方法,将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,则电池正极的电极反应式为 。
试题篮
()