两串联电解池,左边放硫酸铜,右边放一定量的某硝酸盐溶液,电解时当左池有1.6g Cu析出时,右池析出0.45g固体,则右池溶质为:
| A.AgNO3 | B.NaNO3 | C.Mg(NO3)2 | D.Al(NO3)3 |
用惰性电极实现电解,下列说法正确的是
| A.电解氢氧化钠稀溶液,溶液浓度增大,pH变小 |
| B.电解氯化钠溶液,溶液浓度减小,pH不变 |
| C.电解硝酸银溶液,要消耗OH-,溶液pH变小 |
| D.电解稀硫酸,实质是电解水,溶液pH不变 |
某电解池内盛有CuSO4溶液,插入两根电极,接通直流电源后,欲达到如下要求:①阳极质量不变 ②阴极质量增加 ③电解液pH减小,则应选用的电极是
| A.阴、阳两极都用石墨棒 | B.铜作阳极,铁作阴极 |
| C.铁作阳极,铜作阴极 | D.铜作阳极,铂作阴极 |
500 mL KNO3和Cu(NO3)2的混合溶液中c(NO3-)=6.0 mol/L,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4 L气体(标准状况),假定电解后溶液体积仍为500 mL,下列说法正确的是
| A.电解后溶液中c(H+)为2 mol/L |
| B.上述电解过程中共转移2 mol电子 |
| C.电解得到的Cu的物质的量为0.5 mol |
| D.原混合溶液中c(K+)为2 mol/L |
电浮选凝聚法是工业上采用的一种污水处理方法:在污水中通电生成Fe(OH)3胶体,Fe(OH)3胶体可吸附污染物而沉积下来,具有凝聚净化的作用:电极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去浮渣层,即起到了浮选净化的作用。某研究小组用电浮选凝聚法处理污水,设计装置如图所示,下列说法不正确的是
| A.装置A中铁片为阳极,发生的电极反应是Fe-2e- = Fe2+ |
| B.装置B中通入空气的电极反应是O2+2CO2+4e- = 2CO32— |
| C.污水中加入适量的硫酸钠,可增强溶液的导电性,提高污水的处理效果 |
| D.标准状况下,若A装置中产生了44.8L气体,则理论上B装置中要消耗CH4为1.12L |
一些科学家采用高质子导电性的SCY陶瓷(能传递H+),实现了氨的电化学合成。该过程N2和H2的转化率远高于现在工业上使用的氨合成法。对于电化学合成氨的有关叙述正确的是
| A.N2在阴极上被氧化 |
| B.可选用铁作为阳极材料 |
| C.阳极的电极反应式是N2+6e-+6H+ = 2NH3 |
D.该过程的总反应式是N2+3H2 2NH3 2NH3 |
在一盛有饱和Na2CO3溶液的烧杯中插入惰性电极,保持温度不变,通电一段时间后:
| A.溶液的PH值增大 | B.Na+和CO32-的浓度减小 |
| C.溶液的浓度不变,有晶体析出 | D.溶液的浓度增大 |
下列叙述中,正确的是
①电解池是将化学能转变为电能的装置
②原电池是将电能转变成化学能的装置
③金属和石墨导电均为物理变化,电解质溶液导电是化学变化
④不能自发进行的氧化还原反应,通过电解的原理有可能实现
⑤电镀过程相当于金属的“迁移”,可视为物理变化
| A.①②③④ | B.③④ | C.③④⑤ | D.④ |
某课外兴趣小组进行电解原理的实验探究,做了如下的实验:以铜为电极,按如图所示的装置电解饱和食盐水。

实验现象:接通电源30 s内,阳极附近出现白色浑浊,之后变成橙黄色浑浊,此时测定溶液的pH约为10。一段时间后,试管底部聚集大量红色沉淀,溶液仍为无色。
查阅资料:
| 物质 |
氯化铜 |
氧化亚铜 |
氢氧化亚铜(不稳定) |
氯化亚铜 |
| 颜色 |
固体呈棕色,浓溶液呈绿色,稀溶液呈蓝色 |
红色 |
橙黄色 |
白色 |
*相同温度下CuCl的溶解度大于CuOH
下列说法错误的是
A.反应结束后最终溶液呈碱性
B.阴极上发生的电极反应为:2H2O + 2e¯ ═ H2↑+ 2OH¯
C.电解过程中氯离子移向阳极
D.试管底部红色的固体具有还原性
已知H2O2是一种弱酸,在强碱溶液中主要以HO2-形式存在。现以Al—H2O2燃料电池电解尿素[CO(NH2)2]的碱性溶液制备氢气 (电解池中隔膜仅阻止气体通过,c、d均为惰性电极)。下列说法正确的是
| A.燃料电池的总反应为:2Al+3HO2- = 2AlO2-+ 2H2O |
| B.电解时,Al消耗2.7g,则产生氮气的体积为1.12L |
| C.电极b是负极,且反应后该电极区pH增大 |
| D.电解过程中,电子的流向由a→d,c→b。 |
世界能源消费的90%以上依靠化学技术。
(1)工业制氢的一个重要反应是利用CO还原H2O(g)。已知:
C(石墨,s)+O2(g)═CO2(g)△H="-394k" J/mol
2C(石墨,s)+O2(g)═CO(g)△H="-222k" J/mol
H2(g)+ 1/2O2(g)═H2O(g)△H="-242k" J/mol
则CO还原H2O(g)的热化学方程式为_________________。
(2)氢能被视为最具发展潜力的绿色能源,写出碱式氢氧燃料电池的工作时的负极电极反应:_______。
(3)一种新型锂离子二次电池——磷酸铁锂(LiFePO4)电池。作为正极材料的磷酸铁锂在充、放电时的局部放大示意图如下图,写出该电池充电时的阳极电极反应__________。


(4)LiOH是制备锂离子电池正极材料的重要原料,其电解法制备装置如上图。气体a通入淀粉KI溶液中,发现溶液变蓝,持续一段时间后,蓝色逐渐褪去。则M极为电源的________(填“正”或“负”)极,B极区电解液为_______溶液(填化学式),该离子交换膜是________(填“阳”或“阴”)离子交换膜,解释蓝色褪去的原因______________________。
有序思维模式有利于解决复杂混合体系中的化学问题。下列反应先后顺序判断正确的是
| A.在含等物质的量的CO32-、OH-的溶液中,逐滴加入稀盐酸: OH-、CO32-、HCO3- |
| B.在含等物质的量的Al3+、NH4+的溶液中,逐滴加入NaOH溶液: Al3+、Al(OH)3、NH4+ |
| C.在含铁和铜的混合物中逐滴加入稀硝酸:Fe、Cu、Fe2+ |
| D.惰性电极电解含等物质的量Zn2+、Al3+溶液时阴极电极反应:Zn2+、Al3+、H+ |
下图所示的装置中,若通入直流电5 min时,铜电极质量增加2.16 g,试回答:
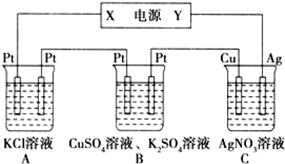
(1)电源电极X的名称为 。
(2)pH变化:A ,B ,C 。(填“增大”“减小”或“不变”)
(3)通电5 min后,B中共收集224 mL气体(标准状况),溶液体积为200 mL,则通电前CuSO4溶液的质的量浓度为 (设电解前后溶液体积无变化)。
(4)若A中KCl溶液的体积也是200 mL,电解后,溶液中OH-的物质的量浓度为 (设电解前后溶液体积无变化)。
海水中富含镁,可经过加碱沉淀、过滤、酸溶、结晶及脱水等步骤得到无水氯化镁,最后电解得到金属镁。已知25 ℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Fe(OH)3]= 1.0×10-38。 当溶液中离子浓度≤1.0×10-5 mol·L-1可视为沉淀完全。
(1)有浓度为1.8×10-3mol·L-1的MgCl2溶液,该溶液中含有少量Fe3+,当溶液中Fe3+沉淀完全时,Mg 2+ 是否开始沉淀 ,Mg(OH)2开始沉淀时溶液的pH为________。
(2)除去MgCl2酸性溶液中少量的FeCl3,可加入的试剂有 。
a.MgO b.Mg(OH)2 c.NH3·H2O d.MgSO4
(3)若在空气中加热MgCl2·6H2O,可生成Mg(OH)Cl或MgO,写出生成Mg(OH)Cl或MgO相关的化 学方程式 。
(4)MgCl2·6H2O在干燥的HCl气流中加热可得到无水氯化镁,其原因是 。
(5)电解熔融的MgCl2,阳极的电极反应式为: 。
试题篮
()