ACV浓缩饮料曾风靡全美,当时美国《环球时报》也曾报道 ACV具有解毒、降脂、减肥和止泻等多种疗效。ACV浓缩饮料中,苹果酸M(相对分子质量为134)是主要的活性物质,其化学成分及相关信息如下:
①含碳35.82%(质量分数,下同),含氢 4.51%,其余为氧元素;
②各取0.134g苹果酸M分别与足量NaHCO3反应放出CO2 44.8mL(标准状况,下同),与足量金属钠反应放出H2 33.6 mL。
③M分子中所有碳原子在同一链线上,无支链。
请回答下列问题:
(1)M的化学式为 ,分子中含的官能团名称是 、 。
(2)为制备M,化学工作者从某气态烃与溴蒸气的取代产物分离出一种饱和的多溴代烃N,然后经多步反应,最后合生成M。合成路线为:
N →有机物A →有机物B →有机物C → M
其中B能发生银镜反应。则:
①有机物N的结构简式为 ;
②有机物C转化为M的反应类型为 。
③A转化为B的化学方程式为 。
(3)实验证明M分子间可形成多种具有水果香味的化合物,若其中某化合物分子中含有七元环,则其结构简式为 。
(4)M有多种同分异构体,其中能同时满足下列条件的结构简式为 。(已知: )
)
①1mol该有机物与足量金属钠反应生成0.5mol H2;
②经核磁共振检测,分子中含有3种不同环境的氢原子;
③1mol该有机物与足量NaOH溶液共热时,最多消耗3molNaOH,并生成两种钠盐。
在某有机物A的分子其结构简式如图,请回答

(1)写出有机物A中官能团的名称: 。
(2)A跟足量NaOH溶液反应的化学方程式是: 。
(3)两分子的A以羧基和酚羟基分子间成环的结构简式为 。
(4)以A为单体利用羧基和醇羟基形成高分子缩聚产物的方程式为 。
羟基扁桃酸是药物合成的重要中间体,它可由苯酚和乙醛酸反应制得 
下列有关说法正确的是
| A.该反应是取代反应 |
B. 和羟基扁桃酸是同系物 和羟基扁桃酸是同系物 |
| C.每个羟基扁桃酸分子中最多有个17原子共平面 |
| D.1 mol羟基扁桃酸最多分别能和1molNaHCO3、2molNaOH、3molNa、4molH2发生反应 |
(6分) A是芳香烃的含氧衍生物。为了测定其分子组成,进行如下实验:
①在一定温度和压强下将A气化,其气体的质量是同温、同压下等体积氦气质量的38倍;②称取7.6gA,在11.2L氧气中完全燃烧,其产物只有CO2和水蒸气。将反应后的混合气 通过浓硫酸后体积为10.64L,浓H2SO4质量增加3.6g。再将余下的气体通过盛有足量Na2O2的干燥管后,气体体积减少至6.16L(气体体积均在标准状况下测定)。试回答:
(1)A的分子式为 ;
(2)A物质苯环上只有一取代基,遇FeCl3溶液无显色反应。1molA只能与1molNaHCO3反应;1molA与足量Na反应生成1molH2。则A的结构简式为 ;
(3)A与足量钠反应的化学方程式是 。
乙醛在氧化铜催化剂存在的条件下,可以被空气氧化成乙酸。依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体)。已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全。有关物质的沸点见下表:
| 物质 |
乙醛 |
乙酸 |
甘油 |
乙二醇 |
水 |
| 沸点 |
20.8℃ |
117.9℃ |
290℃ |
197.2℃ |
100℃ |

请回答下列问题:
(1)试管A内在60℃~80℃时发生的主要反应的化学方程式为(注明反应条件)____________________________________;
(2)如图所示在实验的不同阶段,需要调整温度计在试管A内的位置,在实验开始时温度计水银球的位置应在_____________;目的是____________________;当试管A内的主要反应完成后温度计水银球的位置应在___________________,目的是_____________________________;
(3)“烧杯B”这种加热方式的优点是___________________________;烧杯B内盛装的液体可以是____________(写出一种即可,在题给物质中找);
(4)若想检验试管C中是否含有产物乙酸,请你在所提供的药品中进行选择,设计一个简便的实验方案。所提供的药品有:pH试纸、红色的石蕊试纸、白色的醋酸铅试纸、碳酸氢钠粉末。实验仪器任选。该方案为
____________________________________________ _____________________。
下列关于有机物的叙述正确的是
| A.棉花和合成纤维的主要成分都是纤维素 |
| B.蛋白质溶液中加入浓的硫酸铵溶液会发生变性 |
| C.乙酸乙酯中混有的乙酸杂质可以用饱和碳酸钠溶液除去 |
D.由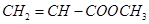 合成的聚合物为 合成的聚合物为 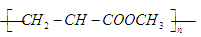 |
如图在试管甲中先加入2mL乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2克无水乙酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管乙中加入5ml 饱和的碳酸钠溶液,按图连接好装置,用酒精灯对试管甲小加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验。试回答:
(1)该实验中长导管的作用是 ,其不宜伸入试管乙的溶液中,原因是 。
(2)试管乙中饱和Na2CO3的作用是①除去乙酸乙酯中的乙醇和乙酸,②
(3)试管乙中观察到的现象是 。
(4)试管甲中加入浓硫酸的目的是 ①催化剂,吸水剂②
(5)液体混合加热时液体体积不能超过试管容积的 ,本实验反应开始时用小火加热的原是 ;(填字母)A.加快反应速率B. 防止了反应物未来得及反应而挥发损失(已知乙酸乙酯的沸 点为77℃;乙醇的沸点为78.5℃;乙酸的沸点为117.9℃)
将 转变为
转变为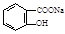 的方法为( )
的方法为( )
| A.与足量的NaOH溶液共热后,再通入CO2 |
| B.溶液加热,通入足量的HCl |
| C.与稀H2SO4共热后,加入足量的Na2CO3溶液 |
| D.与稀H2SO4共热后,加入足量的NaOH溶液 |
甲、乙、丙三位同学,分别在相同条件下用乙酸与乙醇反应来制取乙酸乙酯,但未用饱和Na2CO3溶液来吸收。
(1)甲、乙、丙同学将得到的酯提纯,在未用指示剂的情况下,他们都先加NaOH中和过量的酸,然后用蒸馏法将酯分离出来。但得到的结果却不同:①甲得到了不溶于水的中性酯;②乙得到显酸性的酯;③丙得到大量水溶性物质。试分析产生上述各种现象的原因。
(2)丁同学为了进一步找出原因,将所得产物进行了分离探究,他的实验操作步骤流程
如下图。请你帮他完成该实验并填写下列空白。
分离出的物质名称:A ,B ,C ,D ,E ;
选择的试剂:a ,b ;
分离物质的方法:① ,② ,③ 。
对于能水解的链状有机物C4H6O2,下列说法正确的是
| A.该物质不能使溴的CC14溶液褪色 | B.该物质一定不能发生取代反应 |
| C.该物质可能的结构共有5种. | D.该物质与C2H4O2可能互为同系物 |
乙二酸,又称草酸,通常在空气中易被氧化而变质。其两分子结晶水(H2C2O4·2H2O)却能在空气中稳定存在。在分析化学中常用H2C2O4·2H2O做KMnO4的滴定剂,下列关于H2C2O4的说法正确的是
A.草酸是二元弱酸,其电离方程式为H2C2O4 2H++C2O 2H++C2O |
| B.草酸滴定KMnO4属于中和滴定,可用石蕊做指示剂 |
| C.乙二酸可通过乙烯经过加成、水解、氧化再氧化制得 |
| D.将浓H2SO4滴加到乙二酸上使之脱水分解,分解产物是CO2和H2O |
下列与有机物的结构、性质有关的叙述正确的是( )
| A.苯、油脂均不能使酸性KMnO4溶液褪色 |
| B.甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应 |
| C.葡萄糖、果糖的分子式均为C6H12O6,二者互为同分异构体 |
| D.乙醇、乙酸均能与Na反应放出H2,二者分子中官能团相同 |
【有机化学基础】
白酒产品中的塑化剂主要源于塑料接酒桶、塑料输酒管、成品酒塑料内盖等。DBP是塑化剂的一种,可由下列路线合成: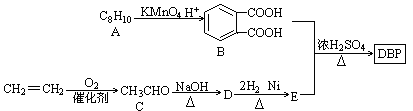
已知以下信息:
(1)A的结构简式是________,D的结构简式是________,D→E的反应类型是________。
(2)D和H2l:l反应生成E,则E官能团名称为________,DBP的分子式为________。
(3)由B和E以物质的量比1:2合成DBP的化学方程式为____________。
(4)写出同时符合下列条件的B的所有同分异构体的结构简式____________。
①能和NaHCO3溶液反应生成CO2③能使FeCl3溶液发生显色反应
②能发生银镜反应 ④苯环上含碳基团处于对位
(5)写出B与碳酸氢钠溶液反应的化学方程式________。
写出C生成D的反应的化学方程式________。
近年来流行喝苹果醋。苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等作用的保健食品。苹果酸( 一羟基丁二酸)是这种饮料的主要酸性物质,其结构如下图所示:
一羟基丁二酸)是这种饮料的主要酸性物质,其结构如下图所示: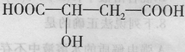
下列相关说法正确的是
| A.苹果酸在一定条件下能发生消去反应 |
| B.苹果酸在一定条件下能催化氧化生成醛 |
| C.苹果酸在一定条件下能发生加聚反应生成高分子化合物 |
| D.l mol苹果酸与NaHCO3溶液反应最多消耗3 mol NaHCO3 |
试题篮
()