通过粮食发酵可获得某含氧有机化合物X,其相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13.0% .
(1)X的电子式是 ;
(2)X与金属钠反应放出氢气,反应的化学方程式是 (有机物用结构简式表达);
(3)X与空气中的氧气在铜或银催化下反应生成Y,Y的结构简式是 ;Y能发生银镜反应,Y与银氨溶液的反应的化学方程式是: 。
(10分)分子式为C2H6O的化合物A具有如下性质:
A+Na―→慢慢产生气泡
A+CH3COOH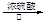 有香味的产物
有香味的产物
(1)根据上述信息,对该化合物可作出的判断是( )。
| A.一定含有—OH | B.一定含有—COOH |
| C.A为乙醇 | D.A为乙酸 |
(2)含A的体积分数为75%的水溶液可以用作___________________
(3)A与钠反应的化学方程式:__________________
(4)化合物A和CH3COOH反应生成的有香味的产物的结构简式为________。
(5)A可由含淀粉[(C6H10O5)n]的农产品如玉米、小麦、薯类等经发酵、蒸馏而得。请写出淀粉水解的化学方程式:__________________
在某有机物A的分子中,其结构简式如下图。
(1)A跟NaOH溶液反应的化学方程式是
(2)A跟NaHCO3溶液反应的化学方程式是
(3)A在一定条件下跟Na反应的化学方程式是:
苹果酸是一种常见的有机酸,其结构简式为:
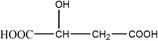
(1)苹果酸含有的官能团名称是__________、__________,在一定条件下,苹果酸可发生化学反应的类型有 (填序号)。
a.水解反应 b.缩聚反应 c.加聚反应 d.中和反应
(2)写出苹果酸与足量金属钠发生反应的化学方程式:__________________________。
(3)1mol苹果酸与足量碳酸钠充分反应生成的气体在标准状况下体积为__________。
苹果醋(ACV)是一种由苹果发酵而成的酸性饮品,具有解毒、降脂等药效。苹果醋是一种常见的有机酸,其结构简式为:

(1)苹果醋中含有的官能团的名称是 ;
(2)苹果醋的分子式为 ;
(3)1 mol苹果醋与足量金属钠反应,能生成标准状况下的氢气 L;
(4)苹果醋可能发生的反应是 。
| A.与NaOH溶液反应 | B.与石蕊溶液作用 |
| C.与乙酸在一定条件下酯化 | D.与乙醇在一定条件下反应 |
【改编】(1)曲酸是一种非常有潜力的食品添加剂,经测定曲酸的分子式为C6H6O4,结构简式为 ,其所含有的官能团有(写结构简式)____________________。
,其所含有的官能团有(写结构简式)____________________。
推测曲酸不可能具有的性质为_______。
| A.能发生酯化反应 | B.易溶于水、醇 |
| C.具有抗氧化性 | D.具有强酸性 |
(2)L-多巴用于帕金森综合症的治疗,其结构简式为 。这种药物的研制是基于获得2000年诺贝尔生理学和医学奖的研究成果。L-多巴分子中所含的官能团的名称是________。
。这种药物的研制是基于获得2000年诺贝尔生理学和医学奖的研究成果。L-多巴分子中所含的官能团的名称是________。
甲醇作为基本的有机化工产品和环保动力燃料具有广阔的应用前景,二氧化碳加氢合成甲醇是合理利用二氧化碳的有效途径。由二氧化碳制备甲醇过程中可能涉及反应如下:
反应Ⅰ:CO2(g)+3H2(g)  CH3OH(g)+H2O(g) △H1=-49.58KJ/mol
CH3OH(g)+H2O(g) △H1=-49.58KJ/mol
反应Ⅱ:CO2(g)+H2(g) CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2
反应Ⅲ:CO(g)+2H2(g) CH3OH(g) △H3=-90.77KJ/mol
CH3OH(g) △H3=-90.77KJ/mol
回答下列问题:
(1)反应Ⅱ的△H2= ,反应Ⅰ自发进行条件是 (填“较低温”、“较高温”或“任意温度”)。
(2)在一定条件下3L恒容密闭容器中,充入一定量的氢气和二氧化碳仅反应反应Ⅰ,实验测得反应物在不同起始投入量下,
体系中二氧化碳的平衡转化率与温度的关系曲线,如图1所示。
① 氢气和二氧化碳的起始的投入量以A和B两种方式投入
A:n(H2)=3mol n(CO2)=1.5mol
B:n(H2)=3mol n(CO2)=2mol,曲线Ⅰ代表哪种投入方式 (用A、B表示)
②在温度为500K的条件下,按照A方式充入3摩尔氢气和1.5摩尔二氧化碳,该反应10分钟时达到平衡:A.此温度下的平衡常数为 ;500K时,若在此容器中开始充入0.3摩尔氢气和0.9摩尔二氧化碳、0.6摩尔甲醇、x摩尔水蒸气,若使反应在开始时正向进行,则x应满足的条件是 。
b.在此条件下,系统中甲醇的浓度随反应时间的变化趋势如图2所示,当反应时间达到3分钟时,迅速将体系温度升至600K,请在图2中画出3~10分钟内容器中甲醇的浓度变化趋势曲线。

(3)固体氧化物燃料电池是一种新型的燃料电池,它是以固体氧化锆氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过,该电池的工作原理如图3所示,其中多孔电极均不参与电极反应。图3是甲醇燃料电池的模型。

①写出该燃料电池的负极反应式 。
②如果用该电池作为电解装置,当有16g甲醇发生反应时,则理论上提供的电量最多为 摩尔。
某课外小组同学拟用乙醇分解法制乙烯,并对该反应进行探究。
(1)实验室制取乙烯的化学方程式为: ;
实验过程中,可观察到混合液变黑,产生有刺激性气味的气体。某研究小组同学经分析、讨论后认定:此现象是在该反应条件下,浓硫酸与乙醇发生氧化还原反应所致。
(2)为证明产物中混有SO2、CO2气体,甲同学设计了如下实验装置
他认为,只要观察到品红褪色,澄清石灰水变浑浊,就可确证混合气体中一定存在有SO2、CO2。你认为此看法是否正确 (填“是”或“否”),理由是 。
(3)为探究乙烯与Br2的反应,乙同学将制取的乙烯气体分别通过: NaOH溶液, Ba(OH) 2溶液,后用排水法收集于1000 mL的圆底烧瓶中(塞好橡皮塞),然后打开橡皮塞,向烧瓶中一次性加入1.5 mL液溴,塞上配有带乳胶管(用止水夹夹紧)的尖嘴玻璃管,摇荡,可观察到瓶内红棕色逐渐消失。然后按下图装好装置,打开止水夹,可观察到有喷泉形成,静置一段时间后,在溶液下部,有一层无色油状液体(约1.5 mL)。
①将乙烯气体通过Ba(OH) 2溶液的目的是 ;
②用化学方程式和简单的文字表述说明产生喷泉的原因_____________ ; ;
③请利用上述喷泉实验反应的产物设计一个简单实验,证明乙烯与Br2发生的是加成反应而不是取代反应 。
烯丙醇是一种无色有刺激性气味的液体,是重要的有机合成原料,其结构简式为CH2=CH—CH2OH。请回答:
(1)烯丙醇的分子式为 ;烯丙醇中除碳碳双键外还含有官能团的是 。
(2)0.3mol 烯丙醇与足量金属钠反应,能生成标准状况下的氢气 L。
(3)写出烯丙醇与溴水反应的化学方程式 ,
(4)烯丙醇与CH3CO18OH发生酯化反应的化方程式为 ,酯化反应生成的产物在一定条件下可以发生加聚反应得到高分子化合物,其结构简式为 。
下表给出了ABCDE五种有机物的有关信息
请根据表中信息回答下列问题:
(1)将A通入到少量的溴的四氯化碳溶液中,主要现象是____________________。
(2)B分子的空间构型为___________________。
(3)实验室用C制取少量的A的反应条件为:以浓硫酸作催化剂、温度为_______℃。
(4)C与E发生反应的化学方程式为_______________________________。
(5)D与新制的氢氧化铜的悬浊液反应的化学方程式为___________________________。
(6)E的一种同分异构体F既能在NaOH溶液中发生水解反应,又能与银氨溶液反应,则F的结构简式为______________________。
(1)乙醇的分子结构如右图: ,其中①②③④⑤表示化学键的代号,用代号回答:
,其中①②③④⑤表示化学键的代号,用代号回答:
i乙醇与钠反应断裂的键是_
ii乙醇与氧气在铜或银作催化剂,加热条件下反应断裂的键是
(2)把一端弯成螺旋状的铜丝放在酒精灯外焰部分加热,看到铜丝表面变成 色。趁热将它反复插入盛乙醇的试管中,铜丝表面又变成 色,并有 气味的物质生成,总反应的化学方程式 。
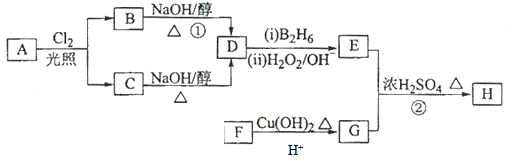
化合物H可用以下路线合成:
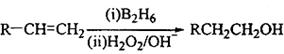
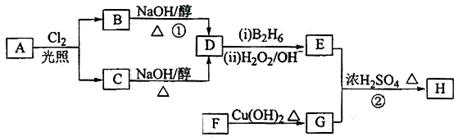 已知:
已知: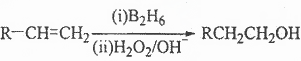
回答下列问题:
(1)11.2L(标准状况)的烃A在氧气中充分燃烧可以生成88gCO2和45gH2O,且A分子结构中有3个甲基,则A的名称(系统命名)为 ;
(2)B和C均为一氯代烃,则反应(1)的反应类型为 ;
(3)在催化剂存在下1molF与2molH2反应,生成3—苯基—1—丙醇。F的结构简式 。
(4)反应②的化学方程式为 ;
(5)与G具有相同官能团的芳香类同分异构体共有 种(不包括G),写出其中任意两种_____________、___________。
已知A、B、C、D都是含有碳、氢、氧三种元素的有机物,其中A、C分别是白酒和食醋中含有的成分,A、B、C、D间有如下转化关系: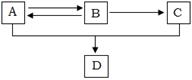
请回答下列问题:
(1)B物质中官能团为 。
(2)写出A与C在浓H2SO4存在条件下加热反应生成D的化学方程式: 。
试题篮
()