在下列中学化学中常见物质的转化关系图中,反应条件及部分反应物和产物未全部注明,已知A.D为金属单质,其他为化合物。试推断:
(1)写出下列物质的化学式:A:________B:________G:________
(2)写出下列反应的化学方程式或离子方程式:
C→F的离子方程式________________________________________
C→E的化学方程式________________________________________
H→I的化学方程式________________________________________
α-松油醇的合成路线如下:

可供选择的试剂:① Br2 ② H2 ③ O2
已知:

请回答:
(1)试剂1是 ,试剂2是 。
(2)A至H中,能发生银镜反应的是 。
(3)D和G的结构简式分别是:D ;G 。
(4)E转化为F的化学方程式是 。
(5)F转化为H的化学方程式是 。
(1)有A、B、C、D四种均含有铝元素的化合物,它们之间存在如下的反应关系:
① A+NaOH=D+H2O ② B=A+H2O ③C+NaOH(适量)="B+NaCl" ④C+D+H2O=B+NaCl
则A是 、C是 (填化学式)
(2)实验室用加热二氧化锰和浓盐酸制氯气,离子方程式
若生成标况下2.24 L Cl2,则被氧化的HCl的物质的量为 。
[有机化学基础]
某药物可通过以下方法合成:

注:非诺洛芬是一种治疗类风湿性关节炎的药物。请回答下列问题:
(1)非诺洛芬中的含氧官能团为 和 (填名称)。
(2)反应①中加入的试剂X的分子式为C8H8O2,X的结构简式为 。
(3)在上述五步反应中,属于取代反应的是 (填序号)。
(4)B的一种同分异构体满足下列条件:
Ⅰ.能发生银镜反应,其水解产物之一能与FeCl3溶液发生显色反应。
Ⅱ.分子中有6种不同化学环境的氢,且分子中含有两个苯环。
写出该同分异构体的结构简式: 。
(5)根据已有知识并结合相关信息,写出以 为原料制备
为原料制备 的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:

化合物F是合成抗过敏药孟鲁司特钠的重要中间体,其合成过程如下: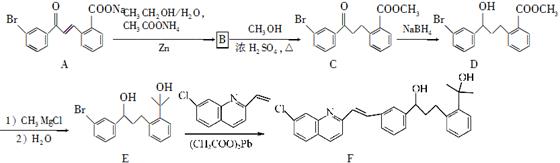
请回答下列问题:
(1)化合物C中含氧官能团为________、________(填名称)。
(2)化合物B的分子式为C16H13O3Br,则B的结构简式为____________。
(3)由C→D、E→F的反应类型依次为________、________。
(4)写出符合下列条件C的一种同分异构体的结构简式:______________。
Ⅰ.属于芳香族化合物,且分子中含有2个苯环;
Ⅱ.能够发生银镜反应;
Ⅲ.分子中有5种不同环境的氢原子。
(5)已知:RCl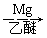 RMgCl,写出以CH3CH2OH、
RMgCl,写出以CH3CH2OH、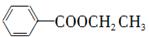 为原料制备
为原料制备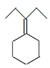 的合成路线流程图(乙醚溶剂及无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图(乙醚溶剂及无机试剂任用)。合成路线流程图示例如下:
H2C=CH2 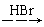 CH3CH2Br
CH3CH2Br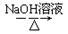 CH3CH2OH
CH3CH2OH
通过学习铁和铁的化合物的一些化学性质, 完成下列问题。
(1)高温下,铁粉与水蒸气反应的化学方程式是 ;
其中 为氧化剂。
(2)

①往A溶液中分别滴入几滴KSCN溶液,溶液A的颜色变化 。将A的饱和溶液滴入沸水中并不断加热,可制得 胶体;当光束通过该胶体时,可看到一条光亮的“通路”,这种现象称为
效应。
②写出上述过程中有关反应的离子方程式:
Fe2O3→A ;A→B 。
③C在空气中发生变化的现象是 。
我国女药学家屠呦呦因创制新型抗疟药青蒿素和双氢青蒿素而获得2015年诺贝尔生理学或医学奖。青蒿素的一种化学合成方法的部分工艺流程如图所示:



己知:①C6H5-表示苯基; ②
(1)化合物E中含有的含氧官能团有 、 和羰基(写名称)。
(2)1 mol化合物B最多可与_____________molH2发生加成反应。
(3)合成路线中设计E—→F、G-→H的目的是
(4)反应B→C,实际上可看作两步进行,依次发生的反应类型是 、_ __ _ 。
(5)A在Sn-p沸石作用下,可生成同分异构体异蒲勒醇,己知异蒲勒醇分子中有3个手性碳原子(连有四个不同基团的碳原子称为手性碳原子),异蒲勒醇分子内脱水后再与1分子H2发生1,4-加成可生成 则异蒲勒醇的结构简式为:
则异蒲勒醇的结构简式为:
(6)下图以乙烯为原料制备苄基乙醛 的合成路线流程图。
的合成路线流程图。

请填写下列空白(有机物写结构简式):
物质1为 ;物质2为 ;试剂X为 .条件3为 。
前四周期原子序数依次增大的六种元素A、B、C、D、E、F中,A、B属于同一短周期元素且相邻,A元素所形成的化合物种类最多,C、D、E、F是位于同一周期的金属元素,基态C、F原子的价电子层中未成对电子均为1个,且C、F原子的电子数相差为10,基态D、E原子的价电子层中未成对电子数分别为4、2,且原子序数相差为2。
(1)六种元素中第一电离能最小的是_____________(填元素符号,下同)
(2)黄血盐是由A、B、C、D四种元素形成的配位化合物C4[D(AB)6],易溶于水,广泛用作食盐添加剂(抗结剂)。请写出黄血盐的化学式___ _,1molAB一中含有π键的数目为__ ______ (阿伏加德罗常数的值为NA),黄血盐晶体中各种微粒间的作用力不涉及____ (填序号)。
a .金属键. b.共价键 c.配位键 d.离子键 e.氢键 f.分子间的作用力
(3)E2+的价层电子排布图为 ,很多不饱和有机物在E催化下可与H2发生加成反应:如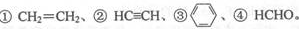 其中碳原子采取sp2杂化的分子有 (填物质序号),HCHO分子的立体结构为 ,它加成后产物甲醇的熔、沸点比CH4的熔、沸点高,其主要原因是 。
其中碳原子采取sp2杂化的分子有 (填物质序号),HCHO分子的立体结构为 ,它加成后产物甲醇的熔、沸点比CH4的熔、沸点高,其主要原因是 。
(4)金属C、F晶体的晶胞结构如图(请先判断对应的图),C、F两种晶体晶胞中金属原子的配位数之比为_ ___ 。金属C的晶胞中,若设该晶胞的密度为ag/cm3,阿伏加德罗常数的值为NA,C原子的摩尔质量为M g/mol,则表示C原子半径的计算式为 cm(不必化简)。
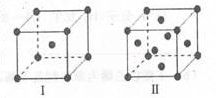
(以下化学反应关系转化图中,A的焰色反应呈黄色,E、F为有刺激性气味的气体,F也是造成酸雨的主要成分,G为强酸性溶液,H为既难溶于水、也难溶于稀酸的白色固体。试回答:

(1)写出化学式:A ;B 。
(2)写出下列反应的化学方程式或离子方程式:
① C→E(化学方程式):
② D+E+H2O→H(化学方程式):
③ E+F+H2O→G(离子方程式):
(3)C溶液电解的另一气体产物的燃烧热为285.8kJ/mol,写出该物质燃烧的热化学方程式: 。
(4)将F气体通入品红溶液中的现象是 ,由此现象说明F气体具有的性质是 。
某废金属屑中主要成分为Cu、Fe、Al,还含有少量的铜锈[Cu2(OH)2CO3]、少量的铁锈和少量的氧化铝,用上述废金属屑制取胆矾(CuSO4·5H2O)、无水AlCl3和铁红的过程如下图所示: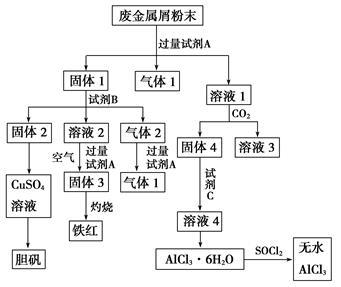
请回答:
(1)在废金属屑粉末中加入试剂A,生成气体1的反应的离子方程式是_________________。
(2)溶液2中含有的金属阳离子是__________;气体2的成分是______________。
(3)溶液2转化为固体3的反应的离子方程式是____________________________。
(4)利用固体2制取CuSO4溶液有多种方法。
①在固体2中加入浓H2SO4并加热,使固体2全部溶解得CuSO4溶液,反应的化学方程式是___________。
②在固体2中加入稀H2SO4后,通入O2并加热,使固体2全部溶解得CuSO4溶液,反应的离子方程式是_____________________________。
(5)溶液1转化为溶液4过程中,不在溶液1中直接加入试剂C,理由是__________________
(6)直接加热AlCl3·6H2O不能得到无水AlCl3。SOCl2为无色液体,极易与水反应生成HCl和一种具有漂白性的气体。AlCl3·6H2O与SOCl2混合加热制取无水AlCl3,反应的化学方程式是______________。
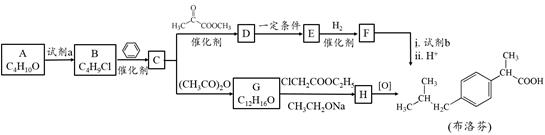
解热、镇痛药物布洛芬的两种合成路线如下:
已知: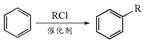 (R为烃基)
(R为烃基)
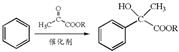 (R为烃基)
(R为烃基)
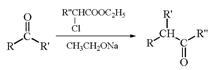 (R、R’、R’’为烃基或氢原子)
(R、R’、R’’为烃基或氢原子)
(1)A为醇,其核磁共振氢谱有四个吸收峰。A的结构简式是 。
(2)A与试剂a反应生成B的反应类型是 。
(3)由B生成C的化学方程式是 。
(4)D与E的相对分子质量相差18,由D生成E的化学反应方程式是 。
(5)G的结构简式是 ,H的含氧官能团的名称是 。
(6)布洛芬有多种同分异构体,写出满足下列条件的任意两种同分异构体的结构简式 。
a. 羧基与苯环直接相连 b. 苯环上有三个取代基,且苯环上的一氯代物有两种
某化学小组用淀粉制取食品包装高分子材料B和具有果香味的物质D。其转化关系如下:

(1) C6H12O6名称是 ;A的电子式是 。
(2)写出下列反应方程式:
①淀粉一C6H12O6:
②C—D:
(3)写出常温下能与NaHCO3溶液反应的D的所有同分异构体的结构简式:
已知有以下物质相互转化,其中A为常见金属, C为碱。试回答:
(1)写出E的化学式__________,H的化学式___________。
(2)写出由E转变成F的化学方程式:______________________。
(3)向G溶液加入A的有关离子反应方程式:__________________。
(4)写出A在一定条件下与水反应的化学方程式:___________________。
由中学化学常见元素组成的单质A、B、C和甲、乙、丙、丁、戊五种化合物有下图所示转化关系,A是由地壳中含量最多的金属元素组成的。请回答:
(1)写出下列物质的化学式:乙_______、丁_______、戊_______。
(2)写出甲物质在工业上的一种主要用途:_______。
(3)写出甲→乙+丙反应的离子方程式:____________,A→乙+C反应的化学方程式____________。
下表是A、B、C、D、E五种有机物的有关信息;
| A |
B |
C |
D |
E |
①能使溴的四氯化碳溶液褪色;②比例模型为: ,③能与水在一定条件下反应生成C ,③能与水在一定条件下反应生成C |
①由C、H两种元素组成;②球棍模型为: |
①由C、H、O三种元素组成;②能与Na反应,但不能与NaOH溶液反应;③能与E反应生成相对分子质量为100的酯. |
①相对分子质量比C少2;②能由C氧化而成; |
①由C、H、O三种元素组成;②球棍模型为: |
根据表中信息回答下列问题:
(1)A与溴的四氯化碳溶液反应的生成物的名称为 ;写出在一定条件下,A生成高分子化合物的化学反应方程式 。
(2)写出B在浓硫酸作用下,与浓硝酸反应的化学方程式 。
(3)C与E反应能生成相对分子质量为100的酯,其化学反应方程式为 。
(4)写出由C氧化生成D的化学反应方程式 。
试题篮
()