A、B是中学化学里常用的物质,其中B是单质,A是化合物;F是红棕色气体,I是红褐色沉淀。它们之间相互反应以及生成物之间的转化关系如图所示。已知,I、L两种物质中除了含不同价态的B元素外,还都含另外两种相同的元素(这两种元素的原子序数均小于18)。请回答:

(1)B和A的浓溶液在常温下难反应,原因是_____________。但加热后,却可以,请写出反应的化学方程式: 。
(2)写出F和G相互转化的化学方程式:
F→G ;
A→H 。
(3)L转化成I的现象是 ;有关的化学方程式 。
正盐A能发生下图所示的反应,图中①~⑧分别代表有关反应中的一种物质(某些物质已略去),其中①、②、④、⑤为无色气体。

请完成下列各题:
(1)写出化学式A ⑥ ⑦
(2)写出下列反应方程式:
⑧+⑦ ②+③+⑥:
②+③+⑥:
①+④ ⑤:
⑤:
(3)⑧ ⑤的离子方程式为:
⑤的离子方程式为:
以下是由甲苯合成乙酰水杨酸和酚酞的合成路线。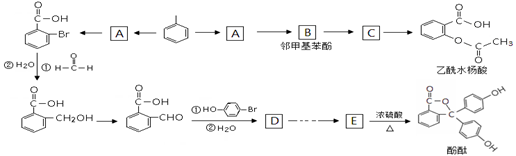
(1).写出“甲苯→A”的化学方程式_____________________________。
(2).写出C的结构简式___________,E分子中的含氧官能团名称为___________。
(3).上述涉及反应中,“E→酚酞”发生的反应类型是______________。
(4).写出符合下列条件的乙酰水杨酸的一种同分异构体的结构简式___________。
①遇FeCl3溶液显紫色
②能与碳酸氢钠反应
③苯环上只有2个取代基的
④能使溴的CCl4溶液褪色。
(5).写出乙酰水杨酸和NaOH溶液完全反应的化学方程式:
___________________________________________________。
(6).由D合成E有多步,请设计出D→E的合成路线(有机物均用结构简式表示)。
(合成路线常用的表示方式为:D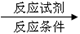 ……
…… E)
E)
_________________________________________________________。
X、Y、Z三种短周期元素,它们的原子序数之和为16。X、Y、Z三种元素常见单质在常温下都是无色气体,在适当条件下可发生如下图所示变化:

已知一个B分子中含有的Z元素的原子个数比C
分子中的少一个。请回答下列问题:
(1)Y单质分子的电子式为 。
(2)X的单质与Z的单质可制成新型的化学电源(KOH溶液作电解质溶液),两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电,则正极通入 (填物质名称或化学式均可);负极电极反应式为 。
(3)已知Y的单质与Z的单质生成C的反应是可逆反应,将等物质的量的Y、Z的单质充入一密闭容器中,在适当催化剂和恒温、恒压条件下反应。下列说法中,正确的是__________(填写下列各项的序号)。
a.达到化学平衡时,正反应速率与逆反应速率相等
b.反应过程中,Y的单质的体积分数始终为50%
c.达到化学平衡时,Y、Z的两种单质在混合气体中的物质的量之比为1:1
d.达到化学平衡的过程中,混合气体平均相对分子质量逐渐减小
A—J是中学化学常见的物质,它们之间的转化关系如下图所示(部分产物已略去)。已知A是一种高熔点物质,D是一种红棕色固体。

请回答下列问题:
(1)A物质的名称为________________;
(2)C与D在高温下的反应在冶金工业上称为 反应,C与D反应的化学方程式: 。
(3)写出G→J的化学方程式:___ ;
写出J→D的化学方程式: ;
(4)A→H的离子方程式为_____________________________;
(5)用离子方程式表示I物质能用于净水的原理___________ _。
聚合物F的合成路线图如下:


请据此回答:
(1) A中含氧官能团名称是_______,C的系统命名为_________。
(2) 检验B中所含官能团所用的试剂有______;E→F的反应类型是___________。
(3) G物质的相对分子质量比 的相对分子质量大2,则符合下列条件的G的同分异构体有__ __种。
的相对分子质量大2,则符合下列条件的G的同分异构体有__ __种。
① 分子中含有苯环,且苯环上有两个取代基 ② 遇氯化铁溶液变紫色
(4) C生成D的反应化学方程式为_____________________________,如果C与NaOH的醇溶液反应,则生成的有机物的结构简式为_______________。
(5) 参照上述合成路线,设计一条由甲醛、乙醛和甲醇为主要原料制备  的合成路线 。
的合成路线 。
互为同分异构体的有机物A、B、C的分子式均为C5H8O2,其中A为直链结构,加热时能与新制的氢氧化铜浊液反应,生成砖红色物质;A分子中核磁共振氢谱图中有三组峰,且峰面积之比为2:1:1。B为五元环酯。C的红外光谱表明其分子中存在甲基。A~I等有机物的转化关系如下:
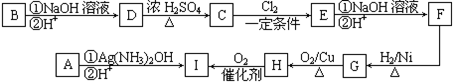
已知:烯烃在一定条件下可与卤素单质发生a—H原子的取代反应。

(1)A、B的结构简式分别是:A ,B 。
(2)C为反式结构,其结构式为 。
(3)写出下列反应的化学方程式;
D→C: 。
G→H: 。
(4)写出下列反应类型:
F→G ,A→I中的① 。
(5)写出F发生加聚反应生成的产物的结构简式 。
(6)与A的官能团组成和个数均相同的同分异构体还有 个。
有一包白色固体粉末,可能含有K2SO4、Na2CO3、NH4Cl、BaCl2、CuSO4中的一种或几种,按以下步骤进行实验:
①取少量固体粉末加到足量水中,得到无色溶液;
②取①中溶液少量继续往其中加入足量稀硫酸,有气泡产生;
③继续向②中的溶液加Ba(NO3)2溶液,有白色沉淀生成;
④取①中溶液少量,加入NaOH溶液并加热,产生刺激性气味的气体,并用湿润的红色石蕊试纸检验气体,试纸变蓝。
根据以上事实判断:
(1)肯定存在的是______________。
(2)肯定不存在的是____________。
(3)不能确定是否存在的是_____________。请简述证明该物质是否存在的实验方案(实验方法、现象、结论)__________________________。
(4)写出上述实验④中产生刺激性气味反应的离子方程式:_____________________。
华北地区雾霾时有发生,这与汽车尾气、工业生产排放的大量有害气体有关。下列反应中,B、C是空气质量监测的物质,其中C是红棕色气体,D是强酸(部分反应条件和产物已略去)。
A →B →C → D
(1)若A是气体单质,则A生成B的化学方程式为___________ 。
(2)若A为气态氢化物且水溶液呈碱性,则A的化学式为___________,写出A在生产生活中的一种用途_____________。
(3)D的浓溶液与铜反应的化学方程式为____________,在此反应中体现了硝酸_______性和_______性。
短周期元素形成的纯净物A、B、C、D、E,五种物质之间的转化关系如图1所示,物质A与物质B之间的反应不在溶液中进行(E可能与A、B两种物质中的一种相同).
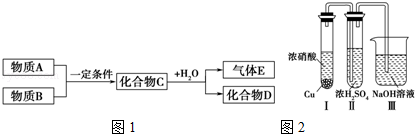
请回答下列问题:
(1)若C是离子化合物,D是一种强碱,则C的化学式 ,并任写一种C的主要用途 .
(2)若E的水溶液呈弱酸性,D是既能溶于强酸、又能溶于强碱的化合物.
①用电离方程式解释D既能溶于强酸、又能溶于强碱的原因(仅写出电离方程式即可): .
②用电荷守恒的等式表示E与NaOH溶液反应生成正盐的溶液中所有离子的浓度之间的关系: .
(3)若C是一种气体,D是一种强酸,则:
①C与水反应的化学方程式为 .
②已知常温下物质A与物质B反应生成1mol气体C的△H=﹣57kJ•mol﹣1,1mol气体C与H2O反应生成化合物D和气体E的△H=﹣46kJ•mol﹣1,写出物质A与物质B及水反应生成化合物D的热化学方程式为 .
③有人认为“浓H2SO4可以干燥气体C”.某同学为了验证该观点是否正确,用如图2所示装置进行实验.
实验过程中,在浓H2SO4中未发现有气体逸出,则得出的结论是 .
④用铂做电极电解H2SO4的溶液,其阳极的电极反应式为 .
某溶液中可能存在下列离子:NH4+、Fe2+、Cl-、SO42-、CO32-中的一种或几种,某同学为了检验它们的存在,进行了如下实验:
①取少量该溶液加入过量的Ba(NO3)2溶液,产生白色沉淀,过滤,得沉淀和滤液;
②向①的沉淀中加入足量的稀硝酸,发现沉淀不溶解;
③向①的滤液中加入硝酸银溶液,未见白色沉淀;
④再取少量原溶液加入2滴KSCN溶液,无明显现象,继续加入氯水,溶液立即变为血红色。
(1)则原溶液中一定存在的离子是______________;
(2)一定不存在的离子是______________;
(3)可能存在的离子是_________,为进一步确定该离子是否存在,该同学还应补做的实验是___________。
下列框图所示的物质转化关系中,甲是日常生活中常见的金属,乙、丙、丁是常见的气体单质。气体B与气体C相遇产生白烟,A是强碱,D的焰色反应呈紫色(部分反应物和生成物及溶剂水已略去)。
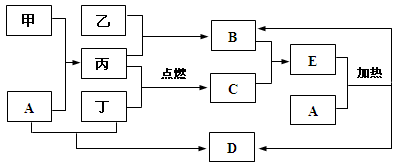
请回答下列问题:
(1)D的化学式为 。
(2)C的电子式为 。
(3)写出A溶液和甲反应的离子方程式: 。
(4)写出工业上制备B的化学方程式: 。
萜品醇可作为消毒剂、抗氧化剂、医药和溶剂。合成α-萜品醇G的路线之一如下:

已知:
请回答下列问题:
(1) 试剂Y的结构简式为________________。
(2) A催化氢化得Z(C7H12O3),写出Z在一定条件下聚合反应的化学方程式____________。
(3) B的分子式为___________;写出同时满足下列条件的B的链状同分异构体的结构简式:________________。
① 核磁共振氢谱有2个吸收峰 ② 能发生银镜反应
用CO2 和环氧化物共聚合成全降解二氧化碳基塑料,既可有效解决CO2过量排放引起的温室效应、又可除去白色污染。已知该反应为:

(-R、-R'代表烃基或氢原子)
(1)该反应为 反应。
(2) 的单体是 。
的单体是 。
通过下列途径既可以得到全降解二氧化碳基塑料还可得到用途广泛的高分子化合物PA66。
已知:

(3)A、B、C分子均为直链结构,且A、B的核磁共振氢谱都只有两个峰,峰面积之比为1:2,则
①A的结构简式是____________,名称是 。
②B是顺式结构, B→C的化学方程式是 。
③由E制备二氧化碳基塑料的化学方程式是 。
(4)D的一种同分异构体在相同条件下也能制得E,其结构简式是 。
(5)已知1 molG可与NaHCO3溶液反应产生44.8LCO2(标准状态下),则
①1 mol E与2 mol HCl反应的化学方程式是 ___________________。
② G和H在一定条件下生成PA66的化学方程式是 。
已知 X、Y、Z、Q、R、E六种元素中,原子序数X<Y<Z<Q<R<E,其结构或性质信息如下表。
| 元素 |
结构或性质信息 |
| X |
原子的L层上s电子数等于p电子数。 |
| Y |
原子核外的L层有3个未成对电子。 |
| Z |
在元素周期表的各元素中电负性仅小于氟。 |
| Q |
单质常温、常压下是气体,原子的M层上有1个未成对的p电子。 |
| R |
核电荷数是Y与Q的核电荷数之和 |
| E |
原子序数比R大3 |
请根据信息回答有关问题:
(1)元素Y的原子核外共有 种不同运动状态的电子,有 种不同能级的电子。
(2)X、Y、Z三种元素的电负性由高到低的排列次序依次为(写元素符号) 。
(3)X、Z、Q元素均表现最低化合价时的三种氢化物中,沸点由高到低的排列次序依次为(写化学式) 。
(4)R的最高化合价为 。R的一种配合物的化学式为RCl3·6H2O。已知0.01 molRCl3·6H2O在水溶液中用过量硝酸银溶液处理,产生0.02 mol AgCl沉淀。此配合物最可能是 。
A.[R(H2O)6]Cl3 B.[R(H2O)5Cl]Cl2·H2O
C.[R(H2O)4Cl2]Cl·2H2O D.[R(H2O)3Cl3]·3H2O
(5)元素E能形成八面体构型的配合物离子[E (YH3) x Q 2]+,则中心离子为(写化学式) ,配位体为(写化学式) ,x 的值为 。
(6)Y的最低价氢化物与Z的一种氢化物反应,生成的两种产物均不污染环境,其反应的化学方程式为 。
试题篮
()