推理是根据已有的事实与结论推出新的判断的思维方法。下列根据已有事实或结论进行的推理正确的是( )
|
选项 |
事实或结论 |
推理或判断 |
|
A |
酸性溶液pH小于 7 |
pH小于7的溶液一定是酸性溶液 |
|
B |
碱能使无色酚酞溶液变红 |
能使无色酚酞溶液变红的一定是碱 |
|
C |
酸与碱反应生成盐和水 |
生成盐和水的反应一定是酸与碱的反应 |
|
D |
氧化物中都有氧元素 |
含有氧元素的化合物都是氧化物 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
“宏观—微观—符号—量”是科学特有的表征物质及其变化的方法。2022年4月16日,神舟十三号载人飞船圆满完成飞行任务。火箭助推器使用偏二甲肼和四氧化二氮作为推进剂,燃烧时发生反应的微观示意图如图,下列说法不正确的是( )
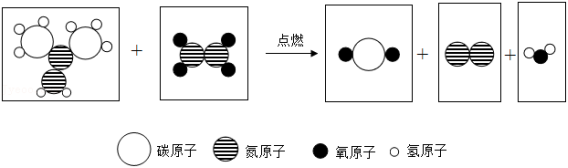
| A. |
从量的角度看:反应前后原子总数减少 |
| B. |
从微观构成看:氮气是由氮分子构成的 |
| C. |
从符号表征看:四氧化二氮的化学式是 |
| D. |
从宏观物质看:燃烧产物中含有单质与化合物两类物质 |
科学以实验为基础,规范操作是科学实验取得成功的关键。下列实验操作规范的是( )
| A. |
|
B. |
|
| C. |
|
D. |
|
学习小组用已知浓度的氢氧化钠溶液测定某硫酸溶液的浓度。取该硫酸溶液20g,滴加10%的氢氧化钠溶液,恰好完全反应时,共消耗氢氧化钠溶液40g。计算:
(1)消耗的 溶液中溶质的质量为 g;
(2)该硫酸溶液的溶质质量分数。(温馨提示: )
有一包白色粉末,可能由 、 、 、 、 中的一种或几种组成,为确定其成分,某化学兴趣小组进行如下实验探究,请你参与探究并回答相关问题。
【提出问题】该白色粉末的成分是什么?
【查阅资料】
(1)部分物质在水中的溶解性表(室温):
|
物质 |
|
|
|
|
|
溶解性 |
溶 |
不溶 |
微溶 |
不溶 |
(2) 不稳定,在溶液中分解生成难溶于水的物质。
【实验探究】
|
实验步骤 |
实验现象及结果 |
实验结论 |
|
①取该白色粉末样品于烧杯,加足量水溶解。 |
样品全部溶解,得到无色溶液A |
白色粉末中不含 |
|
②取少量无色溶液A于试管,加入过量 溶液,充分反应后过滤。 |
得到无色溶液B和白色沉淀C |
白色粉末中含有 |
|
③向白色沉淀C中加入过量稀盐酸。 |
沉淀部分溶解,并有气泡冒出 |
|
|
④在无色溶液B中滴加几滴 溶液。 |
产生白色沉淀 |
白色粉末中含有 |
【交流与解释】
(1)白色沉淀C中加入过量的稀盐酸,产生气泡的反应方程式为 。
(2)在老师的指导下,通过讨论,同学们认识到由上述实验探究尚不能得出白色粉末中含有 ,理由是 。
为了进一步确定白色粉末中是否含有 ,继续进行如下探究。
【继续探究】
|
实验步骤 |
实验现象 |
实验结论 |
|
⑤另取少量无色溶液A于试管中,加入过量的 溶液,振荡,静置。 |
产生白色沉淀 |
白色粉末中含有 |
|
⑥取实验⑤所得上层清液于试管,加入 溶液。 |
产生白色沉淀 |
通过上述实验探究,确定了该白色粉末的成分。
【拓展与反思】在混合溶液中,检验某种离子时,需排除离子间的相互干扰。
化学是一门以实验为基础的科学。请结合图示回答问题:

(1)仪器①的名称为 。
(2)实验室用高锰酸钾制取氧气的化学方程式为 。用B、E装置制取并收集氧气,实验操作步骤有:①点燃酒精灯,待气泡连续均匀放出时收集气体;②熄灭酒精灯;③装入药品,放置棉花并固定仪器;④连接好装置,检验装置的气密性;⑤从水槽中撤出导管。正确的操作顺序是 (填标号)。
a.③④①②⑤
b.④③①⑤②
c.④③①②⑤
d.③④①⑤②
(3)进行铁丝在氧气中燃烧的实验,集气瓶底部加入水或细沙的目的是 。
(4)实验室用锌粒和稀硫酸制取氢气,应选择的发生装置是 (填标号,下同),可选择的收集装置是 (填一种即可)。
(5)现有一新制的碳酸钙产品,某同学设计如图所示的实验,通过测定反应生成的 的质量来确定该产品中 的含量(图中夹持仪器已略去,杂质不与盐酸反应,碱石灰是 和 的固体混合物)。

①关闭止水夹,打开分液漏斗活塞,缓慢滴加盐酸至不再有气泡产生,关闭分液漏斗活塞;打开止水夹,缓缓通入空气。通入空气的作用是 。
②装置D的作用是 。
③实验时,称取的碳酸钙产品的质量为 ,反应后得到 的质量为 ,则该产品中 的质量分数为 (用含 和 的代数式表示)。
氨既是一种重要的化工产品,又是一种重要的化工原料。如图为合成氨以及以氨为原料制硝酸的流程示意图。
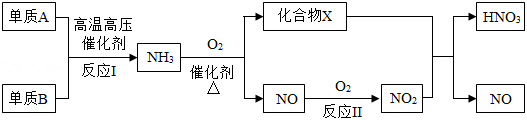
(1)化合物X是一种常见溶剂,其化学式是 。
(2)反应Ⅱ属于 反应(填基本反应类型)。
(3)反应Ⅰ的化学方程式是 。
金属及金属材料广泛应用于生产、生活及科学实验,其应用推动了社会的发展。
(1)下列实验中,铜片上的白磷燃烧,说明铜具有 性;黄铜片和纯铜片相互刻画,纯铜片上留下刻痕,说明黄铜的硬度比纯铜的硬度 (填“大”或“小”)。

(2)铁在潮湿的空气中容易生锈,写出一种防止铁制品生锈的具体方法 。
(3)春秋战国时期,我国就开始生产和使用铁器。工业上用赤铁矿(主要成分 )和一氧化碳反应炼铁的化学方程式为 。
(4)某同学对含 、 、 的混合溶液进行探究,流程如下(M表示一种金属元素):
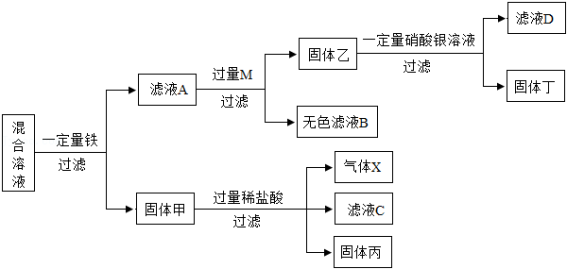
根据实验探究流程,回答下列问题:
①气体X的化学式为 ;
②金属 、 、 、 的活动性由强到弱的顺序是 。
③滤液D中所含溶质的成分可能有 种情况。
2022年3月22日是第三十届“世界水日”,其主题为“珍惜地下水,珍视隐藏的资源”。
(1)地下水是 (填“混合物”或“纯净物”)。
(2)实验室制取蒸馏水时,在烧瓶中加入几粒沸石或碎瓷片的目的是 。实验结束,可加入 比较水蒸馏前后的硬度变化。
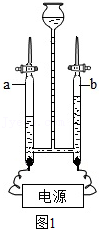
(3)宇航员一部分生活用氧可通过电解水制得。如图1是电解水的实验示意图,玻璃管 (填“a”或“b”)中的气体能使带火星的木条复燃。该实验说明水是由 组成的。
(4)机场、车站等公共场所设有许多直饮水机,能将自来水进一步净化处理得到可直接饮用水,其处理水的过程如图2所示。
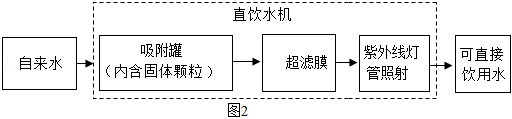
吸附罐中固体颗粒的主要作用是吸附杂质,固体颗粒可选用 ,紫外线灯管照射的作用是 。
(5)图3是我国“国家节水标志”,用一句话谈谈你对该标志的理解或得到的启示 。

化学就在我们身边,人类的生产、生活离不开化学。
(1)从下列选项中选择一种适当的物质填空(填标号)。
A.钛合金
B.医用酒精
C.碳酸氢钠
①可用 擦拭物品消毒;
②可用 治疗胃酸过多症;
③可用 制造人造骨骼。
(2)目前,人类使用的燃料大多来自化石燃料,化石燃料属于 (填“可再生”或“不可再生”)能源。分别取1kg天然气和煤充分燃烧,产生的 和 气体的质量如图所示, 和 中会导致酸雨的是 ,图中更清洁的燃料是 。
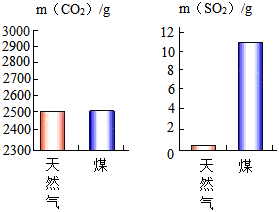
(3)第24届冬季奥运会的火炬“飞扬”以液氢为燃料,体现了绿色奥运的理念。目前,在生活和生产中大量使用氢能源还存在一定的困难,原因是 (填一条即可)。
(1)化学用语是最简明、信息丰富、国际通用的语言。请用化学用语填空:
①氦元素 ;
②镁离子 ;
③2个过氧化氢分子 ;
④某化合物中,同种元素呈现不同的化合价,该化合物可以是 。
(2)下列化学符号中,数字“3”可表示不同的含义,其中表示一个离子所带电荷数的是 (填标号,下同),表示一个分子中所含原子个数的是 。
①
②
③
④
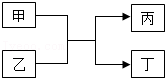
甲、乙、丙、丁是初中化学常见的物质,在一定条件下它们之间的转化关系如图所示。下列推断中正确的个数有( )
①甲、乙、丙、丁可能含有同一种元素
②若甲为单质,则此反应一定是置换反应
③若丙为氯化钠,则甲、乙中一定有碱
④若丙为 ,则甲可能为单质、氧化物、酸、碱或盐
| A. |
1个 |
B. |
2个 |
C. |
3个 |
D. |
4个 |
为探究硝酸钾的溶解性,进行了如图实验(实验过程如图)
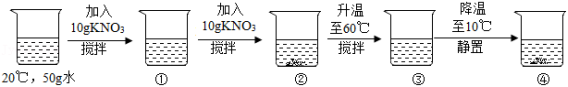
结合硝酸钾在不同温度下的溶解度,判断下列说法不正确的是( )
|
温度/℃ |
10 |
20 |
30 |
40 |
50 |
60 |
|
溶解度/g |
20.9 |
31.6 |
45.8 |
63.9 |
85.5 |
110.0 |
| A. |
①③中的溶液均为不饱和溶液 |
| B. |
②③中溶液的质量:③>② |
| C. |
②③④中溶液的溶质质量分数:③>②>④ |
| D. |
④中析出晶体的质量是0.9g |
下列实验方案设计不正确的是( )
|
选项 |
实验目的 |
实验方案 |
|
A |
鉴别涤纶纤维和羊毛纤维 |
分别灼烧,闻气味 |
|
B |
鉴别 固体和 固体 |
分别加熟石灰研磨,闻气味 |
|
C |
检验 溶液是否完全变质 |
取样,滴加石灰水,再滴加酚酞溶液 |
|
D |
除去 中的水蒸气 |
将混合气体通过盛有浓硫酸的洗气装置 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
试题篮
()