图1、图2、图3是初中化学常见的实验,据图回答下列问题。

(1)图1是测定空气中氧气含量的实验。待红磷熄灭并冷却至室温,打开弹簧夹,观察到烧杯内的 , 约占集气瓶空气体积的 时,说明空气中的氧气被消耗了,消耗氧气的体积约占空气体积的 。
(2)图2是木炭与氧化铜反应的实验装置图。因为木炭与氧化铜的反应条件是 ,所以图中装置用 的酒精灯加热试管,才能达到实验目的。
(3)图3是有关氢氧化钙性质的验证实验。用药匙的柄把一端挑一点氢氧化钙粉末于试管中,依次进行图中的实验。③号试管中观察到的现象是 ,由此得出氢氧化钙微溶于水且氢氧化钙溶液能与酚酞溶液作用;④号试管中观察到的现象是 ,由此得出氢氧化钙能与稀盐酸发生反应。
利用下图装置进行实验(两支玻璃管内径相同).实验前K 1、K 2、K 3均已关闭。
| 实验装置 |
【实验1】制备气体 |
【实验2】测定空气中氧气含量 |
| |
左管中带孔的燃烧匙盛有足量锌粒,右管盛有稀硫酸 Ⅰ.打开K 1和K 2,使反应发生 Ⅱ.在K 1的导管口处收集气体 Ⅲ.… |
左管中燃烧匙盛有足量白磷,右管盛有水 Ⅰ.光照引燃白磷 Ⅱ.待白磷熄灭,冷却,打开K 2,至液面不再变化,右管中液体的高度为h 1 |
(1)实验1:锌与稀硫酸反应的化学方程式为 ;为使反应停止,Ⅲ中的操作是 。
(2)实验2:打开K 2,右管中液面下降,原因是 ;计算空气中氧气体积分数的表达式为 (用h 0、h 1表示)。
(1)为测定空气中氧气的含量,某课外活动小组对课本上的实验做了如下改进:如图1所示,在一个注射器和装有较多铜丝的硬质玻璃管内共封闭80mL空气,然后给硬质玻璃管加热,并缓慢向右推动注射器的活塞,至硬质玻璃管内铜丝变黑且较长时间内无进一步变化时停止加热,待剩余气体冷却至室温,请回答:
①实验前,检查本装置气密性的一种方法是:先固定注射器的活塞,再用酒精灯加热硬质玻璃管,可观察到 ,说明气密性良好。
②实验结束后,注射器内气体的体积减少了约 mL,这是因为 。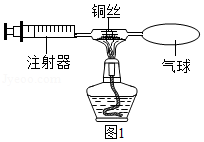
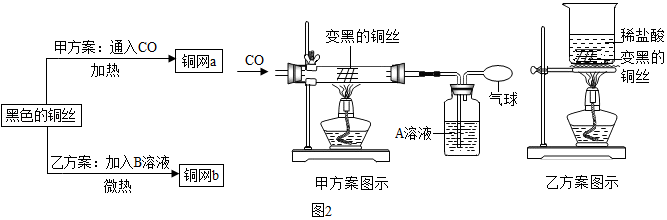
①甲方案的玻璃管中实验现象是 。乙方案的烧杯中发生反应的化学方程式是 。
②甲方案实验过程中,操作步骤正确的是 (填序号)。
A.实验开始时,先通入CO,再加热;实验结束时,先停止加热,再停止通入CO
B.实验开始时,先加热,再通入CO;实验结束时,先停止加热,再停止通入CO
C.实验开始时,先通入CO,再加热;实验结束时,先停止通入CO,再停止加热
D.实验开始时,先加热,再通入CO;实验结束时,先停止通入CO,再停止加热
③两种方案相比,乙方案更好,其原因是 。
磷的燃烧反应在生产生活中有着广泛的应用价值。
(1)红磷在空气中燃烧能冒出浓厚的白烟,军事上常用来制烟幕弹。红磷燃烧的化学方程式为 。
(2)某同学利用燃磷法测量空气中氧气含量,实验过程如图。他测得氧气体积分数约是 %.燃烧结束试管里剩余气体主要是 (填化学式)。

利用气体压强的变化是完成实验的重要手段,各图装置气密性均良好。
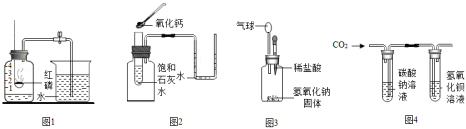
下列说法正确的是( )
| A. |
图1红磷燃烧过程中弹簧夹未夹紧,则测得空气中氧气的体积分数偏小 |
| B. |
图2向试管中加入氧化钙后,石灰水中溶质质量减小,玻璃弯管左侧液面降低 |
| C. |
图3向广口瓶中滴入稀盐酸后,气球变大,说明氢氧化钠和盐酸反应放热 |
| D. |
图4氢氧化钡溶液变浑浊,说明通入的二氧化碳与氢氧化钡发生了反应 |
小文同学利用长柄W形玻璃管,完成了课本上多个化学实验.
(1)燃烧条件的探究与空气中氧气含量的粗略测定
①燃烧条件的探究:在如图1所示装置(省略夹持仪器,下同)中,向W形玻璃管中放入足量红磷和白磷,塞好橡皮塞,关闭活塞,然后将其放入80℃的热水中,观察到红磷不燃烧而白磷燃烧,说明可燃物发生燃烧应具备的条件是 .
②空气中氧气含量的粗略测定:为减小测量误差,待火焰熄灭后,将玻璃管 ,再打开活塞.
(2)一氧化碳与氧化铁反应
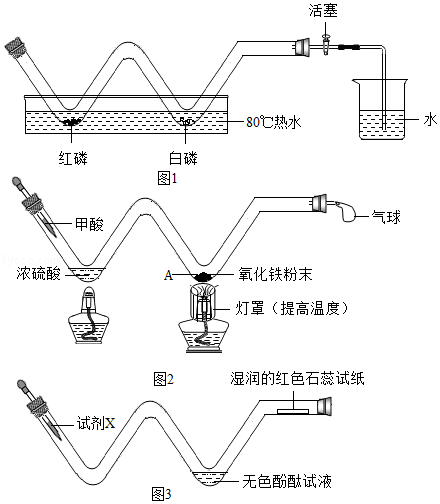
①甲酸(HCOOH)在热浓硫酸的作用下,分解生成一氧化碳和水,该反应的化学方程式是 .
②实验时,A处可以观察到的现象是 .
(3)探究微粒的性质
向玻璃管左端加入试剂X,观察到无色酚酞试液变红,湿润的红色石蕊试纸变蓝,试剂X可能是 ,该装置的优点有 (答1点).
(1)为测定空气中氧气的含量,某课外活动小组对课本上的实验做了如下改进:如图1所示,在一个注射器和装有较多铜丝的硬质玻璃管内共封闭80mL空气,然后给硬质玻璃管加热,并缓慢向右推动注射器的活塞,至硬质玻璃管内铜丝变黑且较长时间内无进一步变化时停止加热,待剩余气体冷却至室温,请回答:
①实验前,检查本装置气密性的一种方法是:先固定注射器的活塞,再用酒精灯加热硬质玻璃管,可观察到 ,说明气密性良好。
②实验结束后,注射器内气体的体积减少了约 mL,这是因为 。

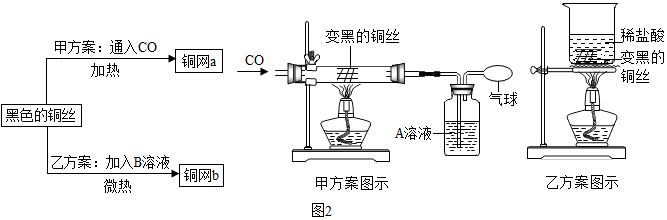
①甲方案的玻璃管中实验现象是 。乙方案的烧杯中发生反应的化学方程式是 。
②甲方案实验过程中,操作步骤正确的是 (填序号)。
A.实验开始时,先通入CO,再加热;实验结束时,先停止加热,再停止通入CO
B.实验开始时,先加热,再通入CO;实验结束时,先停止加热,再停止通入CO
C.实验开始时,先通入CO,再加热;实验结束时,先停止通入CO,再停止加热
D.实验开始时,先加热,再通入CO;实验结束时,先停止通入CO,再停止加热
③两种方案相比,乙方案更好,其原因是 。
实验室用燃烧法测得空气中氧气的含量,最适宜选用的可燃物是( )
| A. |
红磷 |
B. |
硫磺 |
C. |
木炭 |
D. |
蜡烛 |
下列装置都可用于测定空气里氧气的含量,a、b两物质的选择正确的是( )

A.a是铜,b是红磷B.a是铜,b是木炭
C.a是汞,b是红磷D.a是汞,b是木炭
下列有关实验现象的描述错误的是 ( )
A.测定空气中氧气的体积分数时,铜粉与氧气加热生成黑色粉末氧化铜
B.灼烧羊毛有烧焦羽毛的气味
C.铵态氮肥与草木灰等碱性物质混合加热,产生有刺激性气味的气体
D.淀粉遇碘变蓝色
化学兴趣小组设计如图所示的装置测定空气中氧气的含量,胶头滴管中的水滴入生石灰一段时间后,试管内的白磷(白磷的着火点为40℃)开始燃烧,待白磷熄灭并冷却至室温后打开弹簧夹。下列关于该实验的说法错误的是( )

| A. |
试管中的细沙可防止试管炸裂 |
| B. |
胶头滴管中的水和注射器中的水作用相同 |
| C. |
若实验测得氧气的体积分数偏低,可能是试管中白磷的量不足 |
| D. |
若注射器中的水最终减少了10mL,说明空气中氧气的体积分数约为20% |
实验是科学探究的重要方式,请结合图示回答下列问题:
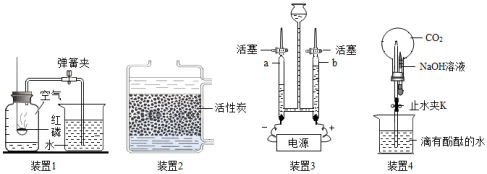
(1)装置1常用于实验室测定空气中氧气含量。请写出红磷燃烧的化学方程式 。
(2)装置2中的活性炭有 性,可用于净化水;常用 区别硬水和软水,生活中常用 的方法降低水的硬度。
(3)装置3常用于实验室电解水,与电源正极相连的玻璃管中收集的气体是 ;此实验可以证明水是由 组成的。
(4)装置4可用于研究CO2与NaOH溶液的反应。关闭弹簧夹K,将NaOH溶液全部挤入烧瓶,振荡;然后打开弹簧夹K。观察到的实验现象: 形成美丽喷泉,写出该反应的化学方程式 。
实验是进行科学探究的重要手段。根据如图回答问题:
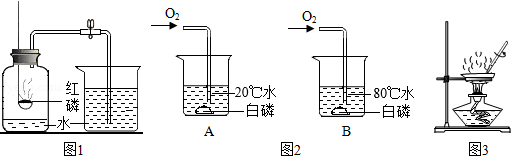
(1)图1是测定空气中氧气含量的实验。由该实验得出关于空气中氧气含量的结论是 。
(2)图2是探究燃烧条件的实验。A中白磷不燃烧,B中白磷燃烧,说明可燃物燃烧的条件之一是 。
(3)图3是蒸发食盐水的实验。其中玻璃棒的作用是 。
下列是初中化学常见的实验。请回答下列问题
(1)图A所示实验结束后,进入集气瓶中水的体积小于瓶内原气体体积的五分之一,造成该现象的原因是 (答出一条即可)。
(2)图B所示实验观察到木屑先燃烧,燃烧的顺序说明燃烧的条件之一是 。
(3)图C所示实验不能验证质量守恒定律的原因是 。
(4)配制一定质量分数的氯化钠溶液,按图D所示量取溶剂,其他操作均正确,最终导致配制的溶液溶质的质量分数 (填“偏大”、“偏小”或“不变”)。
试题篮
()