室温为25℃时,某小组用无水氯化铜粉末制备氯化铜大晶体,制备过程如下:
步骤I:查阅资料,得到氯化铜溶解度数据如下
| 温度(℃) |
0 |
20 |
25 |
40 |
50 |
60 |
80 |
| 溶解度(g) |
69.2 |
74.5 |
76.4 |
81.8 |
85.5 |
89.4 |
98.0 |
步骤Ⅱ:配制少量CuCl 2热饱和溶液,冷却结晶,得到晶种。
步骤Ⅲ:把晶种悬挂在新配制的CuCl 2热饱和溶液中,室温下静置数天,形成大晶体。
步骤Ⅳ:取出大晶体,处理剩余的溶液(母液)。
根据以上信息,回答下列问题:
(1)用20mL蒸馏水(密度约为1g/mL)配制50℃的氯化铜饱和溶液。
①计算需称取CuCl 2的质量是 g。
②将称取的CuCl 2固体和20mL水倒入烧杯中, (填操作名称),直至固体完全溶解。
(2)母液中Cu 2+属于重金属离子,随意排放将导致环境污染。下列方法可用于母液处理的是 。
A.收集母液于敞口容器中,用报纸包住容器口,待水分自然蒸干后保存所得固体
B.向母液中加入适量AgNO 3,充分反应后过滤,滤渣干燥保存,滤液倒入下水道
C.向母液中加入适量NaOH,充分反应后过滤,滤渣干燥保存,滤液倒入下水道
(3)若用铁粉置换出母液中的铜,100g母液需要铁粉的质量至少是 g(只列计算式,已知CuCl 2的相对分子质量为135)。
如图是实验室制备气体的部分装置。

(1)加热混有二氧化锰的氯酸钾制备一瓶氧气用于性质实验。
①该方法制得O2的化学方程式是 。
②可选用 和 (填序号)装置组合。首先检查装置的气密性,方法是:把导管口放入水中,然后 ,观察到有气泡冒出,说明装置气密性良好
(2)氢气被认为是理想的清洁、高能燃料。
①实验室用锌与稀硫酸制取氢气并验证其可燃性,可选用 (填序号)与E装置组合,在E导管口点燃。实验过程是:组装仪器→检查装置气密性→装入药品制备氢气→ →点燃。
②电解水也可制得H2.装置如图F, 管中产生的是氢气
③氢气的生产方法是制约其作为清洁能源广泛使用的原因之一,科学家根据生产方法提出“绿色”氢气和“有污染”的氢气的概念,下列方法可获得“绿色”氢气的是 。
A.用矿石生产锌和硫酸,再相互反应
B.在催化剂作用下,利用太阳能光解水
C.利用煤燃烧发电,再电解水
D.利用风能、水力发电,再电解水
除去下列物质中所含杂质(括号内为杂质)的实验,能达到目的( )
A.NaOH(Na2CO3):加入适量稀盐酸
B.CO(CO2):通过装有浓硫酸的洗气瓶
C.CuO(C):在空气中充分灼烧
D.MgSO4(Na2SO4):溶解,过滤
下列实验方案,不能达到相应实验目的是( )
A. 比较空气与人体呼出的气体中CO2含量
比较空气与人体呼出的气体中CO2含量
B. 探究MnO2能否加快H2O2分解
探究MnO2能否加快H2O2分解
C. 验证燃烧需要温度达到着火点
验证燃烧需要温度达到着火点
D. 探究CO2对铜生锈是否有影响
探究CO2对铜生锈是否有影响
如图的实验设计不能实现其对应实验目的是( )
A. 测定空气中O2含量B.
测定空气中O2含量B. 检验氢气的纯度
检验氢气的纯度
C. 探究燃烧的条件D.
探究燃烧的条件D. 证明密度:CO2>空气
证明密度:CO2>空气
为了达到相应的实验目的,下列实验设计不合理的是( )
A. 分离H2O2和MnO2制O2后的固液混合物
分离H2O2和MnO2制O2后的固液混合物
B. 除去CO中的CO2气体
除去CO中的CO2气体
C. 区分NaCl、NH4NO3、NaOH三种固体
区分NaCl、NH4NO3、NaOH三种固体
D. 探究可燃物燃烧的条件
探究可燃物燃烧的条件
某化学实验小组需制备O2并进行O2部分性质实验,结合以下装置,回答下列问题:
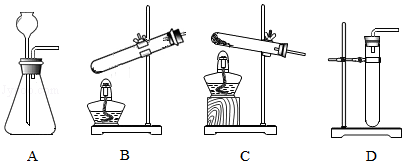
(1)甲同学利用KClO3和MnO2制备O2,其发生装置应选用上述装置中的 ( 选填装置对应的字母),收集O2的方法是 (只填一种),可用 检验O2;
(2)乙同学提出可用H2O2和MnO2制备O2,本着废物利用的原则,可以从甲同学制备O2后剩余的固体中提取MnO2,则提取MnO2的操作步骤依次为:①溶解、② 、③洗涤、④干燥,其中步骤②比①多使用了一种玻璃仪器,该仪器名称是 ,请写出乙同学制O2的化学方程式:
(3)丙同学欲用少量的KMnO4和较多量的KClO3固体混合物加热,以较快制备较多量O2,你认为是否可行? ,(填“可行”或“不可行”),请说明理由: ;
(4)丁同学将硫粉置于收集到的O2中燃烧,可观察到发出 火焰(填火焰颜色),其产物的名称是 ,它是形成酸雨的主要原因.
根据如图实验方案进行实验,能达到相应实验目的是( )
A. 比较Zn和Fe的金属活动性
比较Zn和Fe的金属活动性
B. 探究铁钉生锈时O2是否参与反应
探究铁钉生锈时O2是否参与反应
C. 比较红磷和白磷的着火点
比较红磷和白磷的着火点
D. 测定空气中O2的含量
测定空气中O2的含量
下列依据实验目的设计的实验方案中合理的是( )
| A. |
除去铁制品表面的铁锈,用过量的稀硫酸长时间浸泡 |
| B. |
验证甲烷中含有H 2,点燃,在火焰上方罩一只干冷烧杯,观察内壁是否出现液滴 |
| C. |
鉴别化肥KNO 3和NH 4Cl,取样与熟石灰混合研磨,闻气味 |
| D. |
检验NaOH是否变质,取样,加水溶解后滴加酚酞试液,观察溶液颜色是否变红 |
你认为下列实验方法不可行的是( )
| A. |
区分硬水和软水:分别加肥皂水观察现象 |
| B. |
检验稀烧碱溶液和纯碱水的酸碱性:分别加入酚酞溶液,观察颜色变化 |
| C. |
鉴别黄铜(铜锌合金)与黄金:分别在空气中灼烧,观察现象 |
| D. |
除去稀盐酸中混有的少量硫酸:加入适量的氯化钡溶液,充分反应后过滤 |
t℃时,加热烧杯中的石灰水,发现溶液变浑浊,测得此时溶液的pH>7.关于溶液变浑浊的原因,同学们有两种观点:①Ca(OH) 2的溶解度随温度升高而减小;②Ca(OH) 2与空气中的CO 2反应。他们设计以下方案进行探究,其中没有意义的是( )
| A. |
将装有浊液的烧杯,用冰水冷却,恢复至t℃,观察浑浊是否消失 |
| B. |
取适量浊液,过滤,往滤渣中加入盐酸,观察是否有气泡产生 |
| C. |
取适量浊液,过滤,往滤液中加入Na 2CO 3溶液,观察是否有沉淀生成 |
| D. |
其他条件不变,隔绝空气,再做一个加热石灰水的对比实验 |
下列实验操作不能达到实验目的是( )
| |
实验目的 |
实验操作 |
| A |
区别蚕丝与棉线 |
取样,灼烧,辨别气味 |
| B |
鉴别H 2SO 4溶液和NaOH溶液 |
取样,滴加酚酞溶液,观察现象 |
| C |
区别硬水和软水 |
取样,加肥皂水,振荡,观察现象 |
| D |
配制100g溶质质量分数为20%的盐酸 |
将20g浓盐酸加入80g水中,充分搅拌 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
氧烛是一种便携式供氧设备(如图)。产氧药块由氯酸钠(分解时吸收热量为QkJ•g ﹣ 1)、金属粉末(燃烧时提供氯酸钠分解所需的热量)和少量催化剂组成。某兴趣小组拟自制氧烛,为确定每100g氯酸钠需要添加金属粉末的质量[m(金属)],查得下表数据:
| 金属 |
铁 |
铝 |
镁 |
| 燃烧放出热量/(KJ•g ﹣ 1) |
4.73 |
31.02 |
24.74 |
下列说法正确的是( )

| A. |
m(金属)只能采用不同比例的金属和氯酸钠在空气中实验获得 |
| B. |
m(金属)只能通过氯酸钠分解吸收热量与金属燃烧放出热量进行理论计算确定 |
| C. |
m(金属)过小将使氧烛中反应无法持续进行,过大将减小产氧量 |
| D. |
不用催化剂时,分别使用铁、铝、镁作燃料,m(Fe)最小 |
下列实验方案能达到实验目的是( )
| 选项 |
实验目的 |
实验方案 |
| A |
证明某固体是碳酸盐 |
取样,滴加盐酸,观察是否有气泡 |
| B |
证明二氧化碳能与水反应 |
将二氧化碳通入滴有酚酞溶液的水中 |
| C |
检验氧气已收集满 |
将带火星的木条伸入集气瓶中 |
| D |
证明蜡烛中含有碳元素 |
将内壁蘸有澄清石灰水的烧杯罩在蜡烛火焰上方 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
试题篮
()