O2是人类生活不可缺少的物质,制取O2的方法很多。请回答下列问题:
(1)KMnO4分解法:该反应的化学方程式为 ;
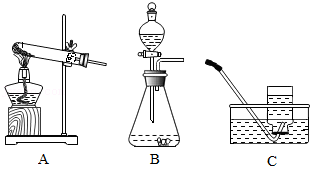
(2)KClO3分解法:应选用图中的 (填图中装置对应的字母)作发生装置;
(3)H2O2分解法:常温下H2O2分解缓慢,通常加入少量MnO2,则MnO2的作用为 ;
(4)可以用C所示装置来收集O2,体现了O2 的性质;
(5)已知N2的沸点为﹣196℃,O2的沸点为﹣183℃。工业上在低温下加压,先使空气液化,然后蒸发,则O2为 (填“先”或“后”)蒸发出来的气体。
请根据下列实验装置图回答问题。
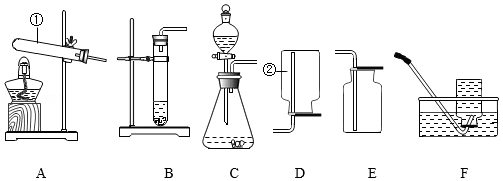
(1)写出标号仪器的名称:①是 ,②是 。能用装置E收集的气体应具有的性质是 。
(2)实验室用过氧化氢溶液和MnO2混合制O2时MnO2的作用是 。收集较纯净的氧气,装置可用 (填字母)。用锌与稀硫酸反应制取氢气的化学方程式为 。
(3)实验室可用铜片与浓硝酸在常温下反应制取少量二氧化氮(NO2)。通常状况下,二氧化氮是红棕色气体,溶于水时与水反应生成硝酸和一氧化氨(NO)。
①制取NO2的发生装置可用 (填字母)。
②收集NO2不用装置F的原因是 (用化学方程式表示)。
试题篮
()