A、B、C三种固体物质的溶解度曲线如图所示。请回答
(1)P点的含义是 。
(2)t1℃时,将10gA物质投入到50g水中充分溶解后,所得溶液的质量为 g
(3)t2℃时,取等质量的A、B、C三种物质分别配制成饱和溶液,需要水的质量最小的是 。
(4)t3℃时,将接近饱和的C溶液变为该温度下的饱和溶液,下列分析正确的是 (填字母序号)。
A.溶质的质量一定变大
B.溶剂的质量一定变小
C.溶质的质量分数一定变大

为除去粗盐中混有的泥沙,某学习小组按以下步骤进行实验:(实验环境温度为20℃)
Ⅰ.称量与溶解Ⅱ.过滤Ⅲ. 。
请回答下列问题:
(1)将步骤Ⅲ补充完整。
(2)如图中图1为氯化钠的溶解度曲线,图2为步骤Ⅰ中的部分操作:

①由图1给出的信息可知:20℃时,NaCl的溶解度是 g。
②从节约能源和提高产率的角度分析,图2中所需水的最佳体积是 mL.(提示:水的密度为1g•mL﹣1;产率 100%)
③用玻璃棒搅拌的目的是 。
(3)过滤时,若漏斗中的液面高于滤纸的边缘,造成的后果是 (填字母)。
a.过滤速度慢
b.滤纸破损
c.部分杂质未经过滤进入滤液
如图是甲、乙两种固体物质的溶解度曲线。
(1)甲的溶解度随着温度的升高而 。
(2)使接近饱和的甲溶液变为饱和溶液的一种方法是 。
(3)t℃时,甲的饱和溶液中溶质与溶液的质量比为 。
(4)乙中含有少量甲,提纯乙可采用的方法是 。

如图是甲、乙、丙三种物质的溶解度曲线。请根据图中信息回答下列问题:
(1)甲、乙两种物质在 ℃时溶解度相等;
(2)t3℃时,把30克甲充分溶解在50克水中,所得溶液质量是 g;
(3)t3℃时,甲、乙、丙三种物质的等质量饱和溶液中,所含溶剂质量最多的是 ;
(4)若甲中混有少量乙,要得到纯净的甲,常用的提纯方法是 。

A、B、C三种物质的溶解度曲线如图所示,请回答下列问题:
(1)t2℃时,A、B、C三种物质溶解度的大小关系是 (用“A、B、C”和“>、<、=”表示)
(2)要使接近饱和的C溶液在保持溶质质量分数不变的情况下变成饱和溶液的方法是 。
(3)将100g质量分数为30%的A溶液由t3℃降温至t1℃,降温后所得溶液中溶质的质量分数是 。
(4)t3℃时,A、B、C三种物质的混合溶液中,A、B、C三种溶质的质量相等,将混合溶液在该温度下恒温蒸发溶剂,首先析出的物质是 。

请根据如图甲、乙、丙三种固体物质的溶解度曲线,回答下列问题。
(1)在 ℃时,甲、丙两种物质的溶解度相等;
(2)在t2℃时,向盛有25g甲物质的烧杯中加入50g水,充分溶解后,所得溶液的溶质质量分数为 。
(3)若乙物质中混有少量甲物质,最好采用 (填“降温结晶”或“蒸发结晶”)的方法提纯乙;
(4)t2℃时,甲、乙、丙三种物质的饱和溶液各100g,所含溶剂的质量由大到小的顺序是 。

溶液在生活、生产中具有广泛的用途。
(1)在20℃时,将20g氯化钾固体加入50g水中,充分搅拌后,仍有3g氯化钾固体未溶解。所得溶液中氯化钾的质量分数为 (计算结果保留一位小数);20℃时氯化钾的溶解度为 。
(2)甲、乙两种不含结晶水的固体物质的溶解度曲线如图。t1℃时,甲溶液的溶质质量分数与乙溶液的溶质质量分数相比,前者与后者的关系是 (填字母)。
A.大于 B.小于 C.等于 D.无法确定
(3)如图是实验室稀释浓硫酸的正确和错误操作,请说明不能将水直接倒入浓硫酸中进行稀释的原因 。


作图法是常用的数据处理方法。如图是A、B、C三种物质的溶解度曲线图,请回答下列问题:
(1)P点的意义是 。
(2)t3℃时,A、B、C三种物质溶解度最大的是 。
(3)将某温度下C的不饱和溶液变成饱和溶液的方法是 (写一种)。
(4)在t3℃时,将A、B、C的饱和溶液分别降温到t1℃时,所得溶液溶质的质量分数由大到小的顺序是 。

人类的生活、生产离不开水与溶液。请用相关的知识回答下列问题。
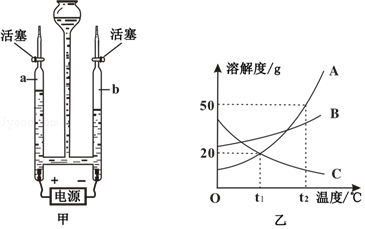
(1)电解水的实验如图甲所示,接通直流电源一段时间后,b玻璃管内产生的气体体积约为16mL时,a玻璃管内产生的气体体积约为 mL。
(2)自来水厂净化水的过程为:水库→取水→加絮凝剂→静置沉淀→过滤→活性炭吸附→清水池→投药消毒→配水泵→用户。其中能除去颜色和异味的操作是 。
(3)A、B、C三种固体物质的溶解度曲线如图乙所示,回答下列问题。
①t1℃时,溶解度等于20g的物质有 ;
②t2℃时,向盛有50g B物质的烧杯中加入100g水,充分溶解后,所得溶液的质量 (填“>”、“=”或“<”)150g;
③t2℃时,A、B、C三种物质饱和溶液的溶质质量分数由大到小的顺序是 。
甲、乙、丙三种物质的溶解度曲线如图所示,回答下列问题:
(1)t1℃时,甲、乙、丙三种物质溶解度由大到小的顺序是 。
(2)t3℃时,将20g物质丙加入50g水中充分溶解,并恢复到原温度,所得溶液的溶质质量分数为 。(结果保留到0.1%)
(3)在不改变溶质质量分数的前提下,将甲的不饱和溶液转化为饱和溶液的方法是 。
(4)下列说法不正确的是 (填字母序号)。
A.t1℃时,用甲、乙、丙三种固体配制等质量的饱和溶液,所需水的质量大小关系是乙>甲>丙
B.t2℃时,甲、丙两物质饱和溶液中所含溶质质量相等
C.将t3℃时的甲、丙的饱和溶液降低温度至t2℃,所得溶液的溶质质量分数相等
D.乙中混有少量甲,可以采用蒸发结晶的方法提纯乙

甲、乙、丙三种物质的溶解度曲线如图所示,请回答。
(1)P点的含义是 。
(2)气体的溶解度随温度变化的趋势与 (填“甲”、“乙”或“丙”)相似。
(3)t3℃时,将40g甲物质加到50g水中充分溶解后,所得溶液的质量为 g。
(4)若乙中含有少量甲,提纯乙的方法是 。
(5)将t3℃时等质量的甲、乙、丙三种物质的饱和溶液分别降温到t1℃,对所得溶液的分析正确的是 (填字母序号)。
A.溶解度:乙>甲>丙
B.溶剂质量:丙>乙>甲
C.溶液质量:乙>甲>丙
D.溶质质量分数:乙>甲>丙

(1)据报道,今年第一季度,南宁市成为全国省会城市的“水质冠军”。以下措施,你认为有利于爱护水资源的是 (填写字母编号)。
A.全民提高节约用水意识
B.应用新技术、新工艺减少污染物的产生
C.抑制水中所有动植物的生长
D.对污染的水体作处理使之符合排放标准
(2)生活中为了降低水的硬度并杀菌、消毒,常用的方法是 。
(3)A、B、C三种固体物质的溶解度曲线如图所示,请根据图中信息完成下列问题:
①溶解度随温度升高而降低的物质是 。
②t3℃时,A物质的溶解度是 。
③以下说法正确的是 。
A.将A的溶液由t2℃降温到t1℃,一定有晶体析出
B.在t3℃时,将等质量的A、B、C三种物质的饱和溶液降温到t1℃,所得溶液中溶剂质量最多的是A溶液
C.t1℃时将A、B、C三种物质各5g分别加入20g水中充分溶解,所得溶液质量的大小关系为C=B>A
D.将A、B、C三种物质的饱和溶液分别由t2℃升温到t3℃,所得溶液中溶质的质量分数最大的物质是B

甲、乙、丙三种物质(均不含结晶水)的溶解度曲线如图所示,回答下列问题:
(1)t1℃时P点的意义是 。
(2)t2℃时,比较甲、丙两物质的饱和溶液的溶质质量分数为:甲 丙(选填“>”、“=”或“<”)。
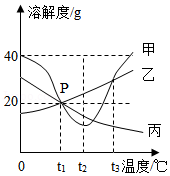
如图为甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线。
①20℃时,甲、乙、丙的溶解度由大到小的顺序是 。
②30℃时,50g水中加入10g固体丙,充分溶解后,所得溶液的质量为 g;
③60℃时,将等质量的甲、乙、丙三种固体分别溶于水中,都恰好配制成饱和溶液,所得甲、乙、丙的三种饱和溶液的质量由大到小的顺序为 。
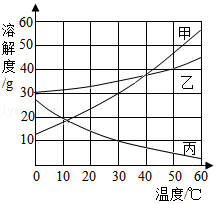
如图是三种常见固体物质的溶解度曲线。回答下列问题:

(1)KNO3的溶解度随温度升高的变化趋势是 (填“逐渐增大”或“逐渐减小”)。
(2)实验室配制溶液有如下步骤:(已知20℃时KCl的溶解度是34g)
①计算:20℃时,将67g的KCl饱和溶液稀释为20%,需加水18g。
②量取: 用量简量取水倒入烧杯中,提供的量筒规格有10mL、20mL、50mL,应该选择 mL的量筒。
③混匀:用 搅拌,使溶液混合均匀。
(3)根据以上溶解度曲线,判断下列说法正确的是 (多选)。
A.40℃时,KNO3的溶解度是64g,表示100g KNO3饱和溶液中含64g KNO3
B.Ca(OH)2的溶解度受温度变化的影响小于KCl的溶解度受温度变化的影响
C.KNO3混有少量KCl时,可用降温结晶法提纯
D.60℃时,将等质量的KNO3、KCl两种物质分别配制成饱和溶液,KNO3需要水的质量大于KCl
试题篮
()