下列操作既能加快硝酸钾的溶解速度,又能增加硝酸钾溶解质量的是
| A.搅拌 | B.振荡 | C.加热 | D.降温 |
甲、乙、丙三种物质的溶解度曲线如右图所示。下列叙述正确是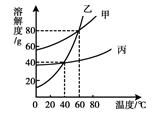
| A.40℃时,丙的溶解度最大 |
| B.由60℃降温至40℃时,甲析出的晶体最多 |
| C.40℃时,乙和丙的饱和溶液中溶质质量分数相同 |
| D.40℃时,100 g水中加入50 g 丙,所得溶液中溶质的质量分数为33.3% |
将60℃的硝酸钾饱和溶液降温至20℃,不发生变化的是
| A.溶液的质量 | B.溶质的质量 |
| C.溶剂的质量 | D.溶质的质量分数 |
右图是甲、乙两种固体物质的溶解度曲线。下列说法正确的是
| A.20℃时,甲、乙饱和溶液中溶质的质量分数不相等 |
| B.20℃时,将60g甲加入100g水中得到溶液A,若再加入100g水,会使溶液A的质量分数变小 |
| C.40℃时,甲的饱和溶液中溶质的质量分数约为33.3% |
| D.可采用降低温度的方法使乙的饱和溶液变为不饱和溶液 |
据《说文解字》记载,我们的祖先在神农氏时代就开始利用海水晒盐。海水晒盐的原理是( )
| A.日晒风吹使海水中的氯化钠蒸发 | B.日晒风吹使溶液由饱和变为不饱和 |
| C.日晒风吹使水分蒸发晶体析出 | D.日晒风吹使氯化钠的溶解度变小 |
下图表示A、B两种物质的溶解度(s)随温度(t)的变化情况,下列说法正确的是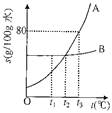
A.A的溶解度大于B的溶解度
B.升高温度可使A的不饱和溶液变为饱和
C.t3℃时,在100g水中溶解60gA能形成饱和溶液
D.t2℃时,A和B的饱和溶液的溶质质量分数相等
下列分析推理正确的是
| A.硝酸钾的溶解度受温度影响大,其溶液只要降温就能析出晶体 |
| B.硝酸铵溶于水时吸热,说明硝酸铵溶解时只发生吸热过程 |
| C.CO2可溶于水,所以其水溶液中的溶质是CO2 |
| D.酒精与水可任意比率互溶,所以不可能制得酒精的饱和溶液 |
下图是
、
、
固体的溶解度曲线,下列说法正确的是

| A. | 60℃三种物质的饱和溶液中,溶质质量分数最大的是 溶液 |
| B. | 将80℃不饱和的 溶液降温至40℃,一定能得到其饱和溶液 |
| C. | 40℃时 的溶解度比 小 |
| D. | 将80℃含有少量 的 饱和溶液降温至20℃,可得到 晶体 |
右图所示曲线a、b、c分别代表A、B、C三种物质的溶解度曲线。下列说法错误的是
A.t1 ℃时,三种物质溶解度大小的顺序是B>C>A
B.t2℃时,A和B两种物质的饱和溶液中溶质质量分数相同
C.t3℃时,在100g水里分别加入三种物质各mg,只有A能形成饱和溶液
D.从混有少量C的A物质中提取较纯净的A,最适宜采用冷却热饱和溶液结晶
下图是KNO3和NaCl的溶解度曲线。下列说法中正确的是
| A.NaCl的溶解度比KNO3的溶解度大 |
| B.t1℃时,100gKNO3饱和溶液中含有20gKNO3 |
| C.t2℃时,NaCl饱和溶液与KNO3饱和溶液中,溶质的质量分数不一定相等 |
| D.在温度高于t2℃时,KNO3的溶解度始终大于NaCl的溶解度 |
硝酸钾和氯化钾的溶解度曲线如图所示,下列叙述正确的是

| A. | 硝酸钾的溶解度一定大于氯化钾的溶解度 |
| B. | 降低温度可使接近饱和的硝酸钾溶液变饱和 |
| C. | ℃时,硝酸钾和氯化钾两种溶液的溶质质量分数一定相等 |
| D. | 60 ℃时100 水中加入90 硝酸钾,充分搅拌,可得到硝酸钾的饱和溶液 |
下图是两种物质的溶解度曲线。下列说法不正确的是 ( )
| A.60℃时,氯化铵、硫酸钠的溶解度相同 |
| B.4O℃时,50g水中最多能溶解25g硫酸钠 |
| C.将50℃时硫酸钠饱和溶液降温,一定有晶体析出 |
| D.将60℃时硫酸钠饱和溶液降温到40℃,溶质的质量分数保持不变 |
根据下图所示的溶解度曲线,判断下列说法中正确的是
| A.甲物质的溶解度小于乙物质的溶解度 |
| B.甲物质的溶解度受温度影响较小 |
| C.将t3℃时的甲、乙两物质的溶液降温到t2℃时都一定会析出晶体 |
| D.当甲物质中混有少量乙物质时,可采用冷却热饱和溶液的方法提纯甲 |
试题篮
()