(昌平25)分别将100g甲、乙的饱和溶液从t2oC降温到t1oC,对所得溶液的叙述正确的是
| A.甲、乙都是饱和溶液 |
| B.所含溶剂质量:甲<乙 |
| C.溶液质量:甲>乙 |
| D.甲、乙溶质质量均减小 |
打开汽水瓶盖会有大量气泡冒出,产生这一现象的原因是二氧化碳的溶解度随( )
| A.压强增大而减小 | B.压强减小而减小 |
| C.温度升高而升高 | D.温度降低而减小 |
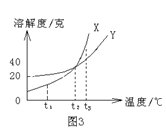
图3是X、Y两种固体物质的溶解度曲线。下列说法中正确的是
| A.t1℃时X的溶解度大于Y的溶解度 |
| B.t2℃时X的溶解度等于Y的溶解度 |
| C.t3℃时X的饱和溶液降温至t2℃时,变为不饱和溶液 |
| D.t1℃时Y的不饱和溶液升温至t2℃时,变为饱和溶液 |
t℃时,有两瓶硝酸钾溶液,一瓶为饱和溶液,一瓶为稀溶液,下列操作中,无法区分这两种溶液的是 ( )
| A.加入少量硝酸钾 | B.加入一定量的水 | C.略降低温度 | D.蒸发水分 |
生活中的下列现象,不能说明气体的溶解度随温度变化而变化的是
| A.打开汽水盖,有大量的气体冲出 |
| B.烧开水时,沸腾前水中有气泡产生 |
| C.夏季养鱼塘中,要经常开启增氧设备 |
| D.冰箱中制取的小冰块中常有小气泡 |
右图是某物质的溶解度曲线,60℃时,取100g水配制成该物质的饱和溶液,当温度降低至30℃时所得溶液的质量为
| A.130g | B.140g | C.160g | D.180g |
根据图示的溶解度曲线判断,下列说法正确的是 ( )
| A.甲物质的溶解度大于乙物质的溶解度 |
| B.甲物质的不饱和溶液温度升高后可以变成饱和溶液 |
| C.将t2℃甲、乙两物质的饱和溶液温度降低到t1℃时都会析出晶体 |
| D.t2℃时,甲、乙的饱和溶液中含有相同质量的溶质 |
如图为硝酸钾的溶解度曲线,下列说法中,正确的是
| A.硝酸钾的溶解度受温度影响不大 |
| B.100g水最多能溶解30g硝酸钾 |
| C.降温能使接近饱和的硝酸钾溶液变成饱和溶液 |
| D.20℃时硝酸钾的溶解度比40℃时硝酸钾的溶解度大 |
溶解度曲线为我们定量描述物质的溶解性强弱提供了便利。请你根据下图的溶解度曲线判断下列说法,其中正确的是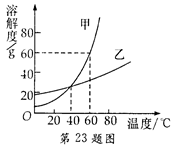
| A.20℃时,甲物质的溶解度大于乙物质的溶解度 |
| B.40℃时,两种物质的溶解度相等 |
| C.60℃时,将80 g甲物质放入100 g水中,所得溶液的质量为180 g |
| D.60℃时,将等质量的甲、乙两种物质的饱和溶液降温到20℃,析出晶体较多的是乙 |
根据图4信息判断,下列叙述不正确的是
| A.硝酸钾的溶解度随温度升高而增大 |
| B.t1 ℃时,氯化钠和硝酸钾的溶解度相同 |
| C.将t2℃时的硝酸钾饱和溶液降温到t1℃,有晶体析出 |
| D.t2 ℃时,80g硝酸钾溶于100g水中可制得饱和溶液 |
如图是甲、乙两种不含结晶水的固体物质的溶解度曲线,下列说法正确的是 ()

| A. | 甲、乙两物质的溶解度都随温度升高而增大 |
| B. | 时,甲、乙两物质的饱和溶液中溶质的质量分数相等 |
| C. | 时,甲的溶解度比乙的溶解度小 |
| D. | 时,甲、乙两物质各20 g可分别完全溶解在100 g水中 |
下表给出了在20℃和100℃时X、Y两种化合物在不同溶剂中的溶解度数据,请分析有关数据,判断利用结晶法从X、Y的混合物中提纯X时,使用哪种溶剂的回收率最高(已知混合物含X70g,含Y15g) ( )
| |
20℃时的溶解度/g |
100℃时的溶解度/g |
||
| 溶剂序号 |
X |
Y |
X |
Y |
| A |
20 |
5 |
90 |
30 |
| B |
15 |
1 |
70 |
10 |
| C |
5 |
15 |
75 |
25 |
| D |
10 |
12 |
80 |
20 |
在25℃时,向饱和的澄清石灰水中加入少量的氧化钙,恢复到25℃时,关于该溶液的下列说法中正确的是 ( )
| A.溶质质量不变 | B.溶质质量减少 |
| C.溶质的质量分数减小 | D.溶质的质量分数增大 |
试题篮
()