被誉为“中国天眼”的FAST,是目前世界上最大口径、最灵敏的射电望远镜,如图所示。请回答下列问题。
(1)选择角钢而不用纯铁作塔架的主要原因是 。
(2)角钢中含有锰(Mn)和硅,锰可以与稀盐酸发生置换反应,生成锰的化合物中锰元素显+2价。请写出锰与稀盐酸反应的化学方程式 。
(3)请你写出一条防止铁制材料生锈的具体措施 。
(4)向硝酸银和硝酸铜的混合溶液中加入一定量的铝粉,反应停止后过滤,得到滤渣和滤液。向滤渣中滴加稀盐酸,无气泡产生,则滤渣中一定含有 ;滤液中一定含有的溶质是 ,可能含有的溶质是 。(均填化学式)

小芳同学对部分化学知识总结整理如下,其中完全正确的一组是( )
A.生活中的化学 |
B.安全常识 |
①自行车链条可采用涂油的方法防锈 ②电木(酚醛塑料)插座破裂后能进行热修补 |
①氢氧化钠有强烈的腐蚀性,如果不慎沾到 皮肤上,要用大量水冲洗,再涂硼酸溶液 ②为防止一氧化碳中毒在室内放一盆水 |
C.化学规律 |
D.物质的鉴别 |
①溶液稀释前后,溶质的质量不变 ②化学反应前后元素的种类和质量都不变 |
①用熟石灰鉴别尿素和氯化钾 ②用灼烧闻气味的方法鉴别棉花和羊毛 |
A.AB.BC.CD.D
近年来,共享单车在国内一些城市走红.

(1)图1共享单车上标出的部件由有机合成材料制成的是 (填序号);
(2)保护共享单车的措施之一是防止其锈蚀,其中链条常采用的防锈方法是 ,防锈的原理是 .
(3)共享单车中有些部件是由钢铁制成的,图2是工业炼铁的反应原理模拟实验,玻璃管中发生反应的化学方程式是 ;从环保角度看,该装置的不足之处是 .
盐酸可以除铁锈。
(1)将一根生锈的铁钉放入足量的稀盐酸中,观察到铁锈逐渐消失,溶液由无色变成 ,该反应的化学方程式为 ,其基本反应类型为 。一段时间后,又观察到铁钉表面有气泡产生,该反应的化学方程式为 。
(2)写出一种防止铁制品锈蚀的方法 。
你认为下列做法正确的是( )
| A. |
为灭掉室内大火,迅速打开门窗降温 |
| B. |
为节约用水,工业废水直接用于农田灌溉 |
| C. |
为除去铝壶中的水垢,用盐酸长时间浸泡 |
| D. |
为防止铁锅生锈,在其表面涂抹一层食用油 |
现在很多家庭自备干粉灭火器,其中一种灭火器是利用压缩的二氧化碳吹干粉(干粉的主要成分是磷酸二氢铵)灭火.
(1)灭火器中的二氧化碳可利用空气中含量最多的气体来代替,该气体是 .
(2)磷酸二氢铵(NH4H2PO4)受热分解时吸收大量的热,并能在可燃物表面形成一层玻璃状的覆盖层.其灭火原理是 .
(3)报废灭火器中的NH4H2PO4可做化肥,但不能作为 (填字母序号)使用.
A、氮肥 B、磷肥 C、钾肥 D、复合肥
(4)铁质的灭火器罐体容易生锈.请你写出一种防止铁生锈的方法 .工业上常用稀盐酸除铁锈(Fe2O3),该反应的化学方程式是 .
人们常说的“五金”是指:金、银、铜、铁、锡。根据所学知识回答:
(1)“真金不怕火炼”是指金即使在高温下也不与 反应;
(2)黄铜片(铜锌合金)和铜片相互刻画,在铜片上留下刻痕,说明黄铜片的硬度比铜片的硬度 (填“大”或“小”);
(3)铁制容器不能用来盛放农药波尔多液(主要成分是硫酸铜和氢氧化钙),用化学方程式表示其原因 ;
(4)防止金属腐蚀是保护金属资源的有效途径之一,写出一种防止铁制品生锈的具体方法 。
人们常说的“五金”是指:金、银、铜、铁、锡。根据所学知识回答:
(1)“真金不怕火炼”是指金即使在高温下也不与 反应;
(2)黄铜片(铜锌合金)和铜片相互刻画,在铜片上留下刻痕,说明黄铜片的硬度比铜片的硬度 (填“大”或“小”);
(3)铁制容器不能用来盛放农药波尔多液(主要成分是硫酸铜和氢氧化钙),用化学方程式表示其原因 ;
(4)防止金属腐蚀是保护金属资源的有效途径之一,写出一种防止铁制品生锈的具体方法 。
下列说法中,不正确的是( )
A.溶液中有晶体析出时,溶质质量减小,则溶质质量分数一定减小
B.将钢铁制成合金是有效减缓钢铁制品锈蚀的方法之一
C.碱溶液中都含有氢氧根离子,因此碱具有相似的化学性质
D.自然界中二氧化碳的循环平衡,对地球生命具有重要意义
金属材料在生产、生活中有广泛的应用,认识金属的性质有利于更好地利用金属。
(1)铁在初中化学实验中多次亮相,如图展示了铁钉的一系列变化。

I.变化①是铁钉与空气中的 发生了反应。
II.变化②中常见除去铁锈的化学方程式为 。
III.如表是小明同学记录的锌粉与稀硫酸反应过程中反应时间与产生气体体积的变化数据:
时间(min) |
1 |
2 |
3 |
4 |
5 |
氢气体积(mL) |
50 |
120 |
230 |
290 |
310 |
实验数据反映,该反应速率的特点是 ,引起该速率变化的原因是 。
(2)将m克锌和铁的混合物放入硝酸铜溶液中,充分反应,经过滤、洗涤、干燥后,固体仍为m克,则反应后滤液中一定含有的溶质是 (填化学式)。
金属材料在生产、生活中有广泛的应用,认识金属的性质有利于更好地利用金属。
(1)铁在初中化学实验中多次亮相,如图展示了铁钉的一系列变化。

I.变化①是铁钉与空气中的 发生了反应。
II.变化②中常见除去铁锈的化学方程式为 。
III.如表是小明同学记录的锌粉与稀硫酸反应过程中反应时间与产生气体体积的变化数据:
时间(min) |
1 |
2 |
3 |
4 |
5 |
氢气体积(mL) |
50 |
120 |
230 |
290 |
310 |
实验数据反映,该反应速率的特点是 ,引起该速率变化的原因是 。
(2)将m克锌和铁的混合物放入硝酸铜溶液中,充分反应,经过滤、洗涤、干燥后,固体仍为m克,则反应后滤液中一定含有的溶质是 (填化学式)。
下列防锈措施不合理的是( )
A.钢管存放在干燥的地方
B.用盐水清洗菜刀
C.及时清除铁制品表面的锈渍
D.在铁管表面镀上一层不易锈蚀的金属
金属材料在人类的生产、生活中有着十分重要的作用。
(1)多种金属可以压成薄片,抽成细丝,说明金属具有 性。
(2)实验室有打磨过的铝片、铁片和硫酸铜溶液。兴趣小组同学欲验证铝、铁和铜的活泼性顺序,进行如下操作:
①取少量硫酸铜溶液于试管A中,将铁片(足量)插入硫酸铜溶液中,充分反应后将铁片取出,观察到的实验现象是 。
② (请补充实验具体操作)。
③取少量硫酸铜溶液于试管B中,将铝片插入硫酸铜溶液中,充分反应,写出该反应的化学方程式 。
结论:三种金属的活泼性由强到弱顺序是 。
(3)金属腐蚀造成的损失巨大,对金属腐蚀的控制尤为重要。下列对金属的防护措施不合理的是 (填序号)。
a、齿轮表面涂油 b、将钢材深埋保存
c、将钢刀浸泡在盐水中 d、车圈镀铬。
2017年4月,“航母”下水,开拓中国新蓝海。
(1)“航母”舰体材料为合金钢,国产航母使用的“超级钢”具有极佳的抗压性、延展性和焊接性。合金钢是 (填序号)
a.合成材料 b.复合材料 c.无机材料
(2)“航母”升降机可由铝合金制造,用石墨作电极在高温条件下电解熔融氧化铝,在阴极和阳极区分别得到A1和O2,阳极区使用的石墨易消耗的原因是 。
(3)“航母”螺旋浆可由铜合金制造。铜合金比铜的硬度 (填“大”或“小”),铜比铁在海水中耐腐蚀的原因是 。
(4)由生铁炼钢时,硅(Si)与氧化亚铁在高温条件下反应生成二氧化硅和铁,该反应的化学方程式为 。

铁及其化合物在生产生活中有广泛的应用。
(一)铁的应用和防护
(1)某麦片中含微量铁粉,食用后铁粉与胃酸反应转化为人体可吸收的铁元素,反应的化学方程式为 。
(2)铁锈主要成分是Fe 2O 3•nH 2O,铁生锈主要与空气中的 有关。
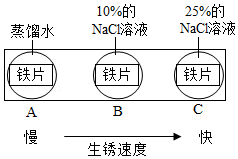
(3)如图实验说明NaCl在铁生锈中的作用是 。
(4)铁生锈的次要过程:Fe 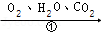 FeCO 3•nH 2O
FeCO 3•nH 2O  FeCO 3
FeCO 3
写出Fe转化为总反应的化学方程式 。
(5)为防止铁生锈,可对铁制品进行"发蓝"处理,使其表面生成致密氧化物(其中Fe、O元素质量比为21:8)保护膜,该氧化物的化学式为 。
(二)废铁的再利用
黄钠铁矾[NaFe x(SO 4) y(OH) z]是一种高效净水剂。用废铁屑(主要成分为Fe,含少量Fe 2O 3和FeCO 3)制备黄钠铁矾的主要流程如图:
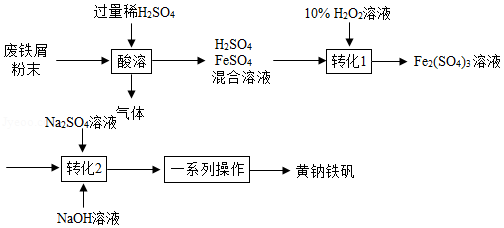
(1)将废铁屑研磨成粉末的目的是 。
(2)"酸溶"时H 2SO 4与Fe、FeCO 3反应,还发生反应的化学方程式有 和Fe+Fe 2(SO 4) 3=3FeSO 4。
(3)"转化1"发生反应的化学方程式为 。反应时温度不宜过高的原因是 。
(三)黄钠铁矾组成确定
称取9.70g黄钠铁矾,用如图装置进行热分解实验。
【资料】
①NaFe x(SO 4) y(OH) z在T 1℃分解会生成H 2O(气态),提高温度至T 2℃继续分解产生SO 3气体,并得到Fe 2O 3和Na 2SO 4。
②浓硫酸可用于吸收SO 3。
(1)装配好实验装置后,先要 。
(2)分别控制温度在T 1℃、T 2℃对A中固体加热。
①控制温度在T 1℃加热,实验后测得B装置质量增加1.08g。
②用D装置替换B装置,控制温度在T 2℃,加热至反应完全。
③T 1℃、T 2℃时,加热后均通入一段时间N 2,目的是 。
(3)反应完全后,将A装置中固体溶于足量水,过滤、洗涤、烘干得4.80g固体,将滤液蒸干得1.42g固体(不含结晶水)。
结论:NaFe x(SO 4) y(OH) z中,x:y:z= 。
反思:若该实验过程中缺少C装置,则x:z的值 (选填"偏大""偏小"或"不变")。
试题篮
()