人类文明进步与金属材料发展关系十分密切。
(1)下列金属制品的主要用途,利用金属导电性的是 。
(2)2018年10月24日,港珠澳大桥正式通车运营。港珠澳大桥是世界最长的跨海钢桥,施工中用了大量的钢材并采用了先进的防锈技术,钢铁制品在空气中容易与 等物质接触而生锈,请写出一种生活中防止钢铁制品生锈的方法 。
(3)铝制品在空气中具有优良的抗腐蚀性能,原因是 (用化学方程式表示)。
(4)将一定量的金属R加入硝酸锌和硝酸银的混合溶液中,充分反应后过滤,得到滤液和滤渣。下列说法正确的是 。
A.若滤液有颜色,则R一定是Cu
B.若滤渣中加入稀盐酸产生气泡,则滤渣中一定有Zn
C.若滤渣中只有2种金属,则滤液中一定有2种溶质
D.若向滤液中加入稀盐酸,无明显现象,则滤渣中一定有Ag,可能有R

金属在生产生活中有广泛应用
(1)“共享单车”作为代步工具,既轻便灵活,又环保。如图是一款自行车的图片,所标材料中,车架主要含有的金属元素是 ,为防止车架生锈,可以采取的防锈措施是 ,铝合金与纯铝相比,其硬度更 (填“大”或“小”)
(2)赤铁矿(主要成分Fe2O3)是炼铁的一种矿石,Fe2O3属于 (填“单质”或“氧化物”)。我国是使用“水法冶铜”最早的国家,请写出铁和硫酸铜溶液反应的化学方程式
(3)为了验证Fe、Cu、Ag三种金属的活动性顺序,下列选用的药品可行的是 (填序号)
①Fe、CuSO4溶液、Ag
②FeSO4溶液、Cu、Ag
③FeSO4溶液、Cu,AgNO3溶液
④FeSO4溶液,CuSO4溶液、Ag
(4)由两种元素组成的某合金6g与足量的稀硫酸充分反应后,生成0.2g氢气。下列说法不合理的是 (填字母代号)
A.合金中的元素可能是Fe和Cu
B.所得溶液中的溶质可能是硫酸镁和硫酸
C.合金中的元素可能是Zn和Fe
D.所得溶液中的溶质可能是硫酸铝和硫酸
E.合金中的元素可能是Zn和Ag
F.所得溶液中的溶质可能是硫酸镁、硫酸铝和硫酸

金属和金属材料在生产生活中有广泛的用途。请回答下列问题:
(1)我国自主研制的C919大型客机试飞成功,标志着我国飞机制造技术又有了新的突破。飞机外壳的主要材料是铝合金,“铝合金”属于 (填“金属材料”或“合成材料”)。
(2)工业上,常用一氧化碳在高温条件下还原赤铁矿(主要成分是Fe2O3)的方法炼铁,该反应的化学方程式为 。铁制品生锈是由于铁制品同时与空气中的氧气和 接触而锈蚀。
(3)向一定量的AgNO3溶液中加入一定量的锌粉和铜粉,充分反应后过滤,得到滤渣和溶液。对滤渣和滤液分析正确的有 (填序号)。
①若滤液呈蓝色,则滤渣中一定含有Ag,一定不含有Cu
②若滤液中只含有一种溶质,则滤渣中一定含有Ag、Cu,可能含有Zn
③若滤渣中只含有一种金属,则溶液中一定含有Zn(NO3)2、Cu(NO3)2一定不含有AgNO3
④若向滤渣中加入稀盐酸无气体产生,则滤液中一定含有Zn(NO3)2,可能含有Ag NO3、Cu(NO3)2
“科教扶贫”是实施精准扶贫的有效途径之一,请结合相关知识回答下列问题。
(1)提倡绿色发展,开发利用新能源,减少使用煤、石油、 三大化石燃料。中国地质调查局2017年5月18日宣布,我国成功完成可燃冰的实验开采工作,可燃冰的气体成分主要是甲烷,要使其在空气中燃烧,还需具备的条件是 。其燃烧的化学反应方程式为 。
(2)倡导科学膳食,注重营养均衡,人类必须摄取的六大基本营养素是糖类、 、油脂、维生素、无机盐和水。其中富含维生素的食物有 (任写一种)。
(3)注重科学选材,完善基础设施。铁是被广泛使用的一种金属材料,其缺点是易与水和 反应而锈蚀,铁锈可用稀盐酸除去,其反应的化学方程式为 。
化学与生活密切相关。请用所学知识填空。
(1)铁制品锈蚀的过程,实际上是铁跟空气中的 和水蒸气等发生化学反应的过程。为防止铁制栏杆生锈,通常采取的措施是 (任写一条)。
(2)人体缺乏某种微量元素将导致甲状腺肿大,该微量元素是 (填字母)。
A.碘 B.铁 C.锌
(3)长期饮用硬水对健康不利,生活中常用的软化水的方法是 。
(4)固体MgH2是氢能源汽车的供能剂,MgH2可以和水反应生成氢氧化镁,同时释放出氢气,该反应的化学方程式是 。
下列防锈措施不合理的是( )
A.钢管存放在干燥的地方
B.用盐水清洗菜刀
C.及时清除铁制品表面的锈渍
D.在铁管表面镀上一层不易锈蚀的金属
金属材料在生产、生活中有广泛的应用,认识金属的性质有利于更好地利用金属。
(1)铁在初中化学实验中多次亮相,如图展示了铁钉的一系列变化。

I.变化①是铁钉与空气中的 发生了反应。
II.变化②中常见除去铁锈的化学方程式为 。
III.如表是小明同学记录的锌粉与稀硫酸反应过程中反应时间与产生气体体积的变化数据:
时间(min) |
1 |
2 |
3 |
4 |
5 |
氢气体积(mL) |
50 |
120 |
230 |
290 |
310 |
实验数据反映,该反应速率的特点是 ,引起该速率变化的原因是 。
(2)将m克锌和铁的混合物放入硝酸铜溶液中,充分反应,经过滤、洗涤、干燥后,固体仍为m克,则反应后滤液中一定含有的溶质是 (填化学式)。
生活处处有化学。从化学的角度看,下列做法不合理的是( )
A.进入久未开启的枯井或地窖,先做灯火实验
B.铁制品生锈后不要轻易去除,以减缓铁的锈蚀
C.误服硫酸铜等含重金属离子的盐后,立即服用豆浆、牛奶或鸡蛋清缓解造成的中毒,并及时送医
D.室外发生火灾时,用湿毛巾捂住口鼻,逆风及时逃离现场
归纳是学习化学的基本方法。下面是小明整理的部分化学知识,其中都正确的选项是( )
A.安全知识 |
B.生活常识 |
①给试管里的液体加热时﹣﹣试管口不要对着人 ②浓硫酸沾到皮肤上﹣﹣用水冲洗后涂上硼酸溶液 |
①铁锅表面保持清洁干燥防止生锈 ②用铅笔芯粉末使铁锁开启灵活 |
C.除去杂质 |
D.元素与人体健康 |
①用稀盐酸除去铜粉中的少量氧化铜粉末 ②滴加氯化钙溶液除去烧碱溶液中的少量碳酸钠 |
①缺氟﹣﹣会引起氟斑牙和氟骨病 ②吃水果、蔬菜﹣﹣可以补充维生素 |
A.AB.BC.CD.D
在野炊活动中,同学们携带了铁桶、牛肉、面条、蔬菜、食用油、食盐、味精、食醋、去污粉(有效成分为碳酸钠)等用品.
(1) 携带过程中,小滨不慎将食盐、去污粉的瓶子混淆了,若将它们重新区分,应选用 (填所携带物品的名称).
(2)小崔生火后在“灶”上悬挂铁锅时,小心调节铁锅到合适的高度,这样做的原因可能是 (填字母序号):
A.使用焰心加热 B.使用内焰加热 C.使用外焰加热
(3)烹饪牛肉汤时,为了解汤的咸味.小秀同学取锅中少量汤品尝,取少量汤进行品尝就可知道整锅汤咸味如何,是因为溶液具有 (填一条性质).
(4)野炊结束时,小俊用干布抹去铁锅表面的水渍,这样的目的是 .
某化学兴趣小组对金属的性质做了如下探究,请你帮他们完成下面的内容。
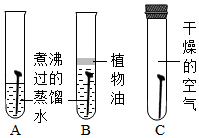
(1)探究铁生锈的原因(如图)(每支试管中均放有完全相同的洁净铁钉):
①一段时间后甲同学观察到: 试管中的铁钉明显生锈了。由此得出铁生锈的原因是铁与 共同作用的结果。
②为防止金属锈蚀,可以采取的措施有 (填一种)。
③在焊接铁制品前,常用稀盐酸清除其表面的锈,该反应的化学方程式是 。
(2)某同学分别向盛有形状、大小相同的铁片和锌片的试管中,倒入等质量、溶质质量分数相同的稀硫酸,以“ ”为依据来判断两种金属的活动性强弱。
(3)将一定质量的铁粉放入硫酸铜、硫酸锌的混合溶液中,充分反应后过滤,所得固体中一定含有的物质是 ,所得滤液中一定含有的溶质是 (填化学式)。
小明去年暑假随父母到南方旅游.江南水乡,烟雨蒙蒙,别有一番风景.
(1)小明发现,南方的公交车铁质部件的锈蚀情况明显比银川的严重.他感到奇怪,但很快就明白了,原因是江南地区的 ,铁更易锈蚀.钢铁材料锈蚀会造成很大损失,写出一个在常温下除铁锈的化学方程式 .
(2)金属家族有众多“兄弟”.把形状、大小相同的铁、铜、铝三种洁净的金属,分别放入溶质质量分数相同的稀盐酸中,反应最为剧烈的金属是 ,不反应的是 ,这反映出不同金属的活动性差异很大.
(3)若要验证金属锌的活动性强弱在铝和铁之间,可选用 溶液,分别将铝和铁放入其中观察.写出其中能反应的化学方程式 .
回答下列与金属有关的问题。
(1)黄铜和纯铜相比,硬度较大的是 ;
(2)铁生锈是铁与O2、 共同作用的结果;
(3)向CuSO4和Na2SO4的混合溶液中加入一定量锌粉,反应停止后过滤,所得滤液中一定含有的溶质是 。
回答下列与金属有关的问题:
(1)写出一种防止铁制品锈蚀的方法 ;
(2)将打磨后的Al丝插入CuSO4溶液中,发生反应的现象为① 、② .
试题篮
()