圆明园十二生肖兽首中的兔首和鼠首均为青铜器(铜、锡合金),某些铜器表面呈绿色,这是铜器长期暴露在空气中生了铜锈(俗称铜绿),为了弄清铜绿的组成和铜生成铜绿的条件,某化学兴趣小组进行了如下探究:
【查阅资料】铜绿的化学式是Cu2(OH)2CO3,它受热会分解生成三种氧化物。
铜绿分解的化学方程式为______ ____。
【猜想与假设】依据铜绿的组成和查阅的资料判断,铜绿可能是铜与氧气及__________共同作用而形成的。
【设计与实验】借鉴课本“铁钉锈蚀条件的探究”实验,小梁设计了“铜片锈蚀条件的探究”实验,实验如下图所示(所用铜片洁净、光亮): 实验较长时间后,发现_______试管中铜片最先生锈(填试管字母编号)。
【评价与改进】小风认为小梁设计的实验还不够完善,要得出正确的结论,还要补充一个实验。你认为要补充的一个实验是(用图表示在下方框内)。
【拓展与应用】小明发现从不同地点收集到的两个铜器(一个材质是纯铜,一个材质是青铜)中,纯铜器的铜绿比青铜器的少,他据此分析认为青铜比纯铜易锈蚀。小明的分析是否全面?请你说明理由:____ 。
铁矿石冶炼成铁是一个复杂的过程,把铁矿石和焦炭、石灰石一起加入高炉,在高温下,利用焦炭与氧气反应生成的一氧化碳把铁从铁矿石里还原出来。一氧化碳还原氧化铁的化学方程式为 。某兴趣小组在学习炼铁的相关内容时,对炼铁时还原剂的选择进行了如下探究。
【提出问题】单质碳也具有还原性,为什么工业上不用焦炭作为还原剂直接还原铁矿石?焦炭还原四氧化三铁的化学方程式为 。
【猜想与假设】焦炭和铁矿石都是固体,接触面积小,反应不易完全。
【查阅资料】氢氧化钠溶液和澄清石灰水化学性质类似,能与二氧化碳反应,但反应无明显现象。
【进行实验】实验步骤及注意事项如下:
①称取两份相同质量的氧化铁粉末。一份与足量的碳粉均匀混合放入下图装置A的试管中;另一份放入下图装置B的玻璃管中。
②装置A和B两组实验同时开始进行。在装置B的反应中,实验开始前应先 (选填“通CO”或“加热”);实验结束后应继续通入CO直至冷却至室温,其原因是 。
【实验现象】当装置B的玻璃管中固体完全由 时(选填“红色变为黑色”或“黑色变为红色”),装置A的试管中仍有红色固体。
【解释与结论】焦炭和铁矿石都是固体,接触面积小,反应确实不易完全,这可能是工业上不用焦炭作为还原剂直接还原铁矿石的一个原因。
【交流与反思】经过查阅资料和讨论,该小组同学发现除了上述原因外,工业上不用焦炭作为还原剂直接还原铁矿石还有一些其它原因,试写出其中的一个原因: 。
【完善实验】联想到单质碳的一些化学性质,甲同学认为在碳还原氧化铁的反应中可能还会有CO产生。为了证明碳还原氧化铁所得的气体中含有CO和CO2,将该气体通过下图的检验装置,
正确的连接顺序是:C → → → → C (选填字母,装置可重复使用)。
经过检验,证实碳还原氧化铁所得的气体中确实含有CO和CO2,因此装置A的不足之处是 。
某校化学研究性学习小组通过实验研究高炉炼铁的化学原理,设计了如下实验装置:
(1)已知HCOOH(甲酸) CO↑+H2O,根据该反应制取CO,A处应选用的气体发生装置是 (填小写字母序号);
CO↑+H2O,根据该反应制取CO,A处应选用的气体发生装置是 (填小写字母序号);
(2)装置中仪器①的名称是 ;装置B内所盛放浓硫酸作用是干燥CO,D装置的作用为 (用化学方程式表示)。
(3)①实验开始时应先点燃 (填“A”或“C”)的热源;②反应前后C装置玻璃管内物质颜色变化是 ;③C装置玻璃管内发生反应的化学方程式为 ;④检验C中的产物是否为铁的方法是 ;⑤待C装置玻璃管内物质冷却后再停止通CO的目的是 。
(4)该装置有一个明显的缺陷,改进的方法为 。
(5)用高炉炼铁得到含杂质的铁10g(杂质不溶于水,也不参加反应)与100g稀硫酸恰好完全反应,滤去杂质,得到滤液质量为108.1g,则含杂质的铁中铁的质量分数为 。
(6分)某同学设计下图所示的实验装置,进行一氧化碳还原氧化铁的实验。试回答:
(1)该装置存在的一个主要问题是 ,你的改进方法是 。
(2)实验过程中图A处玻璃管中能观察到的实验现象是 ,发生反应的化学方程式为 。
(3)B处观察到的实验现象是 。该同学实验完成后,发现过量的澄清石灰水增重0.44g,则通入装置的 气体质量 (填“>”、“<”或“=”)0.28g。
气体质量 (填“>”、“<”或“=”)0.28g。
(5分)请写出下列有关反应的化学方程式,并标明反应基本类型。
(1)铝条在氧气中燃烧 ( )反应;
(2)镁条溶于稀盐酸中 ( )反应;
(3)工业用磁铁矿炼铁 。
钢铁工业是国家工业的基础。
(1)工业上若采用的铁矿石的主要成分为氧化铁,则炼铁的主要反应原理为 (用化学方程式表示),其所用的设备为 ,生铁出口低于炉渣出口的原因是 。
(2)某兴趣小组在实验室中模拟炼铁化学原理的实验,对固体产物成分等进行探究。
【设计实验】用一氧化碳还原纯净的氧化铁粉末,实验装置如图。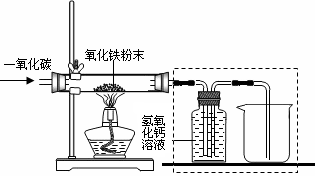
【进行实验】该小组按上述实验设计进行实验,实验时应先 (填“通入一氧化碳”或“点燃酒精灯”),目的是: 。
测得下列数据:
①反应前玻璃管和内盛氧化铁粉末的总质量66.0g(玻璃管的质量60.0g);
②反应后玻璃管和内盛黑色固体的总质量65.8g(冷却到室温称量)。
【分析与讨论】 本实验中,玻璃管内固体粉末由红色全部变为黑色。小明同学认为该黑色固体全部是铁,但小华同学提出了质疑,于是大家提出查阅资料。
【查阅资料】
①一氧化碳还原氧化铁的固体产物的成分与反应温度、反应时间等因素有关。
②一氧化碳还原氧化铁的实验过程中固体产物可能有四氧化三铁、氧化亚铁、铁。
③
| 物质 |
四氧化三铁 |
氧化亚铁 |
氧化铁 |
铁粉 |
| 颜色 |
黑色 |
黑色 |
红色 |
黑色 |
| 能否被磁铁吸引 |
能 |
不能 |
不能 |
能 |
【实验与猜想】
①该小组同学将反应后的黑色固体研磨后,再用磁铁吸引,发现黑色固体粉末全部能被吸引,则该黑色固体粉末中不可能含有 和 。
②进行猜想:黑色固体粉末可能 a.全部为铁 b. c.
【得出结论】 通过实验中获得的数据进行计算,得出黑色固体粉末为 。
【反思与评价】
①一氧化碳还原氧化铁的实验中,若要得到铁可适当提高温度和 。
②实验装置图中采用虚线框内的装置,其作用有 和 等。
金属和金属材料在人类的生产、生活中有着重要的作用。
(1)冬天取暖用的暖气片有铸铁材料、铜铝材料等多种。这主要利用了金属的性。
(2)铁生锈的条件是,因此,铸铁暖气片通常在表面刷漆以防铁被腐蚀。
(3)生产、生活中对钢铁的需求量特别大,在炼铁炉中, 还原氧化铁的化学方程式为。
还原氧化铁的化学方程式为。
(4)新型材料纳米铁粉具有广泛的用途,它比普通铁粉更易与氧气反应,其制备的主要流程如下图所示。
纳米级铁粉遇氧气无需加热就能燃烧,生成物的化学式为。
高温反应器中发生反应的化学方程式为。反应前需向反应器中通入氮气,目的是。
(7分)金属材料在生活中起着重要的作用.
(1)钢铁是常用的金属材料,铁易与空气中的水和 反应而生锈.
(2)铝制品具有更好的抗腐蚀性能,是因为铝表面能生成一层 ,阻止铝进一步被氧化.
(3)金属饰品常含钯、银、铂,某兴趣小组的同学在老师的帮助下进行了相关探究.
【提出问题】依据生活经验,同学们猜测钯的活动性可能与银和铂相近
【查阅资料】钯(Pd)呈银白色,有金属光泽,可用作饰品
【实验药品】钯、铂(Pt)、稀盐酸、硝酸银溶液和氯化钯(PdCl2)溶液
【实验探究】利用上述药品探究钯的金属活动性
| 实验步骤 |
实验现象 |
实验结论 |
| 把钯浸入硝酸银溶液中 |
无明显现象 |
钯的活动性比银________ |
| 把铂浸入氯化钯溶液中 |
___________ |
钯的活动性比铂强 |
得出结论:钯、银、铂的金属活动性由强到弱的顺序为 .
【废液处理】实验结束后同学们把所有液体倒入废液缸,出现白色沉淀.写出产生该现象的化学方程式:_______________.此反应属于 反应(填基本反应类型) .
(6分)下图甲是实验室模拟炼铁的装置图,试回答:
(1)按上图连接实验装置、检查装置的气密性、装药品、固定实验装置后,主要实验步骤有:
①通入一氧化碳;②停止通入一氧化碳;③点燃酒精灯;④熄灭酒精灯;⑤点燃酒精喷灯;⑥熄灭酒精喷灯.正确的操作顺序是____________________________(填序号).
(2)实验过程中仪器①中发生的反应的化学方程式为______________________________,现象是_____________________________________.
(3)实验过程中产生的尾气不能直接排放的原因是 .
(4)图乙是下业生产中炼铁高炉的结构图.实际生产中炼铁的原料铁矿石、焦炭、石灰石是从原料入口加入的,其中焦炭在高炉炼铁时的作用之一是产生高温,另一作用为____________;生铁出口低于炉渣出口的原因是_____________.
某同学用相同的铁钉探究铁生锈与哪些因素有关,设计的实验如图。经过一周观察:试管A和C中的铁钉无明显变化,试管B中的铁钉明显锈蚀。
(1)通过探究发现:铁生锈是铁与 和 共同存在时发生化学反应的过程。
(2)A中加入的蒸馏水要事先煮沸,其目的是 ;
(3)通过探究,请你写出防止铁制品生锈的一种措施 。
下图是课堂中模拟炼铁的实验装置。
(1)写出图中标有序号的仪器名称:① ,② 。
(2)实验过程中,先要进行的是 (填“I”或“II”)
I.加热 II.通一氧化碳
(3)酒精灯上加金属网罩的作用是 。
(4)A中反应的化学方程式是
A中观察到的现象是
B中反应的化学方程式是
B中观察到的现象是
(5)该装置的不足之处是
铁是应用最广泛的金属。
(1)为了检验铁生锈的条件,进行了如上图(略去其中的夹持装置)所示三个对比实验。一段时间后,甲中铁丝发生锈蚀且试管中液面上升,乙和丙中均无明显变化。由此得出铁丝锈蚀的过程,实际上是铁丝与 、 发生化学反应的过程;
(2)铁制品在下列情况:①潮湿空气中②部分浸入食盐水中③干燥的空气中,最易生锈的是 (填序号,下同),不易生锈的是 ;
(3)在“南海一号”打捞出来的文物中,铁器锈迹斑斑,残存很少,请你列举出一种日常生活中常用的防止铁生锈的方法 。
铁是生产、生活中应用广泛的金属材料。
(1)酸菜等酸性的食物不宜用铁质器具长期盛放,因为______________。
(2)为减缓海水对铁质海轮外壳的腐蚀,制造海轮时,会在海轮船底四周镶嵌比铁更活泼的金属。下列金属适宜船底镶嵌的是________(填选项)。
| A.Pb(铅) | B.Cu | C.Pt(铂) | D.Zn |
(3)对铁“发蓝”处理,其表面将形成致密氧化膜而有效避免腐蚀。
①致密氧化膜能有效阻止铁锈蚀的原因是___________________。
②“发蓝”过程的化学方程式如下,式中X的化学式为_________。
36Fe + 4NaNO2 + 9NaNO3 + 26H2O =" 12X" + 13NaOH + 13NH3↑
③为检验“发蓝”处理的铁质零件表面是否形成致密氧化膜,将该零件浸泡于硫酸铜溶液中,发现零件表面出现红色物质。由此可知该零件“发蓝”处理效果______(填“好”或“不好”),因为_____________(用化学方程式表示)。
某校化学研究性学习小组通过实验研究高炉炼铁的化学原理,设计了如图1实验装置:
(1)已知HCOOH CO↑+H2O,根据该反应制取CO,A处应选用的气体发生装置是 (如图2,填字母序号)。
CO↑+H2O,根据该反应制取CO,A处应选用的气体发生装置是 (如图2,填字母序号)。
(2)装置中仪器①的名称是 。
(3)实验开始时应先点燃 (填“A”或“C”)处的热源;反应后C装置的现象是 ,C、D装置中发生反应的化学方程式分别为 、 ;待硬质粗玻璃管内物质冷却后再停止通CO的目的是 。
(4)该装置有一个明显的缺陷是 ,改进的方法为 。
人类的生产和生活都离不开金属。
Ⅰ.金属元素在自然界中分布很广,在地壳中主要以矿物形式存在。下列矿石的主要成分不属于氧化物的
是 (填序号),孔雀石中铜元素的化合价 ;如将一定量的铁加入到硫酸铜和硫酸锌的混合溶液中,充分反应后,滤液中一定含有的溶质是 ,滤渣中一定含有 。
Ⅱ.铁是应用最广泛的金属。
(1)下图是工业炼铁示意图。其中,焦炭的作用是燃烧提供能量和 ;写出有铁生成的化学方程式为 。
(2)某兴趣小组在实验室中模拟炼铁的化学原理,用一氧化碳还原纯净的氧化铁粉末,实验装置如图。
①实验中玻璃管里固体粉末的颜色变化是 ,澄清的石灰水中发生反应的化学方程式是 。
②该装置有何不妥? 。
(3)该化学兴趣小组的同学利用改正后的装置对一份由铁粉和氧化铁组成的混合物进行探究。他们取了7.2g固体样品放入硬质玻璃管通入足量的CO进行实验,高温灼烧至质量不再变化,称得玻璃管中固体质量为6g,请计算:
①该混合物中铁元素与氧元素的质量比。
②该混合物中铁粉的质量分数。(结果保留一位小数)
试题篮
()