研究小组进行木炭还原氧化铁的探究活动。将木炭、氧化铁及试管充分烘干,并将木炭和氧化铁混合均匀、研磨。取适量上述混合物于试管中,用图1所示的装置加热(试管竖直向上,可使加热时的热量尽少散失)。

【提出问题】实验结束后,试管中的剩余固体X含有哪些成分,质量分别是多少?
【查阅资料】
铁的氧化物被还原时,是从高价铁的氧化物逐级还原成低价铁的氧化物,最后还原成金属铁。铁的氧化物及其部分性质如下: 为红色固体;
为红色固体; 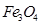 和
和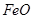 均为黑色固体。其中,
均为黑色固体。其中,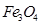 具有很好的磁性,能被磁铁吸引。三种氧化物均不溶于水,但能溶于稀盐酸,分别发生如下反应:
具有很好的磁性,能被磁铁吸引。三种氧化物均不溶于水,但能溶于稀盐酸,分别发生如下反应:
Fe2O3+6HCl ══ 2FeCl3+3H₂O
Fe3O4+8HCl ══ 2FeCl3+FeCl2+4H2O
FeO+2HCl ══ FeCl2 + H2O
黄色的 溶液中滴入无色的KSCN溶液,溶液变为红色,该实验常用于检验
溶液中滴入无色的KSCN溶液,溶液变为红色,该实验常用于检验 ;
; 溶液遇单质铁发生反应:2FeCl3 + Fe = 3FeCl2,溶液变为浅绿色。
溶液遇单质铁发生反应:2FeCl3 + Fe = 3FeCl2,溶液变为浅绿色。
【猜想】固体X可能含有:①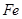 ②
②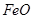 ③
③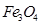 ④⑤
④⑤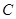
【实施实验】
目的:确定固体X的组成。
| 步骤 |
操作 |
主要现象 |
结论 |
| I |
取部分冷却后的固体X倒在滤纸上,用磁铁充分吸引。 |
部分固体被吸引到磁铁上 |
可能有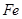 或 或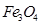 |
| II |
取滤纸上的剩余固体少量,放入图2所示的试管a中,通入氧气,用酒精灯加热。 |
固体剧烈燃烧, b中溶液变浑浊 |
一定有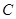 |
| III |
另取滤纸上的剩余固体少量,放入试管中,加入足量的稀盐酸。 |
无明显现象 |
一定没有 |
| IV |
取步骤I磁铁上的固体少量,放入试管中,逐滴加入稀盐酸。 |
产生。 |
一定有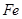 |
| V |
在步骤IV所得溶液中逐滴加入。 |
溶液不变红色 |
一定没有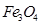 |
【反思改进】
同学们讨论发现,用上述实验方法不能确定固体X中一定没有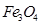 ,理由是。
,理由是。
为确定固体X中是否含Fe3O4并测定其中各成分的质量,同学们又进行了以下实验:
| 步骤 |
操作 |
数据 |
| I |
重新取部分冷却至室温的固体X,称量其质量为m1。 |
m1 =" 17.9" g |
| II |
将称量好的固体X全部放入图3所示的锥形瓶中,称量整套装置及药品的质量为m2;打开分液漏斗旋塞,放入足量稀盐酸后关闭旋塞,待没有气泡产生并恢复至室温,再次称量整套装置及药品的质量为m3。 |
m2 =" 317.9" g m3 = 317.3.g |
| III |
将锥形瓶中剩余的固体过滤、洗涤并干燥,称量其质量为m4。 |
m4 =" 1.1" g |
【获得结论】
(1)为确定固体X中是否含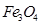 ,m1~m4中应该用到的数据有。
,m1~m4中应该用到的数据有。
(2)固体X的成分及质量分别是。
某同学为了研究炼铁的原理并测定生成铁的质量,用一氧化碳与氧化铁反应,按下图进行实验。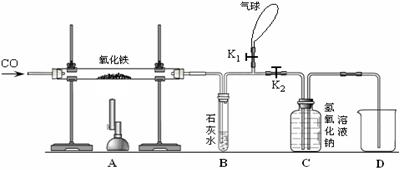
(1)首先,该同学称量氧化铁的质量,然后进行实验,他先打开K1,关闭K2,通入一氧化碳,其目的是排尽玻璃管内的空气,防止加热时因一氧化碳不纯而引起爆炸,然后关闭K1,打开K2,加热,反应一段时间后,冷却,再次称量固体的质量,发现固体质量减少了12克,则生成铁的质量为_____,玻璃管中发生反应的化学方程式为_________________。
(2)装置B中反应的化学方程式是________________________________。
(3)装置C的两个作用是________________________________________________,
(4)实验结束后,烧杯内的溶液中含有的溶质是_________________(写化学式)。
下图为某学习小组探究金属化学性质时所做的四个实验,仔细分析后回答下列问题:

(1)描述
中的实验现象.
(2)写出 中反应的化学方程式.
(3)要证明
的活动性顺序,至少要做的实验是(填序号).
(4)开始反应后
中溶液逐渐变为黄色,原因是.
试题篮
()