某化学反应的微观过程如图,则下列说法中,不合理的是
| A.该反应属于氧化反应 |
| B.甲、乙两物质参加反应的质量比为13:16 |
| C.物质丁的化学式是H2O |
| D.反应前后氧元素的化合价发生了改变 |
下图是工业上制备氢气的微观示意图,其中不同的“球”代表不同的原子。下列说法不正确的是
| A.该反应是化合反应 |
| B.反应前后,原子的种类、数目不变 |
| C.该反应中共涉及一种单质和三种化合物 |
| D.该反应中参加反应的两种分子的个数比为1:1 |
下图是A、B、C三种固体物质的溶解度曲线。下列分析不正确的是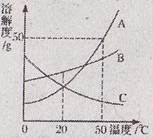
A.50℃时,三种物质的溶解度由大到小的顺序是A>B>C
B.50℃时,把50 g A放入50 g水中能形成75 g A的饱和 溶液
C.将C的饱和溶液变为不饱和溶液,可采用降温的方法
D.分别将三种物质的饱和溶液从50℃将至20℃时,所得溶液溶质质量分数大小关系是B>C=A
下列转化不能一步完成的是
| A.Cu→Cu(NO3)2 | B.HCl→FeCl3 | C.CaCO3→Ca(OH)2 | D.C6H12O6→C |
在玻璃中加入溴化银(AgBr)和氧化铜可制得变色镜片,其中所含物质及变色原理如图所示,下列说法不正确的是
浅色镜片 深色镜片 浅色镜片
| A.溴化银应避光保存 |
| B.变色镜片可反复变色 |
| C.变色镜片颜色变深的过程发生了化合反应 |
| D.变色镜片中的氧化铜在变色过程中质量不变 |
手机、电脑使用的锂电池内的反应可表示为Li+MnO2==LiMnO2。下列说法正确的是
| A.反应中MnO2是催化剂 | B.反应前后锰元素的化合价不变 |
| C.MnO2中Mn的质量分数约为63% | D.生成物LiMnO2为氧化物 |
下列实验方案中,设计合理的是
| A.用点燃的方法除去CO2中少量的CO |
| B.一次性鉴别K2CO3、BaCl2、NaNO3三种溶液,可选用的一种物质是稀盐酸 |
| C.用无色酚酞试液检验NaOH溶液是否变质 |
| D.用氯化钡溶液鉴别稀硫酸和稀盐酸 |
探究金属活动性顺序时,将锌粒放入硫酸铜溶液中,观察到锌粒表面有紫红色物质析出,同时还伴有无色无味气体产生的“异常”现象。推测该气体可能是
| A.氢气 | B.二氧化硫 | C.二氧化碳 | D.一氧化碳 |
氢氧化钴[Co(OH)2]能与酸性溶液反应,可作涂料和清漆的干燥剂。制备方法:
①Co+2HCl═CoCl2+H2↑ ②CoCl2+2NaOH═Co(OH)2↓+2NaCl.下列判断错误的是( )
| A.①为置换反应 | B.钴的金属活动性比铜强 |
| C.②为复分解反应 | D.Co(OH)2可以干燥氯化氢气体 |
在CaCO3→ CaO→ Ca(OH)2 → NaOH的各步转化中,所属的基本反应类型不包括
| A.化合反应 | B.分解反应 | C.置换反应 | D.复分解反应【】 |
下列除去物质中所含杂质(括号内为杂质)的方法正确的是
| A.CO2(HCl)气体,先通过NaOH溶液,再通过浓硫酸 |
| B.O2(N2)气体,通过灼热的铜粉 |
| C.NaCl溶液(Na2CO3,),,加入稀盐酸,至不再产生气泡 |
| D.Fe(Cu)粉,加入足量的硫酸铜溶液 |
下列鉴别物质所使用的试剂或方法不正确的是
| A.硝酸铵和纯碱——水 | B.氧气和氮气——燃着的木条 |
| C.硬水和软水——肥皂水 | D.稀硫酸和氯化钠溶液——酚酞溶液 |
下列说法不正确的是( )
| A.氧气具有氧化性,是一种常见的氧化剂;一氧化碳具有还原性,是一种常见的还原剂 |
| B.氧化反应有快慢之分,有的氧化反应进行的很慢,甚至不易察觉,可称为缓慢氧化 |
| C.红磷、碳、铁等固体都可用于空气中氧气的测定 |
| D.煤、石油、天然气这些化石燃料是不可再生能源,而乙醇、氢气则是可再生能源 |
物质的性质决定其用途.下列叙述错误的是( )
| A.熟石灰能和酸发生反应,可用熟石灰改良酸性土壤 |
| B.氮气化学性质不活泼,可将氮气充入食品包装袋内延长食品保质期 |
| C.“洗洁精”有乳化功能,可用“洗洁精”洗涤餐具上的油污 |
| D.甲醛能使蛋白质失去生理活性,可用甲醛溶液浸泡水产品防腐 |
下列对于物质变化的认识中,正确的是
| A.我们观察到的物质的宏观变化,本质上都是构成物质的微粒不断运动与变化的结果 |
| B.外界条件是导致物质变化的决定性因素 |
| C.物质发生化学变化时,微粒之间一定发生了相互作用,而物质发生物理变化时,微粒之间没有发生相互作用 |
| D.凡是伴随着能量的变化,一定是化学变化 |
试题篮
()