(8分)电石是一种重要的化工原料,极易与水反应:CaC2+2H2O=Ca(OH)2+X↑。
(1)将电石长期露置于空气中,会发生下列变化:
题干中电石与水反应后所得的气体X的化学式是_______,残渣中的主要成分是Ca(OH)2和_______ (写名称)。
(2)工业上利用电石制备某化工原料的流程如下(注:加入NH4Cl溶液的目的是溶解残渣中的难溶盐):
①CaCl2溶液中通人NH3、CO2两种气体,生成CaCO3的化学方程式为_______ 。
②流程中溶液A可循环使用,溶液A中的主要成分的化学式是_______。
③实验室中对过滤所得的固体进行洗涤在_______ 中进行,加洗涤剂时以浸没固体的量为宜。
(3)检验沉淀洗涤干净的方法:取最后一次洗涤液少量置于试管中滴加试剂硝酸银溶液,若观察到_______ ,则证明洗涤干净。
(4)电石应该_______保存。
氨气易溶于水,易与浓硫酸反应,不与碱石灰(干燥剂)反应。氨气还具有还原性,在加热的条件下能将氧化铜还原为铜,同时生成氮气和水。反应的化学方程式为:2NH3 + 3CuO ="==" N2 + 3Cu + 3H2O
某化学小组为验证氨气的组成,设计了如下图所示实验。已知:该实验装置气密性良好,实验前装置C、D的质量分别为65.60 g、132.47 g,实验中所用试剂均足量。
实验步骤:
I.打开K1,关闭K2,通人氨气一段时间后,关闭K1,打开K2。(注:K1接个气球)
Ⅱ.点燃酒精灯加热,待黑色固体部分变为红色后,停止加热。
Ⅲ.继续通氨气至玻璃管冷却。
Ⅳ.记录量气管读数为VmL。
V.称量装置C、D的质量分别为65.36 g、132.74 g。
请回答下列问题:
(1)若用加热氯化铵和熟石灰固体制取氨气,则发生装置与实验室制取二氧化碳气体装置 (填“相同”或“不相同”)。
(2)步骤Ⅳ读数时,应注意视线、刻度线 。三线在一条直线上。
(3)反应生成水的质量为 。
(4)实验过程中通入氨气的作用各不相同。步骤I是 ;步骤Ⅱ是还原氧化铜;步骤Ⅲ是 。
(5)请根据该实验数据列计算式,证明氨气中不含氧元素。相关计算式为 。
某校兴趣小组在我市某地收集到两种岩石样品A和B。他们进行了如下实验探究(B是常用的建筑材料,H是单质,图中部分产物被略去):

(1)写出有关物质的化学式:
A的主要成分 ,B的主要成分 ,X ,Y 。
(2)写出图中下列步骤的化学方程式:
② ,⑥ 。
达州盛产天然气,有“中国气都”之称的美誉。天然气的主要成分是甲烷(CH4),某校化学兴趣小组的同学对甲烷燃烧的产物产生了兴趣,请你参与:
【提出问题】甲烷燃烧后生成哪些物质?
【查阅资料】含碳元素的物质完全燃烧生成CO2,不完全燃烧生成CO;无水CuSO4遇水变蓝。
【猜想与假设】
甲 CO2 H2O ; 乙 CO H2O;
丙 NH3 CO2 H2O; 丁 CO2 CO H2O 。
(1)你认为 同学的猜想是错误的,理由是 。
【实验探究】:为了验证上述猜想与假设,将甲烷在一定量的O2中燃烧的产物依次通过下列装置:
(2)A、B装置的顺序能否颠倒?(填“能"或“否”) 。
(3)实验中观察到A中无水CuSO4变蓝,B、D中澄清石灰水变浑浊,C中红色粉末变成黑色,由此推断 同学猜想成立。
请写出C中红色粉末变成黑色的化学方程式: 。
【反思与交流】为避免有毒的CO污染环境,所以含碳元素的物质燃烧必须满足的条件是 。
D装置后添加一大气球的原因是: 。
下图所示是气体制取与性质验证的组合实验。打开A中分液漏斗活塞后,A、B、C、D、E中均可观察到明显现象。
(1)A中发生反应的化学方程式为 。
(2)B中的现象是 。
(3)E中的现象 ,产生此现象的原因是 (用化学方程式表示)
(4)F装置收集的气体是 。
有限的元素可组成种类繁多的物质,依据表中的元素回答下列问题。
| 元素名称 |
氢 |
碳 |
氧 |
钙 |
铁 |
| 元素符号 |
H |
C |
O |
Ca |
Fe |
(1)若某物质是相对分子质量最小的氧化物,该物质的化学式是 。
(2)若某可燃性气体在氧气中燃烧,能生成两种氧化物,该气体一定含有的元素是 。
(3)若某元素组成的单质及其氧化物,均能和X发生化合反应生成同一种物质。
相关反应的化学方程式是 。
(4)甲~己六种物质的转化关系如下图所示。已知甲能使澄清石灰水变浑浊;己是无色溶液,能在某种黑色固体物质催化下,生成可供给呼吸的气体。(部分反应物、产物及反应条件已略去,“ → ”表示物质之间能发生转化)
①己→丁反应的化学方程式是 。
②下列说法正确的是 (填序号)。
a.丁和己一定含有相同元素
b.乙生成甲和丁一定需要点燃
c.戊转化成甲可能发生置换反应
d.上述反应一定都有气体生成
实验室中验证氧气的性质,进行了如下实验:
①将硫粉点燃伸入氧气集气瓶,燃烧的现象是 ;
②将红热的铁丝伸入氧气集气瓶中,燃烧的方程式为 ;
③将灼热的铜丝(表面已变黑)伸入CO气体中(如图),发生的化学反应的方程式为 ,产生的现象是 ;
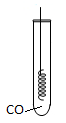
④以上的化学反应都可以称为氧化反应,理由是 ,
而上述①和②的反应也可以称为 (填写反应基本类型)反应。
为充分开发利用海洋资源,全面促进海洋经济持续健康发展,烟台市近日出台《2014年烟台市海洋经济发展意见》。请围绕“海洋”这个话题回答以下问题:
(1)从海水中提取出的粗盐中除了NaCl外,还含有Ca2+、Mg2+、SO42-及泥沙等杂质,为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液。下列操作顺序中最合适的是 。
| A.②④⑤①③ | B.⑤④②③① |
| C.⑤②④③① | D.②⑤④①③ |
(2)海水提取出粗盐后的母液中,还含有较多的氯化镁,用氯化镁可制得金属镁。
①工业上从母液中提取氯化镁的过程如下图:反应1的基本反应类型是 ;物质X是 (填名称)。
②海水制镁过程中对于如何富集镁离子,甲、乙、丙三位同学各自提出自己的设想:
甲:直接往海水中加入石灰乳
乙:高温加热蒸发海水后,加入石灰乳
丙:向晒盐后的卤水中,加入石灰乳
通过分析比较,你认为 的设想最为经济合理(选填“甲”、“乙”或“丙”).
(3)我国化学家侯德榜在氨碱法的基础上创立的“侯氏制碱法”,是向滤出NaHCO3晶体后的NH4Cl溶液中加入NaCl粉末,析出可用作肥料的NH4Cl。NH4Cl和NaCl的溶解度曲线如图所示。
①写出一条P点表示的意义 。
②将t2℃时NH4Cl饱和溶液的温度降到t1℃,溶液中NH4Cl的质量分数会 (填“变大”“变小”“不变”之一)。
③当NH4Cl固体中含有少量NaCl时,可采用 (填“降温结晶”或“蒸发结晶”)的方法提纯NH4Cl。
按要求写出以下反应的化学方程式:
(1)红磷在空气中燃烧 .
(2)镁在二氧化碳中燃烧生成氧化镁和碳 ,所以,金属镁着火时不能用二氧化碳灭火.
(3)硫酸铜溶液中加入铁,只生成铜和硫酸亚铁 .
废液中含有AgNO3和Cu(NO3)2,工厂设计生产方案如图所示:

(1)加入的X、Y物质分别是 .
(2)写出①、③两步反应的化学方程式:第①步: ;第③步: .
(3)你认为此方案的生产目的是 .
如图是画家用碳墨绘画的我国明朝诗于谦《石灰吟》的国画,诗中写道:“千锤万凿出深山,烈火焚烧若等闲,粉身碎骨浑不怕,要留清白在人间”.试回答:

(1)文房四宝中的徽墨是松树枝不完全燃焼产生的炭黑,炭黑书写的字画能够保存多年而不变色,原因是 .若在生活中选用含碳元素的燃料,为确保其充分燃烧,可采取的方法为 ,请写出乙醇不完全燃焼生成二氧化碳、一氧化碳和水的化学方程式 、
(2)诗句中“千锤万凿出深山”所体现物质的变化是 变化;“烈火焚烧若等闲”所体现的化学反应是石灰石受热分解,反应的化学方程式为 ,该反应是反应 (填“吸热”或“放热”).
(3)“要留清白在人间”指的是氢氧化钙暴露在空气中所发生的化学反应,判断氢氧化钙已经变质的方法是 。
下图是密闭体系中某反应的微观示意图,“○”和“●”分别表示两种不同的原子。

(1)该反应所属的基本反应类型是 。
(2)参加反应的“ ”生成的“
”生成的“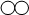 ”、“
”、“ ”三种粒子的个数比是 。
”三种粒子的个数比是 。
(3)写出符合该微观示意图的一个具体化学反应的文字表达式: 。
煤是社会生产、生活中最重要的能源,工业上常把煤进行气化和液化处理,使煤变成清洁能源.煤气化和液化流程示意图如下:
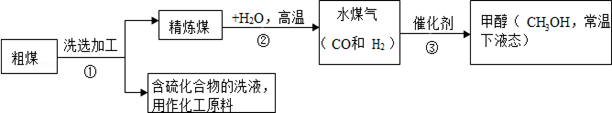
(1)第①步操作发生的是 (填“物理”或“化学”)变化.
(2)第②步是精炼煤与水蒸气的反应,化学方程式为 .
(3)第③步反应的基本类型属于 .
(4)从“绿色化学”的角度分析,“煤的汽化和煤的液化”生产流程的优点 .
下列是对物质的一些性质和变化的描述:
①铜在空气中加热能跟氧气反应;②碱式碳酸铜是绿色的固体;③镁条在空气中燃烧,产生耀眼的白光,放出大量的热,生成白色的固体;④铁矿石被粉碎;⑤胆矾是蓝色的固体.其中,描述物理性质的是______,描述物理变化的是______,描述化学变化的是______,描述化学性质的是______(用序号填写).
A-F为初中化学常见物质,他们由H、C、O、Cl、Na、Ca中的元素组成。
①取D溶液进行实验,操作及部分现象如上图所示,其中E是由两种元素组成的化合物。D与F反应的化学方程式为 。
②关于整个实验下列说法正确的是 。
A、E溶液一定是盐酸溶液
B、烧杯三中的无色溶液一定是中性
C、烧杯三的溶液中一定有阳离子是Na+,Ca2+
D、烧杯三中的溶质存在的情况只有一种
试题篮
()