同学们学习了复分解反应发生的条件后,利用所学知识对稀盐酸与如图中的三种物质之间能否发生反应作出判断,并进行实验验证:
组别 |
甲 |
乙 |
丙 |
实验示意图 |
|
|
|
能否反应 |
能 |
能 |
能 |
实验现象 |
无明显现象 |
有气泡产生 |
产生白色沉淀 |
同学们判断Ca(OH)2溶液和稀盐酸能发生化学反应的依据是生成物中有 生成。
【提出问题】
怎样证明Ca(OH)2溶液与稀盐酸发生了反应?
【分析讨论】
同学们经过讨论后认为,如果盐酸和氢氧化钙减少(或消失),或者有新物质生成,都能证明反应已经发生。
【查阅资料】
CaCl2溶液呈中性。
【实验探究】
方案 |
实验操作 |
实验现象 |
实验结论 |
方案一 |
小羽取少量Ca(OH)2溶液于试管中,先滴入2~3滴无色酚酞溶液,再加入稀盐酸 |
|
反应物消失,二者发生了反应 |
方案二 |
小美向甲组反应后的溶液中加入适量AgNO3溶液 |
产生白色沉淀 |
有新物质生成,二者发生了反应 |
【实验评价】
小凯认为小美的结论不正确,理由是 。
【总结归纳】
(1)Ca(OH)2溶液与稀盐酸发生了化学反应,其反应的化学方程式为 。
(2)对于无明显现象的反应,我们可以分析比较反应物和生成物的性质,从多个角度设计实验进行证明。
【拓展延伸】
将少量CO2通入NaOH溶液中也无明显现象,请你设计一个实验方案证明二者发生了反应 (写出操作方法和现象)。
大明和小明发现市场上有些食品装在充满气体的塑料袋内,显得鼓鼓的。经询问得知:这样充气的包装,主要是为了使食品能较长时间保鲜、保质和不易压碎。那么,这是什么气体呢?大明猜想是二氧化碳,小明猜想是氧气。
(1)假设大明的猜想正确,请你用实验方法证明(要求写出操作步骤和实验现象)
(2)假设小明的猜想正确,请你用实验方法证明(要求写出操作步骤和实验现象)
(3)你认为食品充气包装中,对所充气体的要求是(写出两点):
① ,② 。
(4)根据⑶中要求,你认为 (填"大明"或"小明")的猜想正确。
下列关于测定空气中氧气含量的实验分析中(图中药品为红磷和水),不正确的是
| A.氮气不与红磷反应且难溶于水,是设计该实验的依据之一 |
| B.不能用木炭代替红磷 |
| C.图I中进入集气瓶的水约占烧杯中水体积的五分之一 |
| D.图II所示装置也可以测定空气中氧气含量 |
下列物质的转换是我们已学过的常见物质反应,E能使带火星的木条复燃,H能使澄清石灰水变浑浊,在反应②中,B的质量和化学性质均不改变。
则图中E为______,H为____ _,属于化合反应的是__ _,(填序号,下同),属于分解反应的是___ _,写出③的符号表达式____ __________。
下面是几种实验室制取气体的发生装置与收集装置。
(1)指出仪器名称Ⅰ ,Ⅱ 。
(2)实验室可用二氧化锰与双氧水制取氧气。若要较好地控制产生氧气的速度,应选用装置 (填编号)。写出其反应的化学方程式 。
(3)、用D装置收集氧气,操作的正确顺序为 (填编号)。
a.将导管伸入集气瓶口,气体进入瓶中
b.将装满水的集气瓶倒置在水槽中
c.当气体收集满时,用毛玻璃片盖上瓶口,将集气瓶移出水面放置
(4)若用E装置进行排空气法收集氧气,气体应从 (填“a”或“b”)端通入。
某校化学兴趣小组将用剩的过氧化氢溶液倒入放有生锈铁钉的废液缸中,发现产生了大量的气泡,经检验此气体为氧气。根据学过的知识初步判断,是生锈铁钉中的某种物质加快了过氧化氢的分解,那么究竟是哪种物质加快了过氧化氢的分解速率?请你参与他们的研究,分享和体验探究实验的快乐。
【猜想与假设】
甲同学:铁钉表面的氧化铁加快了H2O2的溶液分解。
乙同学:铁钉里的 加快了H2O2的溶液分解。
【设计方案和实验】完成下列表格
| 实验方案 |
实验现象 |
结论 |
| 方案一:向盛有10mL 5% H2O2溶液的试管中加入2g 氧化铁粉末,将一根带火星的木条放在试管口,观察现象。 |
|
甲同学结论成立。 |
| 方案二:向盛有10mL 5% H2O2溶液的试管中加入 粉末,将一根带火星的木条放在试管口,观察现象。 |
无现象 |
乙同学结论 。 (填“成立”或“不成立”) |
【讨论交流】丙同学认为“方案一”只能说明Fe2O3加快了H2O2溶液的分解,并不能说Fe2O3就一定是催化剂。你是否支持丙同学的观点? ,如果要证明氧化铁是催化剂,就要设计一个实验来证明,这个实验的设计原理是 。
【拓展】
(1)实验证明Fe2O3粉末可以作为H2O2分解的催化剂。该反应的文字表达式
(2)下表是丙同学探究影响H2O2分解速率时所记录的部分数据,通过对数据分析,你能得出什么结论? 。
用足量等体积H2O2溶液制取相同体积O2所需的时间:
某拓展性学习小组在学校科学实验创新比赛中,做了一个有趣的实验,装置如图。
实验设计:三颈烧瓶中充满二氧化碳气体,A颈、B颈分别连接充满氢氧化钠溶液和盐酸的注射器,C颈插有两端开口的玻璃导管(伸入瓶内的一端连有小气球),装置气密性良好。
实验操作:先通过A颈往瓶内注入氢氧化钠溶液,观察到小气球的形状发生了变化;过一段时间后再通过B颈往瓶中注入盐酸,发现小气球的形状又发生了改变。
请描述小气球形状的变化情况,并对此作出合理的解释。

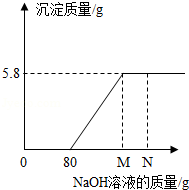
向100克MgCl 2和HCl的混合溶液中,逐滴加入10%的氢氧化钠溶液,反应情况,如图所示。
(1)当滴加氢氧化钠溶液的质量至N点时所得溶液的pH值为 (填编号);
A.大于7 B.等于7 C.小于7
(2)通过计算,确定M点的值,写出计算过程。
生活中常见物质的性质、制法的是化学研究的重要内容。
(1)复分解反应发生后,生成物肯定不会是 (填"单质"或"化合物")。
(2)盐酸与氢氧化钠溶液反应时溶液pH的变化如图所示。下列说法正确的是 。
a.m点所示溶液为碱性
b.n点所示溶液中加紫色石蕊溶液呈红色
c.p点所示溶液中的溶质为NaCl和NaOH
d.该图所对应操作是将盐酸滴入氢氧化钠溶液中
(3)浓硫酸和浓盐酸敞口放置均会变稀,这是为什么?
(4)如图装置可作一氧化碳还原氧化铁的实验,并检验生成的气体产物。

①B装置玻璃管里可观察到的现象为 。
②C装置中反应的化学方程式为 。
③实验结束后,若要确定A装置的溶液中溶质的成分,请设计合理的实验方案,简要写出实验步骤、现象和结论。(提示:Na 2CO 3溶液呈碱性)
(5)工业上可利用"铝热反应"焊接钢轨、冶炼难熔金属等,其原理是在高温下用铝将这些金属从其氧化物中置换出来,若用铝与四氧化三铁反应来制取25.2kg铁,理论上需要消耗铝的质量是多少?

已知:①NaHCO3 固体受热分解 2NaHCO3 Na2CO3+CO2↑+H2O;②Na2CO3 受热不分解。回答下列问题:
(1)关于 NaHCO3 固体的叙述错误的是 (填标号)。
A.俗称小苏打 B.难溶于水
C.可与稀盐酸发生反应 D.是发酵粉的主要成分之一
(2)欲测定某 NaHCO3固体样品(只含Na2CO3杂质且分布均匀)中NaHCO3的质量分数,将 5.0g 该样品加热至质量不再改变,测得剩余固体的质量、生成CO2的质量随时间变化如图所示。
①NaOH溶液的pH 7(填“>”、“=”或“<”),用该溶液将生成的CO2完全吸收,发生反应的化学方程式为 。
②由图中数据可知,上述5.0g NaHCO3 样品完全分解产生CO2的质量为 g,产生H2O的质量是 g。
③计算该样品中NaHCO3的质量分数(根据化学方程式写出完整的计算步骤)。

用溶质质量分数为5%的NaOH溶液中和73g的稀盐酸,反应过程中溶液的酸碱度变化如图所示。请计算
(1)用质量分数为10%的氢氧化钠溶液配制5%的氢氧化钠溶液100g,需要水 克。
(2)当a为80g时,所得溶液中溶质的质量分数是多少(结果精确到0.1%)?

某同学在实验室用氯酸钾和二氧化锰的混合物制取氧气,并对反应后固体剩余物进行回收、利用,实验操作流程及数据记录如下

请回答下列问题:
(1)滤液可作化肥使用,你认为它属于 肥;
(2)该同学制得氧气的质量 g;
(3)计算滤液中溶质质量分数。
海水中蕴藏着丰富的资源,海水“晒盐”过程中可得到粗盐和卤水.粗盐中常含有多种杂质,必须对其分离和提纯,才能用于生产和生活;卤水经常用作工业制镁的原料.
(1)实验室除去粗盐中不溶性杂质的实验步骤为:溶解、过滤、蒸发结晶.在三步中都要用到的一种玻璃仪器是 .
2杂质,得到较为纯净的食盐晶体.请简述实验操作步骤: .
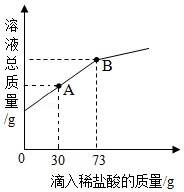
22的混合粉末6g,向其中加入20g水,经充分溶解后,再逐滴加入溶质质量分数为10%的稀盐酸.烧杯中溶液的溶液的总质量与加入稀盐酸的质量关系如图所示,请回答下列问题:
①当滴入稀盐酸30g时(即图中A点时),烧杯内溶液中的溶质是 (填写化学式).
②当滴入稀盐酸73g时(即图中B点时),试通过计算,求此温度时所得不饱和溶液中溶质的质量(计算结果精确至0.1g).
某学校兴趣小组在参与"五水共治"行动中,考察了某工厂的废水处理工程,并取该厂未经处理的废水样品进行测定分析:
(1)用紫色石蕊试液检验废水的酸碱性,石蕊试液呈 色,说明该废水显酸性.
(2)另取废水样品少量,滴加适量Ba(NO 3) 2,有白色沉淀产生,说明该废水中一定含有的酸根离子是 .
(3)同学们进一步了解到该废水中中含有一种酸,为测定其所含酸的质量分数,取该废水200克于烧杯中,逐渐加入硝酸钡溶液,生成的沉淀质量与加入硝酸钡溶液的质量关系如图所示,请计算废水中硫酸的质量分数.(假设该废水中的其他物质均溶于水且不与硝酸钡溶液反应).

试题篮
()