下列图象与对应的叙述相符合的是( )
| A. |
|
| B. |
|
| C. |
|
| D. |
|
数据处理能及时获得更多的信息。下列图示中,不能正确反映化学原理及实验操作规范的是( )
A.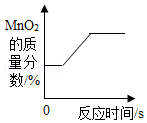 加热一定质量的KClO3和MnO2的混合物
加热一定质量的KClO3和MnO2的混合物
B.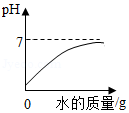 稀释浓硫酸
稀释浓硫酸
C.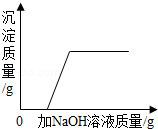 向pH=4的CuSO4溶液中滴加NaOH溶液
向pH=4的CuSO4溶液中滴加NaOH溶液
D.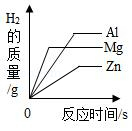 向足量相同质量分数的稀硫酸中分别加入等质量Zn粉、Al粉、Mg粉
向足量相同质量分数的稀硫酸中分别加入等质量Zn粉、Al粉、Mg粉
向一定量的稀盐酸中,分别加入足量的水、金属铁、氢氧化钙溶液、硝酸银溶液,下列图示正确的是( )
A.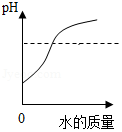 B.
B.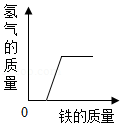
C.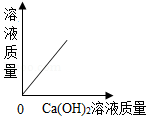 D.
D.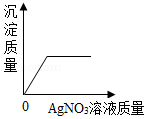
下列图示与相应的文字描述完全符合的是( )
A.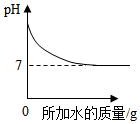 加水稀释NaOH溶液
加水稀释NaOH溶液
B. 加热分解KMnO4固体
加热分解KMnO4固体
C.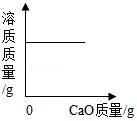 向饱和石灰水中加入CaO
向饱和石灰水中加入CaO
D.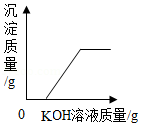 向稀硫酸和硫酸铜的混合溶液中加入KOH溶液
向稀硫酸和硫酸铜的混合溶液中加入KOH溶液
小明利用稀硫酸与生锈的铁屑反应制取硫酸亚铁,实验流程如图:
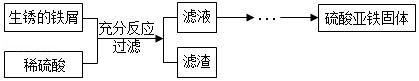
资料:①Fe2(SO4)3+Fe═3FeSO4;②硫酸亚铁容易被氧化为硫酸铁等物质。
(1)配制50克溶质质量分数为19.6%的稀硫酸,需溶质质量分数为98%的浓硫酸 克。
(2)写出该实验中的一条化学方程式(除资料①中的反应外) 。
(3)稀硫酸与生锈的铁屑充分反应后,要确保铁有少量剩余,其目的是 。
化学实验是进行科学探究的重要方式。
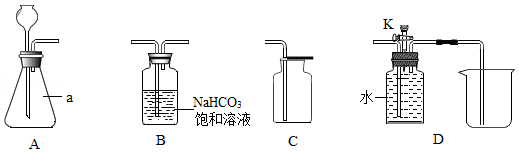
(说明:NaHCO 3饱和溶液的作用是吸收氯化氢气体;装置气密性良好;其他连接装置略)
实验一 氧气的实验室制取
(1)写出图中标号a仪器的名称: 。
(2)用A、C装置制取氧气,所需药品是 。
实验二:制取较纯净的CO 2并探究其性质
[药品准备]将30g质量分数为36%的浓盐酸稀释为9%的稀盐酸
(3)计算加入水的体积为 mL.(水的密度为1.0g/cm 3)
(4)配制稀盐酸时所需仪器有 (填序号)。
①量筒 ②玻璃棒 ③蒸发皿 ④胶头滴管 ⑤烧杯 ⑥托盘天平
[操作步骤]
步骤一:在A装置中加入足量石灰石,依次连接A、B、C装置,再向A中加入适量的稀盐酸。一段时间后,经检验A、B装置内的空气已排净。写出A中发生反应的化学方程式: 。
步骤二:待A中反应停止后,拆下C装置,再将D装置与A、B连接,关闭活塞K, (补全实验步骤),在D中收集实验所需的较纯净的CO 2。
步骤三:打开活塞K,用一支50mL注射器从D中缓慢抽取20mL CO 2,关闭K,再抽取20mL滴有紫色石蕊溶液的水溶液,用橡皮塞堵住注射器的针孔,轻轻振荡。观察到的现象: 。
[问题交流]步骤一中能充分证明A、B装置内的空气已排净的可靠方法是 。
[后续探究]……
将20g质量分数为98%的浓硫酸稀释为25%的稀硫酸。下列说法中不正确的是( )
A.实验步骤:计算、量取、混匀、装瓶贴签
B.实验仪器:量筒、胶头滴管、烧杯、玻璃棒、细口瓶
C.稀释浓硫酸时将水沿烧杯内壁慢慢注入浓硫酸中,并不断搅拌
D.浓硫酸不慎沾到皮肤上,应立即用大量水冲洗,再涂上3%~5%的碳酸氢钠溶液
盐酸是重要的化工原料,也是实验室中最常用的化学试剂之一。
(1)用质量分数为37%的浓盐酸配制1000g质量分数为0.37%(pH约为1)的稀盐酸。
①所配稀盐酸中溶质的质量为 g,所需浓盐酸的质量为 g。
②已知浓盐酸密度为1.19g/cm3,量取上述所需浓盐酸用到的仪器是 (填标号)。
A.10mL量筒
B.50mL量筒
C.试管
D.胶头滴管
③测定所配稀盐酸的酸碱度,应将pH试纸放置在 上。
(2)取少量氢氧化钙粉末于试管中,加入2mL水,振荡,得到白色浑浊液,滴加1滴酚酞溶液,再滴加稀盐酸至反应完全,可观察到的现象是 。
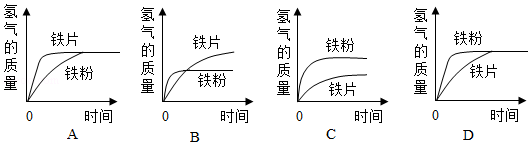
(3)取等质量的铁片和铁粉放入两支试管中,分别加入相同体积相同浓度的稀盐酸。
①铁与稀盐酸反应的化学方程式为 。
②如图示意图中,与实验结果相符的是 (填标号)。
潍坊有丰富的海洋资源,氯化钠占整个海洋盐类的80%以上.下列有关氯化钠的说法正确的是( )
A.室温下的氯化钠饱和溶液不能再溶解氯化钾
B.取出部分上层溶液,可将接近饱和的氯化钠溶液变为饱和
C.可用硝酸银溶液鉴别氯化钠和氯化镁溶液
D.将100g质量分数为20%的氯化钠溶液稀释为10%,所用的仪器有:烧杯、量筒、玻璃棒和胶头滴管
"酸"一词从有酸味的酒而来。常温下酸溶液的pH 7(">"、"<"或"="),硫酸是用途广泛的酸,实验室稀释浓硫酸的正确方法是 。
工业上常用红锌矿(主要含ZnO)和18﹣25%的稀硫酸为原料制取硫酸锌.
(1)硫酸锌中硫元素和氧元素的质量比是 .
(2)100g溶质质量分数为98%的浓硫酸配制成溶质质量分数为20%的稀硫酸,需要水的质量是 g.
物质的变化常伴随能量变化。
(1)能量的变化常表现为温度的改变。稀释浓硫酸时,溶液的温度 ;
(2)氢气被认为是理想的清洁、高能燃料。请写出氢气在氧气中燃烧的化学方程式 。
下列四个图象分别对应四个变化过程的一种趋势,其说法正确的是( )
①表示在等质量的铁粉和锌粉中分别加入足量的溶质质量分数相等的稀硫酸
②用加热一定质量的氯酸钾和二氧化锰固体混合物的方法制取氧气
③向一定量的硫酸和硫酸铜的混合溶液中逐滴加入一定质量分数的氢氧化钠溶液
④向一定量的氢氧化钠溶液中加水稀释,溶液的pH变化

| A. |
上述图象只有2个正确 |
| B. |
上述图象只有3个正确 |
| C. |
上述图象全部正确 |
| D. |
如果将②中的纵坐标改为固体总质量,该图象能正确反映相应的变化趋势 |
酸、碱、盐在生产生活中具有广泛的用途.
(l)制作“叶脉书签”需用到10%的氢氧化钠溶液.现配制50g质量分数为10%的氢氧化钠溶液.
①若用氢氧化钠固体配制,需称量氢氧化钠的质量为 g.
②用氢氧化钠固体配制10%的氢氧化钠溶液过程中需要用到的仪器除了托盘天平、药匙、量筒、烧杯、胶头滴管、试剂瓶外,还需要 .
③下列操作正确的是 (填字母).
A.称量氢氧化钠固体时,左盘放砝码
B.在托盘天平的左右托盘上垫滤纸称量氢氧化钠固体
C.将准确称量的氢氧化钠固体放入装有水的量筒中溶解
D.将配制好的氢氧化钠溶液装入试剂瓶中,塞好瓶塞并贴上标签
④若用20%的氢氧化钠溶液加水(水的密度为lg/cm3)配制50g质量分数为10%的氢氧化钠溶液,需20%的氢氧化钠溶液的质量为 g;配制时应选用 mL的量筒量取水(填“10”或“50”).
(2)某固体粉末可能含有碳酸钙、硫酸钠、氯化钠、氯化钡、硫酸铜中的一种或几种.为确定该固体粉末的成分,进行了如下实验:
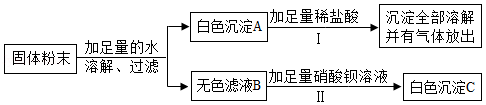
回答下列问题:
①反应I 的化学方程式为 .
②白色沉淀C是 (填化学式).
③原固体粉末中一定不含 (填化学式).
试题篮
()