回答下列问题。
(1)某兴趣小组参观火力发电厂,了解到废气中的SO2、NO2、CO、CO2会影响环境,设计如图流程处理废气。
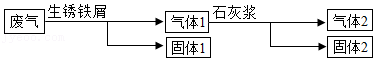
①用生锈铁屑处理废气中的CO,体现CO 性。
②用石灰浆不用石灰水的原因是 。
③固体2中有 (写两种物质)。
(2)A~D为初中化学常见物质,转化关系如图。A是由两种元素组成的钙盐,C是火力发电厂排放的温室气体。
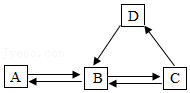
①B转化为A的化学方程式为 。
②若D广泛用于玻璃、洗涤剂的生产,则D转化为B的基本反应类型是 ;检验D中阴离子的方法是 。
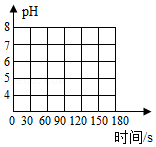
③将足量C通入石蕊溶液中,现象是 ;测得该溶液pH=4,加热至90s时C完全排出,画出加热过程pH变化图像。
了解溶液的酸碱性,学会测定溶液酸碱度对于生活、生产以及人类的生命活动具有重要的意义。请回答下列问题。
(1)测定溶液的酸碱度时,用干净的玻璃棒蘸取待测液滴在 上,然后再与标准比色卡对照,得出该溶液的pH。
(2)测得家庭生活中常用的炉具清洁剂pH 7(填“<”“=”或“>”)
(3)某盐酸溶液pH=3,要使其pH>7可采用的方法是 。
铅蓄电池在生产、生活中使用广泛。其构造示意图如图1,回答下列问题:

(1)铅蓄电池充电时是将电能转化为 (填序号)。
a、机械能 b、热能 c、化学能
(2)铅蓄电池放电过程中,反应的化学方程式为Pb+PbO 2+2H 2SO 4═2PbSO 4+2H 2O,据此可知,铅蓄电池在放电时,溶液的pH不断 (填"增大"、"减小"或"不变")。
(3)如图2是回收废铅蓄电池的一种工艺流程:
①从材料分类角度看,塑料是一类 材料。
②废硫酸可以与氟磷灰石[Ca 5(PO 4) 3F]反应,反应的化学方程式为2Ca 5(PO 4) 3F+7H 2SO 4═3CaSO 4+3Ca(H 2PO 4) 2+2HF,反应产物中可用作化肥的物质是 。
③如表是一些金属熔点的数据:
| 金属 |
锡 |
铅 |
铋 |
镉 |
| 熔点∕℃ |
231.9 |
327.5 |
271.3 |
320.9 |
日常所用保险丝由铋、铅、锡、镉等金属组成,其熔点约为 (填序号)
A.300﹣320℃
B.230﹣250℃
C.60﹣80℃
D.20﹣40℃
④废硫酸直接排放会污染环境,拟选用如表物质中和后再排放:
| 物质 |
CaCO 3 |
Ca(OH) 2 |
NH 3 |
NaOH |
| 市场参考价(元/kg ) |
1.8 |
2.0 |
6.5 |
11.5 |
已知:2NH 3+H 2SO 4═(NH 4)SO 4,如果要求花最少的钱来中和等质量、等浓度的废硫酸,则应选择 (填序号)。
a、CaCO 3 b、Ca(OH) 2c、NH 3d、NaOH。
小科从标签得知雪碧成分中有水、二氧化碳、柠檬酸、柠檬酸钠等。查阅资料知道1体积雪碧中含有约3体积二氧化碳,柠檬酸的含量约为2.8g/1000mL.柠檬酸与碳酸钠反应的化学方程式为:
2C6H8O7+3Na2CO3═2C6H5O7Na3+3CO2↑+3H2O。
他用一瓶500mL的雪碧做了如下实验:。
实验步骤 |
步骤一 |
步骤二 |
步骤三 |
步骤四 |
操作过程 |
倒出三分之二雪碧,测其pH |
在剩余雪碧中加入约6g Na2CO3 |
立即盖上瓶盖,摇匀。 |
测溶液pH |
现象或结果 |
pH约为3 |
产生大量气泡 |
气泡消失,瓶子略瘪 |
pH约为9 |
【发现问题】CO2去哪儿了?
【提出猜想】①CO2被溶解了;②CO2与H2O发生了反应;③CO2与Na2CO3溶液发生了反应。小思否定了猜想①和②,其理由是 。
【设计实验】对猜想③进行实验探究。
实验编号 |
实验一 |
实验二 |
实验三 |
实验四 |
实验装置 |
|
|
|
|
操作过程 |
Na2CO3溶液中滴加CaCl2溶液 |
Na2CO3溶液中通入过量CO2后,滴加CaCl2溶液 |
收集一瓶CO2,加入30mL饱和Na2CO3溶液,盖上瓶盖摇匀 |
将实验三的溶液低温蒸发、干燥,得到的白色粉末按如图所示装置进行实验 |
实验现象 |
产生白色沉淀 |
无明显变化 |
瓶变瘪,瓶底有晶体析出 |
A试管口有水滴,澄清石灰水变浑浊 |
根据实验探究过程,回答下列问题:
(1)设计实验一的作用是 。
(2)实验四中A试管口略向下倾斜,其目的是 。
(3)根据实验探究得出:CO2与Na2CO3溶液反应的化学方程式: 。
试题篮
()