已知粗盐中含有泥沙、氯化钙和硫酸镁等杂质。为制得纯净的氯化钠固体,某化学兴趣小组进行了如下操作:
(1)写出X溶液中溶质的化学式 。
(2)请设计实验证明溶液B中含有NaOH.(简要写出实验步骤和现象)
(3)最后制得氯化钠的质量大于粗盐中氯化钠的质量,写出一个可使氯化钠质量增加的化学方程式 。
为了除去粗盐中CaCl2、MgCl2、Na2SO4等可溶性杂质,需进行如下操作:①溶解;②依次加过量的BaCl2、NaOH、Na2CO3溶液;③过滤;④加适量盐酸;⑤蒸发、结晶。[提示:Mg(OH)2、BaSO4、BaCO3难溶于水;微溶物不形成沉淀;Na2CO3溶液呈碱性]
(1)以上操作中所发生的复分解反应共有 个。
(2)操作①、③、⑤要用到同一种玻璃仪器,该仪器在操作⑤中的作用是什么?
(3)请设计实验方案证明操作③所得溶液中含有NaOH.(写出实验步骤和现象)
除去NaCl溶液中CaCl2、MgCl2、Na2SO4杂质的操作有:①溶解;②依次加过量的BaCl2、NaOH、Na2CO3溶液;③过滤;④加适量的盐酸;⑤蒸发结晶。
(1)过滤后滤液中的溶质有 种,过滤中玻璃棒的作用是 。
(2)加盐酸后反应的化学方程式为 。(写出一个即可)
为除去粗盐中的CaCl2、MgCl2、Na2SO4等可溶性杂质,进行了如下操作:①溶解;②依次加过量的BaCl2、NaOH、Na2CO3溶液;③过滤;④加适量盐酸;⑤蒸发结晶。加入Na2CO3溶液的作用是 ;操作③得到固体的成分有CaCO3、BaCO3和 ;操作④中测定溶液的酸碱度可以使用 。
化学与人类的生产生活密切相关,已为人类的进步作出了巨大的贡献。请用所学的化学知识回答下列问题。
(1)生活中常接触到"加碘食盐","高钙牛奶",其中的"碘"和"钙"应理解为 (填编号)。
A元素 B.原子 C.单质
(2)糖类物质是人体能量的主要来源,其中最基本的糖类物质是葡萄糖,其化学式为 。当血液中的葡萄糖浓度过低时,人会产生头晕、心悸等低血糖症状,因此我们每天去合理摄入糖类物质。
(3)"84"消毒液是一种常用的消毒剂,其主要成分是次氯酸钠(NaClO),制取它的方程式为2NaOH+Cl 2=NaClO+X+H 2O,则X的化学式为
(4)不法分子,常用铜锌合金假冒黄金行骗,请你写出一种鉴别真假黄金的化学方法:
(5)某工厂用粗盐配制的氯化钠溶液中,经分析发现含有少量的氯化钙杂质,请你写出,除去该杂质的化学方程式: 。
在“一定质量分数的氯化钠溶液的配制”和“粗盐中难溶性杂质的去除”两个实验中都能使用到的仪器是( )
A.烧杯、玻璃棒、托盘天平、量筒
B.烧杯、玻璃棒、托盘天平、试管
C.托盘天平、量筒、烧杯、漏斗
D.蒸发皿、酒精灯、烧杯、铁架台
请从A或B两题中任选一个作答,若两题均作答,按35﹣A计分.
| A用浓硫酸配制100g 9.8%的稀硫酸 |
B粗盐中难溶性杂质的去除 |
| (1)实验需要5.4mL浓硫酸和90mL水.量取两种液体用到的仪器有 (填序号). (2)稀释时,需将浓硫酸缓慢倒入水中,并不断进行搅拌,其原因是 . |
(1)过滤需要用到的仪器有 (填序号). (2)蒸发过程中,需不断进行搅拌,其原因是 . |
| 可供选择的主要仪器: ①试管 ②烧杯 ③蒸发皿 ④托盘天平 ⑤10mL量筒 ⑥100mL量筒 ⑦药匙 ⑧胶头滴管 ⑨漏斗 ⑩酒精灯⑪铁架台⑫玻璃棒 |
|
| |
|
下列实验方法错误的是( )
选项 |
实验目的 |
实验方法 |
A |
鉴别硬水和软水 |
加入肥皂水振荡,观察是否有大量泡沫 |
B |
鉴别蔗糖和NH4NO3固体 |
加入少量水溶解,测量溶液温度 |
C |
除去粗盐在难溶性杂质 |
加适量水溶解,过滤,蒸发 |
D |
除去KCl溶液中少量CuCl2 |
滴加NaOH溶液至不再生成沉淀,过滤 |
A.AB.BC.CD.D
完成下列实验。
(1)现提供下列装置:

①写出上图中B装置甲仪器的名称 。
②实验室用A装置进行高锰酸钾制氧气的实验,化学方程式为 ,用D装置收集氧气,气体由导管 进入(填“a”或“b”)
③实验室用锌粒和稀盐酸制氢气,用C装置代替B装置的优点是 :若要检验氧气中是否含有氯化氢气体,可将气体通过盛有 溶液的D装置(填“AgNO3”或“饱和NaHCO3溶液”)
(2)对一定质量的粗盐(含泥沙)进行初步提纯。
①实验主要步骤:称量与 、过滤、蒸发;实验中多次使用玻璃棒。过滤时它的作用是 ;蒸发时,待蒸发皿中出现 时停止加热。利用余热将滤液蒸干。
②下列因素会导致获得的精盐质量偏小的是 (填序号)
a.蒸发时液滴溅出 b.过滤时,滤纸破损
c.粗盐中加入过量的水 d.过滤后,滤纸上的泥沙未同水冲洗。
海洋是巨大的资源宝库,从海洋中可以获得很多物质,连云港水资源丰富。
(1)通过晾晒海水得到的粗盐中含有多种可溶性杂质和不溶性杂质(泥沙等)。实验室中除去粗盐中不溶性杂质获得精盐的步骤是:溶解→过滤→蒸发→计算产率等。
①过滤操作中玻璃棒的末端要轻轻的斜靠在 一边。蒸发时为防止液滴飞溅,除用玻璃棒搅拌外,还可以采取的操作是 。
②下列操作可能导致精盐产率偏高的是 (填字母)
a.食盐没有完全溶解即过滤 b.过滤时液面高于滤纸边缘
c.器皿上粘有的精盐没有全部转移到称量纸上
(2)海水中含量最多的氯化物是氯化钠,其次是氯化镁。如图1是从海水中获得氯化镁溶液的流程。
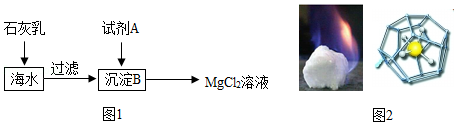
①在海水中加入石灰乳后,发生反应的化学方程式是 。
②上述过程中试剂A与沉淀B发生的是中和反应,则试剂A是(填名称) 。
(3)2017年5月18日,在中国南海海域实现可燃冰(CH 4•nH 2O)试采成功,这将使人类能源格局翻开新篇章。
①可燃冰中,水分子形成一种空间笼状结构,甲烷和少量N 2、CO 2等分子填入笼内空隙中,无固定的化学计量关系,因此可燃冰属于 (选填"纯净物"或"混合物")。
②若某种可燃冰中CH 4与H 2O的质量比是1:9,则该可燃冰中n= 。
③可燃冰中甲烷完全燃烧的化学方程式是 。
根据"粗盐中难溶性杂质的去除"实验,回答有关问题.
(1)实验步骤:
①溶解 称取5.0g粗盐,逐渐加入10mL水中,直到不再溶解,剩余粗盐1.2g.
②过滤
③蒸发 请从溶解度的角度分析,试验中不采用降低溶液温度的方法得到精盐的依据是
④计算产率 得到精盐3.2g,则精盐的产率为 (计算结果保留一位小数).
(2)整个实验中至少要进行 次称量.
(3)从海水中获得的粗盐,经过上述实验得到的精盐属于 (填"混合物"或"纯净物").
某校化学兴趣小组进行粗盐(含有泥沙)提纯实验,并利用所得精盐配制100g20%的氯化钠溶液。
实验一:如图1是甲同学进行粗盐提纯实验的操作示意图。
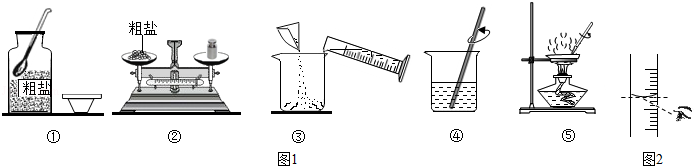
(1)操作①中的一处明显错误是 。
(2)操作⑤对应的实验中,停止加热的恰当时机是 。
(3)该同学实验中缺少过滤操作,在此操作中玻璃棒的作用是 。
实验二:乙同学用提纯得到的精盐配制100g20%的氯化钠溶液。
(4)配制时,除如图1提供的仪器外,还需要试剂瓶、镊子和 (填一种仪器名称)。
(5)若其他操作均正确,采用如图2所示观察方式量取水,则所配溶液的溶质质量分数 _ (填">"、"<"或"=")20%。
试题篮
()