初中化学中常见的物质A~G有如图所示的转化关系(“—”表示两种物质能够发生反应,“→”表示物质间存在着相应的转化关系,反应条件、部分反应物和生成物未列出)。已知B是一种黑色的固体,F是一种常用的溶剂,B、C、D、E是不同类别的物质。请分析后回答下列问题:
(1)F的化学式为 。
(2)请写出B→G的化学方程式 。
(3)请描述C与D反应的现象 。

化学来源于生活又服务于生活,它在保护身体健康、能源、环境和材料等方面,为满足人类不断增长的物质、精神需求作出了巨大的贡献。请用所学的化学知识回答下列问题。
(1)生活中常用"加碘食盐"、"高钙牛奶"来补充人体所需的"碘"和"钙",这里的"碘"和"钙"应理解为 (填字母)。
| A. |
元素 |
| B. |
原子 |
| C. |
单质 |
(2)能供给呼吸的气体是 ,该气体进入人体后会与最基本的糖类物质葡萄糖发生反应,为人体活动提供能量。
(3)胃酸的主要成分是盐酸,胃舒平主要成分【Al(OH)3)】常用于治疗胃酸过多症,写出用胃舒平治疗胃酸过多症时的化学反应方程式 。
(4)长征五号火箭目前是中国运载能力最大的火箭,起飞推力超过1000吨,运载能力接近25吨。它使用由零下183℃的液氧和零下253℃的液氢为芯一级和芯二级发动机的推进剂,所以该火箭也被称为"冰箭"。将氧气和氢气转化为液氧和液氢的变化属于
变化,芯一级和芯二级发动机工作时发生反应的化学方程式为 ,使用氢气作为燃料的突出优点是 。
(5)2021年3月全国两会期间,政府工作报告中提到的"碳达峰"、"碳中和"成为热词。碳中和必须做好"加减法",一手减少二氧化碳等温室气体排放,一手发展碳捕集和封存技术等,实现排放量和吸收量的平衡。碳捕捉技术常用NaOH溶液来捕捉二氧化碳,工艺流程如图所示(部分条件及物质未标出)。捕捉室中发生反应的化学方程式为 ,该转化中循环使用的物质是 。

工业上可以通过如图工艺流程处理工厂排放的含二氧化硫的尾气,并获得硫酸和氢气。

主反应器中发生反应的化学方程式为:SO2+2H2O+I2═H2SO4+2HI
请回答下列问题:
(1)该反应的物质中属于氧化物的有 。
(2)该反应前后,化合价发生变化的元素有碘和 。
(3)尾气中SO2的质量分数为10%,若吸收该尾气80t,理论上能够生产硫酸的质量为
t。
(4)在整个工艺流程中,能被循环利用的物质是 。
有限的元素可以组成种类繁多的物质,依据表中的元素回答下列问题。
| 元素名称 |
铜 |
钠 |
钙 |
氧 |
碳 |
氢 |
| 元素符号 |
Cu |
Na |
Ca |
O |
C |
H |
(1)常用作冶炼金属的还原剂是 (任写一种物质的化学式)。
(2)能使紫色石蕊溶液变红的有机物是 (写化学式)。
(3)战国《周礼》中记载"煤饼烧蛎房(即牡蛎壳)成灰",蔡伦将此"灰"溶于水即得碱。请写出蛎房烧成灰的化学方程式 。
(4)甲、乙、丙都是由以上元素组成的初中化学常见物质,其中甲为氧化物,它们之间有如图所示转化关系(部分反应物、生成物及反应条件已略去,"→"表示某一种物质经一步反应可转化为另一种物质)。
①若丙为黑色固体,则乙→丙发生反应的化学方程式为 。
②下列推断正确的是 (填序号)。
| A. |
a.甲只能为H 2O或CO 2 |
| B. |
b.乙可以为氧化物或碱、盐 |
| C. |
c.乙和丙不可能为同种类别的物质 |
| D. |
d.丙→甲发生的反应可能是化合反应或分解反应、置换反应、复分解反应 |

“太阳能光伏发电”能有效推进“碳中和”,发展“低碳经济”,其关键的材料是高纯硅。如图是高纯硅的简易生产流程。
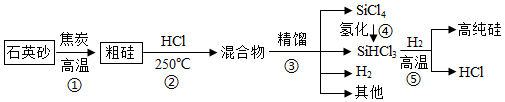
请回答:
(1)石英砂的主要成分是 。四氯化硅(SiCl4)中硅元素的化合价为 。
(2)“精馏”是蒸馏的一种,其原理是利用混合物各成分的 不同,将物质分离出来。
(3)上述流程中可循环使用的物质是 。
(4)流程⑤中发生反应的化学方程式为 。
某工厂废液中含有氯化钠、氯化铜和氯化亚铁。某课外小组要从废液中回收铜并得到铁红(主要成分Fe2O3),要求全过程不引入其他金属元素。设计实验方案如图所示:
请回答下列问题:
(1)工厂废液中加入过量A反应的化学方程式为 。
(2)用化学式表示固体甲的成分 。
(3)溶液甲中的金属离子是 (用离子符号表示)。
(4)完成步骤④的化学方程式:4Fe(OH)2+O2+2 ═4Fe(OH)3。
A﹣F为初中化学中常见的六种物质。其中E是一种碱,它广泛应用于制取肥皂,以及石油、造纸、纺织和印染等工业。它们之间的转化是初中常见的化学反应,转化关系如图所示(“→”表示一种物质可以转化为另一种物质,反应条件、部分反应物和生成物已略去)。请回答下列问题:
(1)E的化学式: ;
(2)C→F的反应属于 反应(填基本反应类型);
(3)写出F→E的化学方程式: ;
(4)A不可能的物质类别是: (填“单质”、“氧化物”、“酸”、“碱”、“盐”中的一种)。

电子工业上制造铜电路板,常用30%的FeCl3溶液腐蚀镀铜电路板上的铜箔(Cu),如图是某兴趣小组设计的处理该生产过程中产生废液的流程图,据如图回答下列问题:
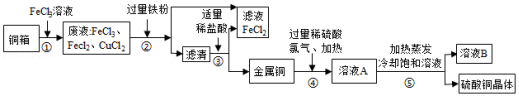
查阅资料:2Cu+2H2SO4+O2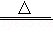 2CuSO4+2H2O;2FeCl3+Fe═3FeCl2
2CuSO4+2H2O;2FeCl3+Fe═3FeCl2
(1)步骤①所得的废液中只含有FeCl3、CuCl2、FeCl2三种溶质,据此可判断步骤①中铜与FeCl3反应生成的两种产物是 (写化学式)。
(2)步骤②中加入的铁粉与氯化铜发生反应的化学方程式是 ,步骤②还需要进行的实验操作是 。
(3)步骤③加入适量稀盐酸充分反应。当观察到 现象时,说明滤液中只剩下铜。
(4)步骤②③所得FeCl2可与一种气体单质发生化合反应生成FeCl3,实现循环使用,根据质量守恒定律可推测该单质是 。
(5)溶液B中含有的溶质是 。
钛和钛合金被认为是21世纪的重要金属材料,广泛应用于航天、医疗等领域。工业上以金红石(主要成分为TiO 2)为原料生产钛金属,流程如图1:

根据流程图信息,回答下列问题:
(1)钛在元素周期表中的信息如图2,钛原子的质子数是 。
(2)反应①的化学方程式为 。
(3)反应②的基本反应类型是 。
(4)反应②是在氩气环境下进行的,氩气的作用是 。
(5)航天飞机常用到钛合金,是因为钛合金具备很多优良性能,如 。(请你写出一点)。
海洋是一个巨大的资源宝库。海水资源综合利用的部分途径如图。
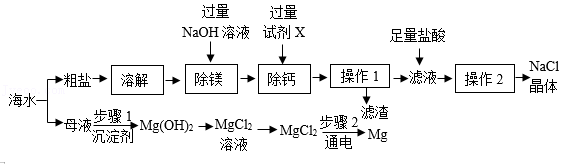
已知:粗盐中的杂质有泥沙、MgCl2、CaCl2,流程中部分操作及试剂已省略。
(1)试剂X的作用是除去粗盐中的Ca2+,则试剂X为 (填化学式)。
(2)“操作1”中玻璃棒的作用是 ,“操作2”的名称为 。
(3)滤渣中除泥沙外,还含有 。
(4)实际生产中,步骤1常选用 作为沉淀剂。
(5)步骤2需电解 状态的MgCl2以获得金属镁。
某兴趣小组利用废镍材料(含有金属Ni及少量Fe、Ag)探究相关物质的性质并回收镍,设计流程如图所示(部分产物略去)
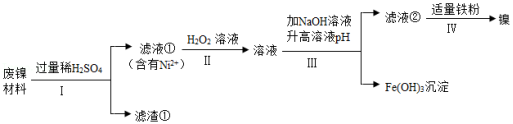
查阅资料:a.H 2O 2溶液可将Fe 2+转化为Fe 3+。
b.Fe 3+、Ni 2+转化为对应的氢氧化物沉淀时,溶液pH有如图关系:

(1)步骤Ⅰ的操作为 。
(2)滤渣①的成分为 。
(3)单质Fe参与反应的化学方程式为 (任写一个)。
(4)滤液②中有Ni 2+、无Fe 3+,则滤液②pH可能为 (填序号)。
A.pH=1
B.pH=2
C.pH=6
D.pH=10
(5)Ni、Fe、Ag三种金属的活动性由强到弱的顺序为 。
某工厂生产高锰酸钾的流程如图所示,请回答下列问题:
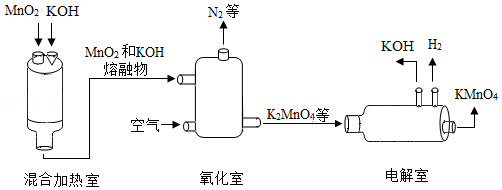
(1)“混合加热室”发生的主要是 (填“物理变化”或“化学变化”)。
(2)“电解室”反应中,反应前后化合价发生变化的元素有 (写元素符号)。
(3)生产流程中可循环利用的物质是 (写化学式)。
(4)写出氧化室中发生反应的化学方程式: 。
(5)取47.4g高锰酸钾,加热一段时间后停止,共收集到3.2g氧气,计算剩余固体中氧元素的质量分数是 (计算结果保留到0.1%)。
2021年6月8日是第13个“世界海洋日”。烟台有漫长的海岸线,蕴藏着丰富的海洋资源。某兴趣小组设计的综合利用海水的部分流程图如图。据如图回答:
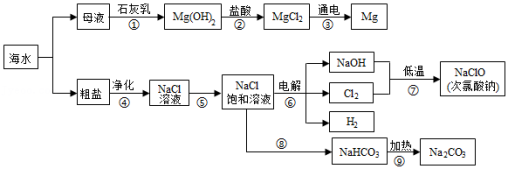
(1)海水制镁,步骤①②③是利用母液制镁的流程,该流程中发生中和反应的化学方程式是 。步骤①中制取氢氧化镁选择向母液中加入石灰乳,而不是向海水中直接加入石灰乳,原因是 。
(2)海水晒盐。通常采用 (填“降温”或“蒸发”)结晶的方法使海水中的氯化钠析出。通过步骤④除去粗盐溶液中含有的MgCl2、Na2SO4、CaCl2等可溶性杂质,需要依次加入过量的BaCl2溶液、过量的Na2CO3溶液、过量的NaOH溶液,然后过滤,在滤液中加入适量的稀盐酸。其中加入过量的Na2CO3溶液的目的是 。
(3)海水制碱。步骤⑧⑨是氨碱法制纯碱的流程,步骤⑧中需要向NaCl饱和溶液中先后加入的两种物质是 (写化学式)。步骤⑨中发生反应的化学方程式是 。
(4)步骤⑥是电解NaCl饱和溶液制取烧碱,该反应中的反应物是 。
(5)步骤⑦用烧碱低温制取次氯酸钠的反应原理为:Cl2+2NaOH═X+NaClO+H2O,则X的化学式是 。
蔗糖是储藏在某些植物中的糖,日常生活中食用的白糖、冰糖的主要成分就是蔗糖,它是食品中常用的甜味剂。工业制备蔗糖的流程如图所示。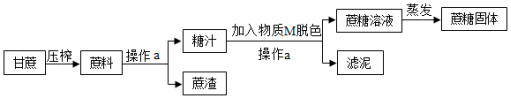
(1)操作a的名称是 。
(2)上述流程中物质M可能是 。
(3)在实验室进行蒸发操作时,要用到玻璃棒,其作用是 。
(4)蔗糖(C12H22O11)属于 (填“有机化合物”或“无机化合物”)。
试题篮
()