化学就在我们身边,人类的衣、食、住、行都离不开化学。
(1)杂交水稻之父袁隆平说“人就像一粒种子,要做一粒好的种子”、水稻种子的主要成分为淀粉,淀粉属于 营养物质。
A.蛋白质
B.糖类
C.油脂
D.维生素
(2)碱性甲烷燃料电池具有低污染、高效率等特点,是一种很有前途的能源利用方式。
①电池总反应方程式为CH4+2O2+2KOH═K2CO3+3X,则X的化学式为 。
②K2CO3属于 类化合物(填物质类别),其中碳元素化合价为 。
(3)4500L氧气可加压装入容积为30L钢瓶中,其原因是 (从微观角度解)。
(4)在农业生产中,改良酸性土壤(硫酸型酸雨所致),通常加入 ,以中和其酸性,反应的化学方程式为 ,该反应属于 (填基本反应类型)。
2009年,我国华为公司推出了5G商用芯片,制造芯片要用到高纯硅,如图为制备高纯硅和二氧化硅的主要工艺流程。

(1)反应①从基本反应类型角度分析,该反应属于 反应。
(2)反应②的化学方程式为 ,该工艺流程中可以循环利用的物质是 。
一种新型复合光催化剂(C3N4/CQDs),能利用太阳光分解水,原理如图所示。回答下列问题:

(1)这个过程将 能转化为化学能。反应Ⅱ属于基本反应类型中的 。
(2)写出反应Ⅰ的化学方程式: 。
阅读下面科普短文,并根据文章内容,回答相关问题。
铝(Al)是自然界中含量最多的金属元素,其主要存在于硅铝酸盐中。铝也是活泼金属,常温下在空气中铝的表面会形成致密的氧化膜,使铝不会进一步氧化并能耐腐蚀。因此,铝粉常用来做涂料,俗称银粉、银漆,以保护铁制品不被锈蚀,而且美观。
铝的密度很小,仅为2.7g/cm3,质地较软,可制成硬铝、超硬铝、防锈铝等各种铝合金。汽车、火车、船舶、宇宙火箭、航天飞机、人造卫星等,也是用大量的铝及其合金制造而成的。如一架超音速飞机约由70%的铝及其合金制成。
铝热法是以铝粉为还原剂的一种金属热还原法,当铝粉与金属氧化物起反应时,产生足够的热量,使生成的金属(或合金)和其他成分熔融分离而获得金属(或合金),广泛应用于生产纯金属、低碳铁合金,以及焊接金属(如铁轨)等。焊接铁轨时发生的化学反应为:2Al+Fe2O3 2Fe+Al2O3,该反应产生大量的热,温度可达2000℃以上。
2Fe+Al2O3,该反应产生大量的热,温度可达2000℃以上。
(1)“银粉”、“银漆”保护铁制品不被锈蚀的原因是是隔绝了 。
(2)铝合金制造超音速飞机是利用了铝合金 的性质。
(3)铝热法焊接铁轨时所发生的反应属于 (填基本反应类型)。
(4)高炉炼铁的主要原理同样是运用了热还原法,写出以赤铁矿为原料炼铁的化学方程式: 。
为解决能源与环境问题,有学者提出如图1所示的含碳物质转化的技术路线。
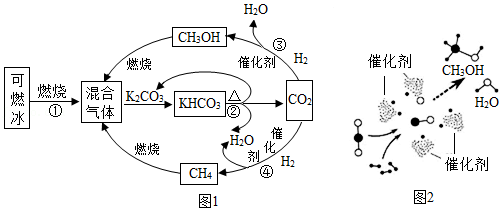
(1)“可燃冰”中甲烷完全燃烧的化学方程为 。
(2)反应②属于 (填基本类型)。
(3)反应④中,参加反应的CO2和生成的CH4的分子数目之比为 。
(4)我国学者开发促进反应③的一种新型催化剂,催化过程微观示意图如图2。该过程的中间产物 (填化学式)、氧和氢进一步作用生成甲醇(CH3OH)和水。
(5)该技术路线有利用于实现 (填标号)。
A.碳循环利用
B.减少碳排放
C.减少白色污染
金属在生产和生活中有着广泛应用。
(1)下列金属制品在应用中,利用金属导热性的是 。
a.金属硬币 b.铜制火锅 c.铝制导线
(2)铝比铁活泼,但铝在空气中比铁稳定,其原因是 。
(3)工业上用盐酸除去钢板表面上的锈要严格控制盐酸的用量,用量过多会发生反应而损坏钢板,用化学方程式表示损坏钢板的反应 。
(4)高铁的迅速发展对钢轨的需求量越来越大,质量要求越来越高。工业上经常用“铝热反应”来焊接钢轨,其原理是:  ,该反应的基本类型是 反应;若焊接钢轨需要50.4kg铁,理论上需要铝的质量是 kg。
,该反应的基本类型是 反应;若焊接钢轨需要50.4kg铁,理论上需要铝的质量是 kg。
置换反应是中学化学反应的基本反应类型之一.
已知:化合物A+单质B→化合物C+单质D.试回答下列问题.
(1)若D为氢气,A为稀硫酸,则B应满足的条件是 .
(2)若D为铜,化合物A的化学式可能为 .
(3)已知在高温条件下碳与水蒸气可反应生成一氧化碳和氢气(水煤气的主要成分),写出该反应的化学方程式 .若家中发生燃气(天然气)泄漏,下列措施不可行的是 (填字母序号).
A.检查并关闭气源阀门 B.轻轻打开门窗通风.C.立即打开抽油烟机排气
(4)非金属单质也具有类似金属与盐溶液之间发生置换反应的规律,即活动性较强的非金属可把活动性较弱的非金属从其盐溶液中置换出来,如在溶液中可发生下列反应:
Cl 2+2NaBr═2NaCl+Br 2、I 2+Na 2S═2NaI+S↓、Br 2+2KI═2KBr+I 2
由此判断S、Cl 2、I 2、Br 2四种单质中非金属活动性最强的是 ,最弱的是 .
(5)在化学反应中,物质所含元素的化合价发生变化的反应就是氧化还原反应,据此判断置换反应 (填"属于"或"不属于")氧化还原反应.
目前世界上60%的镁是从海水中提取的,综合利用海水制备镁的流程如图所示。
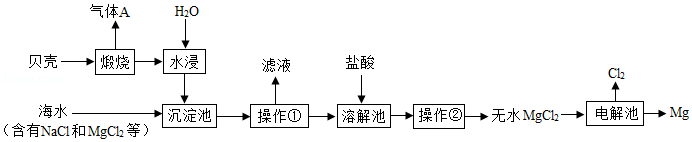
根据上述流程回答下列问题。
(1)气体A是 。操作①的名称是 。
(2)"水浸"过程中发生反应的化学方程式是 ;"沉淀池"中发生的主要反应的化学方程式是 。
(3)上述流程所发生的化学反应中,没有涉及的基本反应类型是 。
A﹣F是初中化学常见的6种物质,分别由C、H、O、S、Fe、Cu中的一种或几种元素组成。已知A、C是单质,B、C、D、E是不同类别的物质,E的固体俗称“干冰”,F是氧化物,F中两种元素的质量比为4:1.这些物质之间的相互关系如图所示,图中“﹣”表示能相互反应,“→”表示转化关系(部分反应物、生成物及反应条件已略去)。
(1)写出A、D的化学式:A ;D 。
(2)写出E的一种用途: 。
(3)写出D→E反应的基本反应类型: 反应。
(4)写出B﹣C、F→E反应的化学方程式:B﹣C: ;F→E: 。

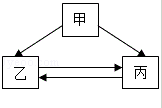
已知甲、乙、丙是初中化学常见的三种物质,且三种物质中均含有相同的某种元素。它们的转化关系如图所示("→"表示一种物质能转化为另一种物质,部分反应物、生成物及反应条件已略去)
(1)若乙、丙是组成元素相同的气体,且丙是有毒气体,则甲可能是 (填化学式),写出乙转化为丙的化学方程式 。
(2)若丙是相同条件下密度最小的气体,则乙是 (填化学式),甲转化成丙的基本反应类型是 。
化学科学的发展为人类创造了巨大的物质财富.我国涌现了许多化学家,他们的成就为世界所瞩目.侯德榜就是其中一位,他发明的联合制碱法,至今仍为世界各国所应用.联合制碱法的生产流程如图:
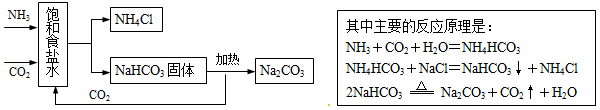
根据以上信息回答下面的问题:
(1)联合制碱法的原理中没有涉及的基本反应类型是什么?
(2)原料中的氯化钠在生活中的用途也很广泛,请你举出一例.
(3)侯德榜发明的联合制碱法有哪些优点(答出一点)?
质量守恒定律的发现,对化学的发展做出了重要贡献。

(1)通过分别称量下列两组试剂在密闭容器内混合前后的总质量,能验证质量守恒定律的是 (填标号)a.大理石和稀盐酸 b.NaOH溶液和Na 2SO 4溶液
(2)在足量氧气中点燃镁条的实验过程中,固体质量变化如图一。
①从燃烧条件分析,固体质量在t 1前没有发生变化的原因是
②该反应的化学方程式为
③参加反应的氧气质量为 g
(3)在一定条件下,A和B反应生成C,微观示意图如图二。回答下列问题:
①一个A分子由 个原子构成
②C分子中原子的质量比N:O=
③该反应的化学基本反应类型为
④上述反应中一定发生改变的是 (填标号)
a.元素种类 b.原子种类 c.分子种类
稀硫酸、硫酸铜溶液、氢氧化钠溶液、铁钉是常见的四种物质,物质之间的反应关系如图所示。图中两圆相交部分(Ⅰ、Ⅱ、Ⅲ、Ⅳ)表示物质间两两反应。
(1)Ⅰ处反应属于基本反应类型中的 反应。
(2)Ⅱ处反应现象是溶液由蓝色变成浅绿色,铁钉表面 。
(3)Ⅲ处两种溶液反应,滴入酚酞试液后溶液变红,说明此溶液呈 性。
Ⅳ处反应的化学方程式是: 。

以黄铁矿(主要成分为FeS 2)为原料生产硫酸的工艺流程如图所示:
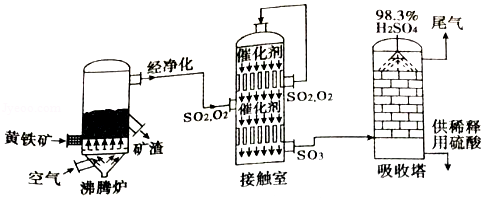
(1)沸腾炉中发生反应的化学方程式为:4FeS 2+11O 2 2X+8SO 2,其中X的化学式为 。
(2)接触室中发生反应的化学方程式为:2SO 2+O 2 2SO 3,产物SO 3中硫元素的化合价为 ;吸收塔中发生反应的化学方程式为:SO 3+H 2O═H 2SO 4,该反应的基本类型是 。若有800kg三氧化硫进入吸收塔中,且完全被吸收,则理论上制得硫酸的质量为 kg。
(3)O 2、SO 2、SO 3、H 2SO 4四种物质中属于氧化物的是 。
(4)实验室中稀释浓硫酸的操作是 。
试题篮
()