以下是甲、乙两同学对有关镁与盐酸反应的系列研究。
研究一:镁与盐酸反应过程中的能量变化以及反应速率的变化:
(1)反应中试管外壁发烫,说明镁与稀盐酸反应是 反应(填
“吸热”或“放热”)。
(2)实验测得镁片产生气体的速率(v)与时间(t)的关系如图所示,
则t1~t2时间内反应速率逐渐加快的主要原因是 。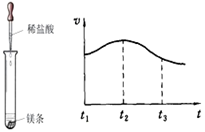
研究二:反应后所得溶液的酸碱性探究:
(3)甲同学反应后用pH试纸测定试管中溶液的酸碱性,发现pH小于7,说明甲同学所得溶
液呈 性(选填“酸”“碱”或“中”)。
甲同学:猜想Ⅰ:稀盐酸过量,使溶液pH小于7;猜想Ⅱ:氯化镁溶液pH小于7。为
验证猜想,甲同学需测定 溶液的酸碱性,实验表明该溶液显弱酸性。
(4)乙同学重复甲同学实验时,发现反应后所得试管中溶液pH大于7。发现实验与甲同学实
验不同的是,反应后的试管中镁条有剩余。乙同学猜想可能是镁与热水反应生成了碱性
物质。乙同学为验证猜想,在滴有两滴酚酞的热水中放入一段打磨过的镁条,观察到溶
液很快变为红色,同时还观察到镁条表面有气体生成,收集并点燃该气体,发现能燃烧,
请根据实验现象写出镁与水反应的化学反应方程式 。
(5)金属氯化物溶液pH值大小与金属的活动性有关,如氯化钠溶液显中性,氯化镁溶液显弱酸性,则氯化钾溶液显 性。
(6)活泼金属能与水在一定条件下反应。实验发现钠与冷水剧烈反应,产生大量的气体。由
此可见金属与水反应与金属的活动性顺序 (填“有关”或“无关”)。
研究三:金属活动性强弱与原子结构的关系:
下图为镁原子、钙原子和钡原子结构示意图。已知其中Ba的活动性最强,据此推测,金属的活动性除与原子的最外层电子数有关,还与 有关。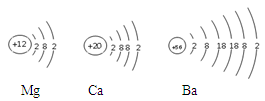
研究四:确定镁条的成分:
称取3.2g表面被氧化的镁条, 放入100g稀盐酸中恰好完全反应,生成气体0.2g。求:
(7)此镁条中金属镁的质量。(写出计算过程,共3分)
(8)反应后所得溶液中溶质的质量分数 。(计算结果保留一位小数)
如图所示为各物质之间的转换关系,请回答下列问题:
(1)写出下列字母所代表物质的化学式:A: D: E: ;G: 。
(2)写出过程①、②的化学方程式① ;
② ,其基本反应类型是 .
构建知识网络是一种重要的学习方法。下图是关于X物质化学性质的知识网络,“——”表示相连的两种物质能发生反应,“ ”表示一种物质转化成另一种物质,X的水溶液遇硝酸钡溶液产生不溶于硝酸的白色沉淀,D是生活中常见金属,与X反应产生气泡,溶液变浅绿色,A、B、C、D属于不同类别的物质。完善这个知识网络:
”表示一种物质转化成另一种物质,X的水溶液遇硝酸钡溶液产生不溶于硝酸的白色沉淀,D是生活中常见金属,与X反应产生气泡,溶液变浅绿色,A、B、C、D属于不同类别的物质。完善这个知识网络: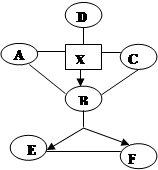
(1) 写出A、B的化学式: A ;B 。
(2) 根据自己得出的知识网络写出一个复分解反应
化学方程式:
(3)写出E与F反应的反应化学方程式:
____________________________________
某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动。以下是教学片段,请你参与学习并帮助填写空格(包括表中空格)。
【演示实验】将一定量的稀硫酸加入到盛有NaOH溶液的小烧杯中。
【学生板演】该反应的化学方程式______________。
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
【假设猜想】针对疑问,大家纷纷提出猜想。甲组同学的猜想如下:
猜想一:只有Na2SO4
猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH
猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的。不合理的猜想是
____________________。
【实验探究】(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有____________。
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaCl2溶液、Na2CO3溶液,进行如下三个方案的探究。
| 实验方案 |
测溶液pH |
滴加Na2CO3溶液 |
滴加BaCl2溶液 |
| 实验操作 |
 |
 |
 |
| 实验现象 |
试纸变色,对比比色卡,pH<7 |
|
产生白色沉淀 |
| 实验结论 |
溶液中有H2SO4 |
溶液中有H2SO4 |
溶液中有H2SO4 |
【得出结论】通过探究,全班同学一致确定猜想二是正确的。
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定。同时指出【实验探究】(2)中存在两处明显错误,请大家反思。同学们经过反思发现了这两处错误:
(1)实验操作中的错误是____________________。
(2)实验方案中也有一个是错误的,错误的原因是_____________________。
(14分)水在实验室和日常生活中有很多用途。
I、溶液是日常生活中的常见物质,水是最常用的溶剂。
20℃时,将等质量的甲、乙两种固体物质,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图2,甲、乙两种物质的溶解度曲线如图3。请结合图示回答下列问题: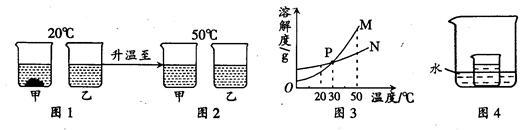
(1)图1中一定为饱和溶液的是
(2)图3中表示乙的溶解度曲线是 ;P点表示的含义是 。
(3)在图4所示的实验中,小烧杯内盛放的是20℃时甲物质的饱和溶液。某同学要使小烧杯内有固体析出时,他应向大烧杯的水中加入下列物质中的 (填字母)。
A.氧化钙 B.氯化钠 C.氢氧化钠 D.硝酸铵
Ⅱ、水在工业生产中也很重要。
以电解食盐水为基础制取氯气等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一。电解饱和食盐水可以得到多种化工产品,主要过程如下: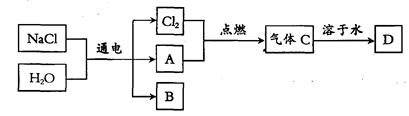
[资料卡:石灰水中的溶质是一种碱——Ca(OH)2]
(4)已知气体A是密度最小的气体,B是一种碱,D是一种酸。写出金属铝和酸D反应生成气体A的化学方程式: 。
(5)B的化学式为 。
(6)工业上电解食盐水是在立式隔膜电解槽中进行,产生的Cl2和气体A在两处逸出并分别收集、储存。
①已知20℃,S(NaCl)=36g,则室温下,68 kg饱和食盐水中溶质的质量为 。
②电解一段时间,当收集到氯气的质量为0.71 kg时,列式计算生成的B的质量 。
③0.71 kg氯气和A完全反应生成气体C,溶于一定量的水中形成酸D。若酸D中的溶质质量分数为36.5%,则其中水的质量为 。
某研究性学习小组学习了工业“侯氏制碱法”的原理后,知道如下反应:
NaCl + NH3 + CO2 + H2O = NaHCO3↓+ NH4Cl 。
【提出问题】能否在实验室模拟“侯氏制碱法”制取NaHCO3的过程呢?
【实验验证】如下图是该学习小组进行模拟实验时所用到的部分主要装置和药品。
请回答下列问题:
⑴ 检验A装置气密性的方法是:塞紧带长颈漏斗的橡胶塞,夹紧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于试管内的水面,停止加水后,若 ,说明装置不漏气。
⑵该实验中用B装置制取的气体是 (填化学式),B装置中盛装浓氨水的仪器名称为 ,本实验中使用该仪器的优点是 。
⑶D是连接在装置A与装置C之间的气体净化装置,进气口是 (填a或b),D的作用是除去HCl气体,反应的化学方程式为 。
⑷实验时先向饱和NaCl溶液中通入较多的NH3(溶液显碱性),再通入足量的CO2,其原因是 (填写序号)。
① 使CO2更易被吸收 ② NH3比CO2更易制取 ③ CO2的密度比NH3大
⑸用 的方法将生成的NaHCO3晶体从混合物中分离出来。
【得出结论】利用“侯氏制碱法”在实验室可以制取NaHCO3 。
A、B、C、D、E、F、G表示的是7种初中化学常见的物质,7种物质均由H、C、O、Na、Cl中的一种或几种元素组成。
(1)常温下A、B为液体,A在一定条件下分解生成B和单质C。该反应的化学方程
为_____。C的一种主要用途是________。
(2)D和E均含有三种元素,且D中各原子个数比为1∶1∶1,G溶液分别与D、E、F溶液反应均可生成B和氯化钠。
① F属于_____(填 “酸”、“碱”、“盐”或“氧化物”)。
② D与G反应的化学方程式为_____,此反应属于基本反应类型中的_____反应。
③ 一定量的E与G充分反应后得到无色溶液,向其中加入足量的F溶液,无明显
现象。由此推断,原无色溶液中的溶质是(写出所有可能)________。
已知A、B、C、D四种物质是初中化学常见的不同类别物质。A为可溶性的碱,A、B、C中均含三种元素,反应①有两种沉淀生成。(“—— ”表示两种物质间能发生化学反应。)
(1) ①的方程式为 ,
(2) ①②③④四个反应中属于置换反应的有 .
某NaCI样品在生产过程中可能含有残余的MgCl2、CaCl2和Na2S04三种物质中的一种或几种,现按下图所示进行检验,出现的现象如图中所述。

试根据实验过程和发生的现象,回答下列问题:
(1)沉淀A是(写化学式)
(2)实验步骤①的现象可以说明混进的物质有(写化学式)
(3)实验证明,溶液B中一定存在的溶质是(写化学式) 。
(4)实验过程③中发生反应的化学方程式为 ____
(5)上述实验现象还不能确认CaCl2是否残留在了NaCl样品中,请你利用溶液D进行实验确认判断:(说明选用试剂、现象和结论)__ __
下列图像与所对应操作相符的是.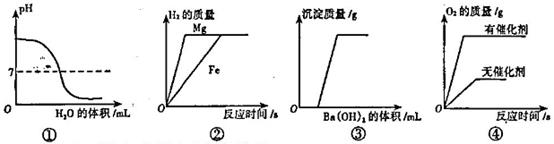
| A.①是对氢氧化钠溶液加水稀释 |
| B.②是将镁片和铁片(均足量)分别和等质量、等溶质质量分数的稀硫酸混合 |
| C.③是向HCI与Na2 SO4泥合溶液中加入Ba (OH)2溶液 |
| D.④是用等质量、等浓度的双氧水分别制取氧气 |
(6分)如图以稀盐酸为例的反应关系体现了酸的化学性质,其中X与图中所给物质的类别不同.结合此图回答下列问题:
(1)Ca(OH)2的俗名是__________________(填一种即可);
(2)反应②为__________(填“放热”或“吸热”)反应;
(3)反应⑤的化学方程式为 ;此反应属 于___________(填基本反应类型);
(4)图中只生成盐和水的反应有 (填序号);
(5)若X溶液既能跟稀盐酸反应,又能跟Ca(OH)2反应,则X可能是(BaCl2、CuSO4、K2CO3)中的 。
现有木炭、二氧化碳、氧化铜、石灰水、稀硫酸和碳酸钾溶液六种物质。如图,
已知硫酸的位置,请回答下列问题:
(1)请将另外五种物质的化学式填入圆内,使每个圆内的物质都能与其相连的圆内的物质反应;
(2)写出有木炭参加反应的化学方程式 ;
(3)过量A与稀硫酸反应的实验现象为 。
请根据图示回答问题:

(1)当适量的液体A和气体B是下列哪种组合时,打开
弹簧夹试管中的水会重新沸腾 ;
| A.水和氧气 | B.氢氧化钠溶液和二氧化硫 |
| C.酒精和氮气 | D.氯化钙溶液和一氧化碳 |
(2)请用理化知识解释试管中的水重新沸腾的原因
试题篮
()