下列图像能正确反映其对应实验过程及结果的是 
A B C D
| A.用等质量、等浓度的过氧化氢(H2O2)溶液分别制取氧气 |
| B.在t℃时,向一定量的氯化钠饱和溶液中加入氯化钠固体 |
| C.足量盐酸与一定量的大理石反应生成二氧化碳气体 |
| D.过量锌粉加入到一定量的稀硫酸中 |
某学生做了如下图所示的实验。
| |
第一次 |
第二次 |
| 加入氧化铜的质量 |
m |
m |
| 加入稀硫酸的质量 |
50g |
100g |
| 加入铁粉的质量 |
5.6g |
5.6g |
| 实验现象 |
黑色固体和紫红色固体 |
紫红色固体 |
若第二次所加物质恰好完全反应(滤液损失忽略不计),请回答下列问题:
(1)写出实验中发生反应的化学方程式
(2)第一次实验后的固体物质的化学式为
(3)根据已知条件列出求解第二次实验生成固体物质的质量(x)的比例式
(4)实验中加入氧化铜的质量(m)为 ;
(5)若向第二次反应后的滤液中加入92.8g水,则所得不饱和溶液中溶质的质量分数为 ;
(6)若用溶质质量分数为49%的硫酸溶液配制实验中所需的稀硫酸,则需要加水的质量
为 。
某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁。他们为了测定水垢中碳酸钙的含量,将足量的盐酸加入到10g水垢中,产生CO2气体的情况如图所示。
(1)从图中可以看出,10g水垢反应后生成的二氧化碳最多是 g。
(2)水垢中的碳酸钙质量分数是多少?
为了测定未知浓度稀硫酸的溶质质量分数,取氢氧化钡溶液15g,逐滴加入该待测稀硫酸,同时测定并记录反应过程中混合溶液的pH变化情况(如图所示),过滤后得到滤液32.67g.
求:(1)反应后生成硫酸钡的质量是多少;
(2)该稀硫酸的溶质质量分数。
某化学实验小组要检测黄铜(铜、锌合金)中金属铜的纯度,同学们取20 g黄铜样品,向其中分三次共加入15 g盐酸溶液,充分反应后测得实验结果如下: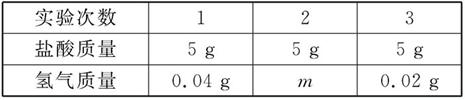
请计算:(1)第2次实验产生氢气的质量m= g。
(2)黄铜(铜、锌合金)中金属铜的纯度。
(3)该盐酸溶液中溶质的质量分数。
过氧化氢溶液长期保存会自然分解,使溶液的溶质质量分数减小。小军从家中拿来一瓶久置的医用过氧化氢溶液,和同学们一起测定其溶质质量分数,他们取该溶液51 g,加入适量二氧化锰,生成氧气的质量与反应时间的关系如图所示。则:
(1)完全反应后生成氧气的质量为 。
(2)计算该过氧化氢溶液中溶质的质量分数。
质量相同的下列金属,分别加入到足量的稀硫酸中充分反应,放出氢气最多的是 ( )
| A.Na | B.Al | C.Cu | D.Zn |
等质量的三种金属A、B、C和相同质量分数的足量稀硫酸反应, 都生成+2价金属硫酸盐,其反应情况如图所示。依图可知三种金属的活动性顺序是 ,它的相对原子质量大小的顺序是 。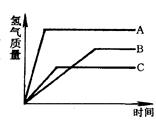
将铜和碳酸钙的混合物在空气中充分灼烧,混合物的质量在冷却后没有变化,则原混合物中铜和碳酸钙的质量比为( )
| A.44:25 | B.25:44 | C.1: 1 | D.无法确定 |
有①Cu-Zn ②Cu-Ag 两种貌似黄金的合金,它们都有其特殊的用途,但一些骗子常用它们做成饰品冒充真黄金欺骗消费者。对此,化学科学有责任加以揭露。
(1)现有上述两种合金制成的假黄金饰品各一件,小明同学只用稀盐酸和必要的实验仪器就鉴别出其中一种饰品是假黄金,它是合金 (填写代号);若要证明另一种饰品也是假黄金,可选用一种盐溶液来验证,这种盐可以是
(写一种盐的名称或化学式);
(2) 取与上述用稀盐酸鉴别出的同种合金10g,放入烧杯中,再向其中加入93.7g某稀盐酸恰好完全反应后,测得烧杯内剩余物质的质量共为103.5g。
①上述过程中变化的质量10g+ 93.7g -103.5g=0.2g是 (填物质的名称或化学式)的质量;
② 10 g,该合金中铜的质量是多少?
我国早在春秋战国时期,就开始生产和使用铁器。某化学小组到钢铁厂做社会调查,将不同质量的生铁样品(假定其中只含铁和碳两种单质)分别放入5只烧杯中,各加入189.2 g质量分数相同的稀硫酸进行实验,实验数据见下表:
| |
烧杯① |
烧杯② |
烧杯③ |
烧杯④ |
烧杯⑤ |
| 加入生铁样品 的质量/g |
3.0 |
6.0 |
9.0 |
12.4 |
14.0 |
| 充分反应后 生成气体 的质量/g |
0.1 |
M |
0.3 |
0.4 |
0.4 |
试计算:
(1)表中M的值为________。
(2)烧杯④中完全反应后,所得溶液中溶质的质量是多少?(写出计算过程)
如图是实验室新采购的一批碳酸钠药品的标签。小明取13.25 g这种碳酸钠药品与盐酸反应,化学方程式为:2HCl + Na2CO3=" 2NaCl" + CO2 ↑+ H2O
用含HCl 7.3 g 的盐酸与它恰好完全反应。计算:
(1)13.25g 样品中Na2CO3的质量是多少?
(2)通过计算判断样品Na2CO3的含量是否符合标签要求。
根据如图所示信息计算:
(1)加入的稀硫酸质量为 g。
(2)所用稀硫酸溶质的质量分数。(化学方程式:2KOH+H2SO4=K2SO4+2H2O)
某合金6 g与足量的稀硫酸充分反应后,如果生成0.2 g氢气,该合金中的元素可能是( )
| A.Zn和Fe | B.Cu和Au |
| C.Zn和Cu | D.Mg和Al |
试题篮
()