如右图所示进行实验: .已知集气瓶的容积为 .氧气的密度为 ,为了节约药品.理论上所取硫的质量不能超过多少克 (计算结果保留两位小数)

已知用赤铁矿石冶炼铁的化学方程式为
请计算:(相信你一定能行!)
(1)
的相对分子质量为;
(2)现有2000吨含氧化铁80%的赤铁矿石,其中含氧化铁吨;
(3)用此2000吨含氧化铁80%的赤铁矿石,理论上可以炼出纯铁多少吨?(要求有计算步骤)
实验室常用石灰石与稀盐酸制取
,某同学设计了两种制取
的部分装置(见右图).

(1)实验室制取
的化学方程式为:·
(2)仪器A的名称是: ,
(3)图1装置的不规范之处是: ;
(4)用图2装置
时,要使反应停止,最简便的操作方法是: ;
(5)实验时,向盛有石灰石的试管中加入足量稀盐酸后,发现石灰石表面仅有极少量气泡产生,原因可能是;
(6)若实验室需制备2.2 L
;.理论上需纯度为80﹪的石灰石多少克,(假设该状态下
的密度为2克/L)。
和
可发生如下反应:
,某学生做了3次该实验(每次均充分反应),反应前
和
的质量和都是l0克.有关实验数据见右表,
的比值可能为
| 序号 |
反应前 的质量 |
反应前 的质量 |
反应后 的质量 |
| ① |
10 |
2 |
6 |
| ② |
4 |
8 |
6 |
| ③ |
|
|
9 |
| A. |
|
B. |
|
C. |
|
D. |
|
某同学为了测定一瓶过氧化氢溶液中溶质的质量分数,取该溶液20g,加入二氧化锰0.5g,完全反应后,称得烧杯内剩余物质的总质量为19.7g。请回答下列问题:
(1)上述过程中生成氧气质量是。
(2)计算该过氧化氢溶液中溶质的质量分数。
用“侯氏联合制碱法”制得的纯碱常含有少量的氯化钠。为测定某纯碱样品中碳酸钠的含量,小明称取该纯碱样品12.4g,向其中逐渐滴加溶质质分数为10%的稀盐酸。放出气体的总质量与所滴入稀盐酸的质量关系曲线如下图所示,请根据题意回答问题:
(1)当滴加稀盐酸至图中B点时,烧杯中溶液的pH 7(填>、=、<)。
(2)从坐标上C点的数值为 g。
(3)求该纯碱样品中碳酸钠的质量分数。(计算结果保留一位小数)
将104g由氯化钠和氯化钡
组成的固体混合物溶解于足量水中,向所得溶液中滴加10.6%的碳酸钠溶液,所加碳酸钠溶液的质量与生成沉淀质量关系见右图
①图中表示恰好完全反应的点是,此时溶液中的溶质为。(写化学式)
②求生成沉淀的质量。
③求原混合物中氯化钠的质量分数。
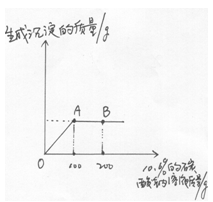
将一定质量的碳酸钠粉末溶于
克水中配制成溶液,取一半该溶液,向其中加入
的盐酸若干克,恰好反应完全,放出气体的质量为
克。试计算:
(1)碳酸钠溶液的总质量;
(2)反应后所得溶液中溶质的质量分数。
在实验室中制取88克二氧化碳,需要多少克碳酸钙跟适量盐酸反应?若改用含杂质20%的石灰石与盐酸反应(杂质不与盐酸 反应),需要这种石灰石多少克?
反应),需要这种石灰石多少克?
氢氧化钠潮解后极易与二氧化碳反应而变质。为测定实验室里一瓶放置已久的烧碱中氢氧化钠的质量分数,某同学取5.3g烧碱样品放在小烧杯中,然后加入20g稀硫酸,恰好完全反应,反应后所得溶液的质量为24.86g。计算该烧碱样品中氢氧化钠的质量分数。
某石灰厂有一批石灰石原料,为了测定该石灰石的纯度,厂化验室技术员称取6.25g研碎的石灰石粉末,进行四次高温煅烧(杂质没有变化)、冷却、称量剩余固体质量的重复操作,记录数据如下:(提示:碳酸钙在高温下分解,生成氧化钙和二氧化碳气体)
| 操作次序 |
第一次 |
第二次 |
第三次 |
第四次 |
| 剩余固体质量 |
5.55g |
4.35g |
4.05g |
4.05g |
试计算:
(1)完全反应后生成二氧化碳;
(2)石灰石样品中碳酸钙的质量分数。
在反应 中, 的相对分子质量之比为9 : 22。若2.6 与 完全反应后,生成 。则在此反应中, 的质量比为 ()
| A. |
4 : 9 |
| B. |
8 : 11 |
| C. |
10 : 11 |
| D. |
31 : 44 |
试题篮
()