实验室常用溶质质量分数为10%的过氧化氢溶液制取氧气。
(1)某兴趣小组打算用如图所示的整瓶溶液配制溶质质量分数为10%的过氧化氢溶液,需加水 g。
(2)在配制过程中,他们发现试剂瓶内壁附着不少气泡,由此推断该瓶过氧化氢溶液的溶质质量分数小于30%,依据是 。
(3)为测定该瓶溶液的溶质质量分数,他们取35g该溶液放入锥形瓶中并加入一定量的二氧化锰。不同时间电子秤的读数如下表所示(不考虑H2O逸出):
反应时间/min |
0 |
1 |
2 |
3 |
4 |
5 |
6 |
锥形瓶+瓶内物质的总质量/g |
340.00 |
338.78 |
335.64 |
335.28 |
335.20 |
335.20 |
335.20 |
请回答:
①反应生成氧气的总质量为 g。
②该瓶过氧化氢溶液的溶质质量分数是多少?(写出计算过程,结果保留到0.1%)

小宁用稀盐酸和石灰石反应制取二氧化碳(石灰石中的杂质既不溶于水也不和酸反应),为了探究反应后溶液的成分,他又进行如下实验:取反应后的溶液50g于烧杯中,逐滴滴入碳酸钠溶液,发现先有气泡产生,后生成白色沉淀。下表为产生的气体总质量、沉淀总质量与滴入碳酸钠溶液总质量的关系。
碳酸钠溶液总质量/g |
25.0 |
50.0 |
75.0 |
100.0 |
125.0 |
150.0 |
175.0 |
200.0 |
气体总质量/g |
1.1 |
2.2 |
2.2 |
2.2 |
2.2 |
2.2 |
2.2 |
2.2 |
沉淀总质量/g |
0 |
0 |
2.5 |
5.0 |
m |
n |
9.0 |
9.0 |
(1)表中n= 。
(2)所取的反应后50g溶液中溶质是 。
(3)所用碳酸钠溶液中溶质的质量分数是多少?
某同学取110g K2CO3溶液于烧杯中,向其中加入CaCl2溶液。反应过程中加入CaCl2溶液与生成沉淀的质量关系如图所示。
请计算:
(1)m的值是 。
(2)恰好完全反应时,所得溶液的溶质质量分数是多少?(写出计算过程,结果精确到0.01%)

某石灰水中含有氢氧化钙1.48g,要使该石灰水中的氢氧化钙转化为碳酸钙沉淀,至少需要二氧化碳的质量是多少?
某品牌补钙剂的主要成分是碳酸钙,实验小组的同学取该补钙剂2.5g,加入溶质质量分数为7.3%的稀盐酸至不再有气泡产生,共收集到二氧化碳0.88g(补钙剂中其他成分均不与稀盐酸反应)。请计算。
(1)该补钙剂中碳酸钙的质量分数。
(2)所用稀盐酸的质量。
小嘉发现:向碳酸钠溶液中倾倒稀盐酸,很快就产生了气泡:向碳酸钠溶液中逐滴加入稀盐酸,滴加一定量后才有气泡产生。查阅资料:向碳酸钠溶液中逐滴加入稀盐酸,先发生的反应是Na2CO3+HCl═NaCl+NaHCO3;当Na2CO3全部转化成NaHCO3后,再发生反应NaHCO3+HCl═NaCl+H2O+CO2↑。为此他用如图所示装置进行了如下实验:
步骤一:在广口瓶中加入10克溶质质量分数为10.6%的碳酸钠溶液,用注射器向瓶中缓慢注入一定量的溶质质量分数为7.3%的稀盐酸,观察到瓶内无明显现象; 步骤二:继续用注射器向瓶中注入稀盐酸,一段时间后观察到瓶内连续产生气泡,烧杯中澄清石灰水?。 |
(1)步骤二中,观察到烧杯中澄清石灰水 。
(2)上述实验中,加入稀盐酸多少克后,才开始产生二氧化碳? 。
(3)向一定量碳酸钠溶液中无论是倾倒还是逐滴加入足量的稀盐酸,完全反应后产生二氧化碳质量是相同的,其本质原因是什么? 。

以某菱镁矿石(主要成分是MgCO3,含少量MnCO3、SiO2)制取MgSO4•7H2O,流程如图:

(1)“酸浸”时,为了提高浸取率,除了搅拌、提高硫酸浓度外,还可采取的措施有
(写出一种)。此时,MnCO3发生反应的化学方程式是 。
(2)“转化”时主要反应是NaClO+MnSO4+H2O═MnO2↓+NaCl+H2SO4,氯元素反应前后化合价变化情况是 (填“升高”或“降低”)。
(3)硫酸镁溶液在不同温度下进行浓缩结晶,可得到不同的晶体:
温度/℃ |
﹣3.9~1.8 |
1.8~48.1 |
48.1~67.5 |
67.5~200 |
析出晶体 |
MgSO4•12H2O |
MgSO4•7H2O |
MgSO4•6H2O |
MgSO4•H2O等 |
①“操作1”的具体操作是:蒸发浓缩滤液至表面有晶膜出现(此时MgSO4溶液已饱和)、 、过滤、洗涤、低温干燥。
②“操作1”所得滤液中能分离出一种可循环使用的物质,该物质是 H2SO4 (填化学式)。循环使用的目的是 。
(4)已知:MgSO4•7H2O中镁元素质量分数为9.76%。采用热分析法测定所得MgSO4•7H2O样品中镁元素质量分数:
①未加热前,测得样品中镁元素质量分数略大于9.76%,可能的原因是 。
②高于900℃后,测得剩余固体中镁元素质量分数大于20%,可能的原因是 。
(5)若用100t菱镁矿石可制得246t MgSO4•7H2O产品,忽略反应过程中镁元素损失,求该菱镁矿石中MgCO3的质量分数。(写出计算过程)
已知一包铁粉中含有两种杂质,小明同学取5.6g该粉末,向其中加入足量的稀硫酸,充分反应后,得到0.5g氢气。则该样品中的杂质可能是( )
A.Mg和ZnB.Al和ZnC.Zn和CuD.Mg和Cu
化学是一门以实验为基础的科学,实验是科学探究的重要手段。
(1)完成“探究某种盐的性质”实验,填写下表。
试管序号 |
甲 |
乙 |
丙 |
实验操作 |
|
|
|
实验现象 |
红色溶液 |
白色沉淀 |
无色气体 |
实验结论 |
该盐是 (选填“NaCl”“Na2CO3”“Na2SO4”),其水溶液呈 性。 |
||
实验解释 |
丙中发生反应的化学方程式: 。 |
||
实验计算 |
全班同学完成试管乙实验,共消耗质量分数为10.4%的BaCl2溶液50g,实验后最多收集到 g白色沉淀。 |
||
(2)处理“CO2的实验室制取与检验”实验废液。全班同学完成该实验共产生1000g含HCl废液(固体已除,大理石中杂质未参加反应),不能直接排放。
【实验方案】先测定废液中HCl的质量分数,再用熟石灰处理废液至中性。
【实验操作】
①称量 g NaOH固体,溶解,配制30g 5%的NaOH溶液。
②取100mL小烧杯,倒入20g废液样品,插入pH计测定溶液的pH,向废液样品中逐滴加入5%的NaOH溶液。实验过程中溶液pH变化如图所示。
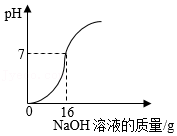
③投入 g熟石灰处理剩余废液(写出计算过程)。
【实验反思】有同学提出也可以根据盐酸具有挥发性直接加热废液除去杂质HCl,并得到CaCl2。写出你的观点及理由: 。
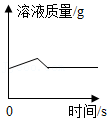
(1)将一定量的锌和金属R的混合粉末加入一定量的氯化铜溶液中,溶液质量的变化情况如图所示。下列说法错误的是 (填标号)。
A.金属活动性Zn>R
B.反应结束后过滤、滤渣中一定有Cu,可能有Zn和R
C.反应结束后过滤,若向滤渣中加入稀硫酸有气泡产生,则滤液一定无色
(2)某金属粉末含有Mg、Al、Cu、Ag中的一种或几种,取24g该金属粉末与足量稀盐酸反应产生2g氢气,则该金属粉末的组成有 种情况。
某化学兴趣小组欲测定某石灰石样品中碳酸钙的质量分数,先将10g样品放入烧杯中,再把100g稀盐酸分5次加入该样品中(该实验条件下,杂质不与酸反应,也不溶解于水,忽略稀盐酸挥发),得实验数据如表格。
稀盐酸的质量 |
充分反应后剩固体的质量 |
第一次加入20g |
8g |
第二次加入20g |
6g |
第三次加入20g |
4g |
第四次加入20g |
2g |
第五次加入20g |
2g |
请计算;
(1)10g石灰石样品中碳酸钙的质量分数是 。
(2)求稀盐酸的溶质质量分数(写出计算过程,结果精确到0.1%)。
孔雀石的主要成分是Cu2(OH)2CO3,还含有Fe2O3、Al2O3、SiO2杂质,用该矿石制备Cu的流程如图所示(部分产物略去):
 (1)过程①中,操作a是溶解和 ,还有一种气体产物是 ,滤液X中含有的金属阳离子为 。
(1)过程①中,操作a是溶解和 ,还有一种气体产物是 ,滤液X中含有的金属阳离子为 。
(2)过程①中硫酸略过量,则过程②调pH除杂的最佳试剂是 (选填“CuO”或“Na2CO3”)。
(3)下列关于制取铜的两种方案的说法,正确的是 。
A.“方案一”得到的铜产品更纯
B.“方案一”不存在消耗能量的问题
C.“方案二”需考虑废气污染的问题
D.“方案二”得到纯铜的产率更高
(4)过程③发生的反应:2CuSO4+2H2O 2Cu+O2↑+ (补充完方程式),当收集到800t氧气时,产生Cu的质量是多少?(写出必要的计算过程)
2Cu+O2↑+ (补充完方程式),当收集到800t氧气时,产生Cu的质量是多少?(写出必要的计算过程)
烧杯中盛有锌粉和铁粉的混合物mg,向其中逐渐加入一定浓度的稀盐酸,测得剩余固体的质量与加入稀盐酸的体积的关系如图所示。下列有关结论正确的是( )
①加入V1mL稀盐酸时,剩余固体中不含锌
②加入V2mL稀盐酸时,溶液中的溶质为FeCl3和ZnCl2
③整个过程中发生反应均为置换反应
④反应中产生氢气的质量一定小于 g
g
⑤剩余固体质量m、n与稀盐酸的体积V1、V2的数量关系为 =
=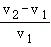

A.①②③④B.①③④C.①③⑤D.①③④⑤
钙是生物体骨骼的重要组成元素。鱼骨中含有碳酸钙,现设计图甲实验测定鱼骨中的碳酸钙含量,并将测得的数据绘制成图乙。

提示①食醋的主要成分是醋酸(HAc)。醋酸和碳酸钙反应的化学方程式为CaCO3+2HAc═CaAc2+H2O+CO2
②鱼骨中其它成分与食醋反应生成的气体可忽略不计
(1)该实验中浓硫酸的作用是 。
(2)由图乙中的AB曲线,可知锥形瓶中反应速率的变化情况是 (选填“变大”、“变小”或“不变)。
(3)根据图中的数据计算鱼骨中碳酸钙的质量分数。
(4)生活中,用喝醋的方法除去卡在咽上的鱼刺,这种做法是不科学的。请你结合实验结果加以说明 。
用沉淀法可测定食用碱样品中碳酸钠的质量分数。取11g食用碱样品(有少量的杂质氯化钠),加水完全溶解制成100g溶液,逐次滴加溶质质量分数相同的氯化钙溶液,实验数据如表:
实验次数 |
第1次 |
第2次 |
第3次 |
第4次 |
第5次 |
第6次 |
加入CaCl2溶液的质量/g |
20.0 |
20.0 |
20.0 |
20.0 |
20.0 |
20.0 |
反应后溶液的总质量/g |
118.0 |
136.0 |
154.0 |
M |
191.0 |
211.0 |
请根据实验数据分析解答下列问题:
(1)表中数据M的值为 。
(2)请画出生成沉淀的质量随滴加氯化钙溶液质量的变化关系图(标明恰好反应时点的坐标)。
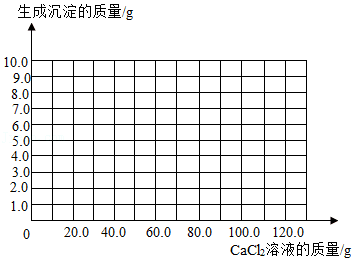
(3)计算该食用碱样品中碳酸钠的质量分数(写出过程,结果保留到0.1%)。
试题篮
()