小明同学为探究“Na2CO3溶液与稀盐酸反应是放热反应还是吸热反应”,设计并进行了3次重复实验,结果如下表:
| 试剂1 |
试剂2 |
混合前温度/℃ |
混合后温度/℃ |
|
| 35毫升稀盐酸 |
25毫升Na2CO3溶液 |
20.0 |
第1次 |
24.2 |
| |
|
|
第2次 |
24.0 |
| 第3次 |
24.4 |
请你帮助填写相关内容:
(1)写出该实验涉及的化学反应方程式 ;
(2)该实验中所用的仪器除烧杯、量筒、玻璃棒、保温瓶外,还必须用到的一种仪器是:
(3)由上表数据可知:Na2CO3溶液与稀盐酸的反应是 (选填:“放热“或“吸热“)
下列离子能在pH=1的无色溶液中大量共存的是
| A.Cu2+、SO42﹣、Cl﹣、Na+ | B.OH﹣、K+、NO3﹣、Ba2+ |
| C.Mg2+、SO42﹣、Al3+、NO3﹣ | D.Na+、CO32﹣、Ca2+、Cl﹣ |
下列有关实验现象的描述中正确的是
| A.红磷在空气中燃烧产生大量白色烟雾 |
| B.木炭在空气中剧烈燃烧,发出白光 |
| C.氢氧化钠溶液滴入硫酸铜溶液中,产生蓝色絮状沉淀 |
| D.碱式碳酸铜粉末与稀盐酸反应,产生大量气泡,绿色溶液变成蓝色 |
已知NH3和HCl发生反应:NH3+HCl=NH4Cl,下图所示实验的叙述中错误的是
| A.浓盐酸和浓氨水都有挥发性 |
| B.该实验证明了分子是不断运动的 |
| C.该化学反应中原子的种类发生了改变 |
| D.白烟是该反应生成的固体小颗粒悬浮于空气中形成的 |
鸡蛋腐败会发出一种无色、有臭鸡蛋气味的气体(H2S).硫化氢气体是一种大气污染物,它在空气中点燃能完全燃烧生成二氧化硫和水,把硫化氢气体通入浓硫酸中,发生的反应为:H2S+H2SO4(浓)=SO2+S↓+2H2O
(1)从上述叙述中,归纳出硫化氢的物理性质:① 、② ;硫化氢的化学性质是:① 、② .
(2)若工厂排放的尾气中含有硫化氢,用浓硫酸来吸收是否可以? ,原因是 .
下列几种溶液敞口置于空气中,溶质成分不变,但溶质的质量分数减小且溶液质量增加的是( )
| A.浓硫酸 | B.浓盐酸 | C.浓硝酸 | D.石灰水 |
把氢气、二氧化碳、一氧化碳的混合气体一次通过:①炽热的炭层;②灼热的氧化铜;③浓硫酸。经充分反应后,最后得到的纯净干燥的气体是
| A.一氧化碳 | B.二氧化碳 | C.氢气 | D.水蒸气 |
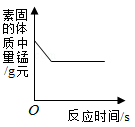
下列图像能正确反映对应变化关系的是
 |
 |
 |
 |
| A.一定质量的碳酸钠中不断加入盐酸 |
B.向一定质量的铜锌合金样品中不断加入稀硫酸 |
C.用酒精灯加热一定质量的高锰酸钾固体 |
D.向盛有少量二氧化锰的烧杯中不断加入过氧化氢溶液 |
为了探究影响大理石与稀盐酸反应剧烈程度的因素,某学习小组将稀盐酸分成四等份,分别加入四支试管中进行下列对比实验。

① ② ③ ④
下列对比实验的设计不合理的是
| 选项 |
对比实验 |
探究影响因素 |
| A |
①和② |
反应物的接触面积 |
| B |
②和③ |
温度 |
| C |
②和④ |
温度 |
| D |
③和④ |
反应物的接触面积 |
四个图像分别对应四个变化过程,其中正确的是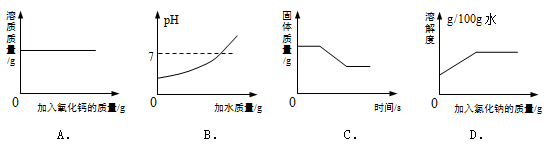
| A.一定量的饱和石灰水中加入氧化钙 |
B.向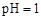 的溶液中加水 的溶液中加水 |
| C.高温煅烧一定质量的石灰石 |
| D.t℃时,在一定量的氯化钠不饱和溶液中不断加入氯化钠固体 |
常温下测得一些食物的近似pH,显碱性的是
| A.苹果汁:3.1 | B.番茄汁:4.2 | C.牛奶:6.5 | D.玉米粥:7.5 |
有一种干燥剂,它的主要成分是生石灰,其化学式为 。将该干燥剂放入水中搅拌,其中主要反应的化学方程式 ,滴入无色酚酞显 色。反应后,取出少量清液于试管中,再向这清液中吹气,有关的化学反应方程式为 。
某工业盐酸中因含有少量FeCl3(不含其它杂质)而显黄色,测知该盐酸中H+和Cl—的个数比为88∶97,则其中Fe3+和Cl-的个数比为
| A.1∶97 | B. 1∶3 | C. 3∶1 | D.3∶97 |
人体内一些体液的近似pH如下,其中碱性最强的是
| A.胃液(0.9~1.5) | B.胰液(7.5~8.0) |
| C.胆汁(7.1~7.3) | D.血浆(7.35~7.45) |
试题篮
()