(10滨州11).欲除去下列物质中的少量杂质,所用试剂正确的是
| |
物质 |
杂质 |
试剂 |
| A |
CO2 |
HCl气体 |
NaOH溶液 |
| B |
NaNO3溶液 |
Na2SO4溶液 |
Ba(OH)2溶液 |
| C |
稀盐酸溶液 |
CuCl2 |
KOH溶液 |
| D |
CaCO3 |
Na2CO3 |
H2O |
下列除去杂质所选择的试剂错误的是( )
| 选项 |
物质 |
杂质 |
所选试剂 |
| A |
CO2 |
水蒸气 |
浓硫酸 |
| B |
CaCl2溶液 |
盐酸 |
CaCO3 |
| C |
Cu |
CuO |
稀盐酸 |
| D |
NaCl溶液 |
NaOH溶液 |
BaCl2溶液 |
除去下列各物质中的少量杂质(括号内为杂质),其中方法错误的是( )
| A.Cu粉(Fe粉):用磁铁吸 | B.NaOH(NaNO3):加稀盐酸 |
| C.NaCl(泥沙):溶解、过滤、蒸发 | D.O2(水蒸气):用浓H2SO4干燥 |
下面除去混合物中少量杂质(括号内为杂质)的方案中,不合理的是
混合物 思路方法 选用物质
| A.CO2(CO)点燃空气 |
| B.NaOH(Na2CO3)沉淀、过滤石灰乳[Ca(OH)2] |
| C.FeCl2(CuCl2) 置换、过滤铁粉 |
| D.NaCl(MgCl2) 沉淀、过滤 NaOH |
将下列物质同时加入到水中,能大量共存且得到无色透明溶液的是 ( )
| A.CaCl2HCl NaNO3 | B.KOHHCl (NH4)2SO4 |
| C.K2CO3 Ba(NO3)2NaOH | D.FeCl3NaClKNO3 |
下列离子能在PH = 12的水溶液中大量共存的是( )
| A.SO42-、NO3-、K+、H+ | B.Na+、Cl-、OH-、Al3+ |
| C.Cl-、NO3-、K+、Na+ | D.Ag+、Cl-、CO32-、K+ |
下列几组物质中能按照右边关系图进行转化的一组是( )(→表示反应一步完成)
| 物质 |
A |
B |
C |
D |
| X |
Fe2O3 |
C |
CaCO3 |
Cu |
| Y |
Fe |
CO |
CaO |
CuO |
| Z |
FeCl2 |
CO2 |
Ca(OH)2 |
Cu(OH)2 |
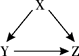
(10南京市20).现有铁、氧化铁、稀盐酸、氢氧化钙溶液、碳酸钠溶液五种物质.存在如图所示的相互反应和转化关系。图中“——”表示两端的物质间可以发生化学反应.“→”表示物质问存在相应的转化关系。下列判断合理的是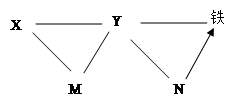
| A.X一定是碳酸钠溶液 |
| B.Y一定是稀盐酸 |
| C.N转化为铁的反应都属于置换反应 |
| D.X、Y、M两两之间都可以发生复分解反应 |
把含镁元素质量相等的下列物质,投入足量且等质量的稀盐酸中充分反应后,所得溶液中的MgCl2质量分数最小的是: ( )
| A.Mg | B.MgO | C.Mg(OH)2 | D.MgCO3 |
下列各级物质的溶液不用其它试剂就可鉴别的是:
| A.HCl CuCl2NaNO3 Na2SO4 | B.BaCl2 Na2CO3 HCl (NH4)2CO3 |
| C.FeCl3 HCl NaCl NaOH | D.Na2CO3 Na2SO4HCl H2SO4 |
下图所示的图象对应叙述关系正确的是 ( )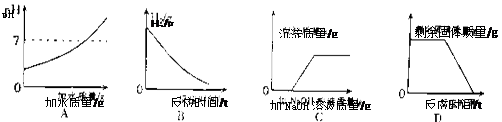
| A.向PH=3的溶液中加水 |
| B.一定质量的稀盐酸与锌粒反应 |
| C.向H2SO4和CuSO4混合溶液中加NaOH溶液 |
| D.煅烧一定质量的石灰石 |
向装有50g稀硫酸的小烧杯中,不断慢慢滴加10%的Ba(OH)2溶液至过量。有关量的变化情况见下图 (横坐标表示氢氧化钡溶液的质量,纵坐标表示小烧杯中量的变化)。其中肯定不正确的是 ( )

根据右图所示的溶解度曲线(A、B都为固态物质),判断下列说法中正确的是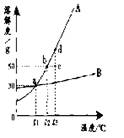
A.t1℃时,A和B饱和溶液的质量分数都为30%
B.t3℃时A的溶解度比B大,故A溶液的质量分数也一定比B溶液大
C.B的浓溶液的质量分数一定比A的稀溶液大
D.把c点对应A的溶液降温至t2℃可得到A的饱和溶液,继续降温可析出A晶体
(10孝感5)向硝酸银、硝酸铜、硝酸镁的混合溶液中加入一些铁粉,待完全反应后,再过滤。下列情况不可能存在的是( ).
| A.滤纸上有Ag,滤液中有Ag+、Cu2+、Fe2+、Mg2+ |
| B.滤纸上有Ag、Cu,滤液中有Ag+、Fe2+、Mg2+ |
| C.滤纸上有Ag、Cu,滤液中有Fe2+、Mg2+ |
| D.滤纸上有Ag、Cu、Fe,滤液中有Fe2+、Mg2+ |
(10义乌10)下列反应中,属于置换反应的是( )
A.CO+CuO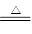 Cu+CO2 Cu+CO2 |
B.3Fe+2O2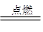 Fe3O4 Fe3O4 |
| C.Cu+2AgNO3=2Ag+Cu(NO3)3 | D.CaCO3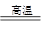 CaO+CO2↑ CaO+CO2↑ |
试题篮
()