牙膏中常用碳酸钙粉末做摩擦剂,利用石灰石(杂质不溶于水和酸)制备纯净碳酸钙的一种方法如图。
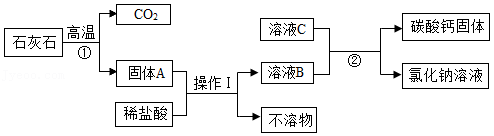
(1)反应①的化学方程式为 ;操作1的名称是 。
(2)反应②的化学方程式为 ,该反应属于 反应(填基本反应类型)。
(3)该方法中,用稀硫酸代替稀盐酸对制备碳酸钙是否有影响?判断并简述理由 。
(4)大气中CO2含量不断上升,会导致 。我国在联台国大会上提出:努力争取2060年前实现“碳中和”,请提出一条实现“碳中和”的措施 。
随着世界人口的增长,人类对农产品需求量增大,增施化肥逐渐成为农作物增产的最有力措施。NH4HCO3、NH4Cl、K2SO4、KCl都是常见的化肥。
(1)化肥能为农作物补充的营养元素主要有三种,上述化肥含有的两种营养元素是 。
(2)有一包用剩的肥料,可能含有上述四种化肥中的一种或几种,为确定其成分,进行了如下实验:
a.取少量肥料样品于研钵中,加入少量熟石灰混合研磨,有刺激性气味。
b.取少量肥料样品于烧杯中,加水溶解,得到无色溶液A。
c.取少量溶液A于试管中,滴加AgNO3溶液,有白色沉淀产生。
d.取少量溶液A于试管中,滴加BaCl2溶液,无明显现象。
e.取少量溶液A于试管中,滴加稀盐酸,无明显现象。
①分析上述实验过程,关于该肥料的成分可以得到的结论是 。
②实验a~e中,不必要进行的一项是 (填标号)。
③设计实验方案进一步确定该肥料的成分,完成下表。(已知:NH4Cl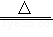 NH3↑+HCl↑)
NH3↑+HCl↑)
实验操作 |
预期现象与结论 |
|
若 ,则该肥料的成分是 。 若 ,则该肥料的成分是 。 |
镉(Cd)及其化合物在电镀、电池、颜料等领域中有广泛应用。镉是种“氢前金属”,金属活动性介于锌和铜之间。镉元素常见化合价为+2。
(1)将含镉物质进行分类,各举一例填入图中(写化学式)。
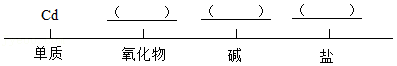
(2)根据金属化学性质的一般规律,下列预测合理的是 (填标号)。
A.镉能与氢氧化钠溶液反应
B.H2或CO能将镉的氧化物转化为金属镉
C.镉能与盐酸或稀硫酸反应
D.硫酸镉溶液中的硫酸锌可加入镉粉除去
(3)已知硫酸镉易溶于水,设计三种制备硫酸镉的方案(要求含镉原料分别属于不同的物质类别)。完成下表:
方案 |
预期反应的化学方程式 |
依据的反应规律 |
① |
|
金属活动性顺序里,前面的金属能把后面的金属从它化合物的溶液里置换出来 |
② |
|
(略) |
③ |
|
(略) |
某校学生利用如图所示两个实验探究酸的性质。

(1)试管A中溶液变浑浊的反应是 (写化学方程式)。
(2)试管B中铁钉变得光亮且表面有气泡生成,溶液呈黄色,将此时溶液中和液面上方存在的微观粒子的种类在图中补充完整(粒子数目不作要求:不考虑空气、水)。
(3)将所有学生完成上述两个实验产生的废液收集并处理,向该废液中加入适量Na2CO3,除去钙、铁元素和过量的酸,可观察到:① ,②产生大量沉淀。静置过滤得到无色溶液,经检测pH约为7,取样滴加 溶液,无明显现象,钙已除尽。
(4)若处理废液时共消耗Na2CO3 212g,则实验室为本次探究实验至少准备了 g盐酸。(已知盐酸的质量分数为7.3%)
阅读下列短文并回答问题。
氢在太阳中的核聚变放出大量光和热,是太阳能的来源,掌握可控核聚变技术对人类未来文明发展至关重要。2021年5月,中科院“人造太阳”EAST实验装置创造了氘、氚核聚变在1.2亿摄氏度下运行101秒的新纪录,为世界核聚变研究的发展作出巨大贡献。
氢气是高热值清洁燃料,目前主要通过电解水和天然气重整的方法获取氢气,其中天然气重整制氢的一种原理为:CH4+H2O CO+3H2,CO+H2O
CO+3H2,CO+H2O CO2+H2。氢氧燃料电池已被用作汽车驱动电源,H2和O2在电池内部(含有H2SO4或KOH等物质的溶液)发生反应产生电能。另外,CH4、C2H5OH等也可用作燃料电池的燃料,它们在燃料电池中的反应本质上与它们在O2中的燃烧相同。
CO2+H2。氢氧燃料电池已被用作汽车驱动电源,H2和O2在电池内部(含有H2SO4或KOH等物质的溶液)发生反应产生电能。另外,CH4、C2H5OH等也可用作燃料电池的燃料,它们在燃料电池中的反应本质上与它们在O2中的燃烧相同。
原子名称 |
质子数 |
中子数 |
核外电子数 |
氘(dao) |
1 |
1 |
1 |
氚(chuān) |
1 |
2 |
1 |
(1)氘、氚原子的构成如表,它们都属于氢元素的原因是 相同。
(2)上述短文出现的物质中,属于碱的是 (填化学式)。
(3)电解18g H2O理论上能获得 g H2。
(4)上述天然气重整制氢原理的两个反应中,化合价保持不变的元素是 。
(5)燃料电池工作时H2SO4溶液中起导电作用的离子是 (填化学符号)。
(6)CH4在O2中充分燃烧的化学方程式是 。
初步学会运用简单的装置和方法制取某些气体,是初中生化学实验技能应达到的要求。
(1)某学习小组将实验室制取常见气体的相关知识归纳如下。

气体 |
制取方法(或原理) |
发生装置 |
收集装置 |
O2 |
方法1:加热 |
均可选择A装置(可根据需要添加棉花) |
均可选择 装置(填代号) |
方法2:加热氯酸钾和二氧化锰的混合物 |
|||
方法3:利用过氧化氢溶液 |
均可选择 装置(填代号) |
||
CO2 |
反应原理:化学方程式为
|
(2)该小组同学将制取的O2和CO2(各一瓶)混淆了,设计如下方案进行区分。
实验方案 |
实验现象 |
实验结论 |
方案1:将带火星的木条分别伸入两个集气瓶中 |
若带火星的木条
|
则该瓶气体是O2 |
方案2:向两个集气瓶中分别滴入少量的 溶液,振荡 |
若溶液变浑浊 |
则该瓶气体是CO2 |
方案3:向两个集气瓶中分别倒入少量的水,振荡后再加几滴紫色石蕊溶液 |
若紫色石蕊溶液变 色 |
则该瓶气体是CO2 |
…… |
…… |
…… |
(3)实验室制取气体的过程主要包括:a.选择制取装置;b.验证所得气体;c.明确反应原理。你认为这3个过程的合理顺序应为 (填代号)。
已知:H2+CuO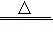 Cu+H2O。有文献报道:在氢气还原氧化铜的一些实验中,得到的固体产物是铜和氧化亚铜(Cu2O)组成的混合物。氧化亚铜为红色固体,在空气中溶于氨水得到蓝色溶液。某兴趣小组对此开展如下探究。
Cu+H2O。有文献报道:在氢气还原氧化铜的一些实验中,得到的固体产物是铜和氧化亚铜(Cu2O)组成的混合物。氧化亚铜为红色固体,在空气中溶于氨水得到蓝色溶液。某兴趣小组对此开展如下探究。

Ⅰ.设计如图1实验装置,开展氢气还原氧化铜实验并检验固体产物。
(1)制取氢气的化学方程式为 。
(2)氧化钙的作用是 。
(3)取反应后的红色固体于烧杯中,加入氨水并搅拌,观察到 ,证明固体产物有Cu2O。
Ⅱ.探究反应生成Cu2O的变化情况。
称取若干份质量均为0.6000g的CuO,在相同条件下分别用氢气还原不同时间(t),检测所得固体中Cu2O的质量(m),结果如图2。
(4)由图2可知,在氢气还原氧化铜反应过程中,Cu2O质量的变化趋势是 。
(5)为确保氢气还原氧化铜所得固体产物不含Cu2O,应采取的措施是 。
Ⅲ.探究反应生成Cu2O的原因。
为解释实验结果,兴趣小组对氢气还原氧化铜的反应过程提出如下假设:
假设1.经历2CuO+H2 Cu2O+H2O,H2+Cu2O
Cu2O+H2O,H2+Cu2O 2Cu+H2O两个反应,且在同一条件下两个反应同时进行。
2Cu+H2O两个反应,且在同一条件下两个反应同时进行。
假设2.经历CuO+H2 Cu+H2O、Cu+CuO
Cu+H2O、Cu+CuO Cu2O、H2+Cu2O
Cu2O、H2+Cu2O 2Cu+H2O三个反应。
2Cu+H2O三个反应。
(6)结合探究Ⅱ结果计算分析,假设1中“在同一条件下两个反应能同时进行”合理的依据是 。
(7)若要确认“假设2”是否合理,在探究Ⅱ的基础上,还需进行的实验是 。
下列装置常用于实验室制取气体。
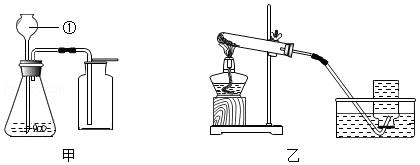
(1)仪器①的名称是 。
(2)用装置甲制取氧气,采用该收集方法的依据是 。用收集的氧气做铁丝燃烧实验,应预先在集气瓶中加入少量的 。
(3)用装置乙制取气体,实验结束时,为防止水槽里的水倒流,应采取的操作是 。
(4)在加热条件下,用醋酸钠(CH3COONa)固体与碱石灰中氢氧化钠反应制取甲烷,同时生成碳酸钠,应选用的装置是 (填“甲”或“乙”),反应的化学方程式为 。
为方便推测某些复杂物质的化学性质,可将其化学式改用常见物质的化学式表示。如碱式碳酸铜[Cu2(OH)2CO3]可改为Cu(OH)2•CuCO3,推测其兼具Cu(OH)2和CuCO3的化学性质。
(1)举重运动员常用碱式碳酸镁[Mg2(OH)2CO3]粉末抹在手掌以增大摩擦力。
①参照上述方法,碱式碳酸镁的化学式可改写为 。
②该物质兼具 (填“酸”或“碱”)和碳酸盐的化学性质。
③该物质分解的化学方程式为Mg2(OH)2CO3 2X+H2O+CO2↑,X的化学式为 。
2X+H2O+CO2↑,X的化学式为 。
(2)某种茶垢清洁剂的主要成分为过碳酸钠(可表示为2Na2CO3•3H2O2)。将过碳酸钠溶解于热水中,有大量气泡产生,其原因是 ;当不再产生气泡后,往溶液中加入足量澄清石灰水,反应的化学方程式为 。
用如图实验验证CO2的性质。
(1)实验室制取CO2的化学方程式为 。
(2)观察到短蜡烛熄灭后,关闭K,片刻后长蜡烛熄灭,由此得到的结论是 。
(3)观察到纸花变红,由此并不能得出“CO2能与水发生化学反应”的结论,理由是 。

用如图实验验证可燃物燃烧的条件,已知:白磷的着火点为40℃。

(1)实验1,能验证可燃物燃烧需要O2的现象是 。
(2)实验2,①中纸片燃烧,②中纸片未燃烧,②中纸片未燃烧的原因是 。
用如图装置研究酸、碱的性质。
(1)向1中滴加Na2CO3溶液,观察到的现象是 。
(2)向2、3中滴加无色酚酞溶液,溶液变红的是 (填序号);再向3中滴加NaOH溶液,NaOH与盐酸反应的化学方程式为 。

如图是去除粗盐中难溶性杂质实验的三步操作。

(1)三步操作的正确顺序是 (填序号)。
(2)B中,用璃棒不断搅拌的目的是 。
用如图实验(夹持仪器已略去)研究铁的性质。
(1)实验1,观察到蜡片熔化,说明铁具有的性质是 。
(2)实验2,反应的化学方程式为 。

试题篮
()