已知A~G为初中化学常见的七种物质。其中A~E属于五种不同类别的物质,B中只含两种元素,D是一种最常用的溶剂。各种物质间的反应和转化关系如图所示(“一”表示相连的两种物质之间可以发生反应,“→”表示一种物质可以转化为另一种物质,反应条件、部分反应物和生成物已略去),请分析后回答:
(1)物质D的名称是 。
(2)D→A的基本反应类型为 反应。
(3)B—F发生反应的实验现象是 。
(4)物质C所属物质类别是 。
(5)写出G→B的化学方程式 。

根据如图中的实验装置回答:
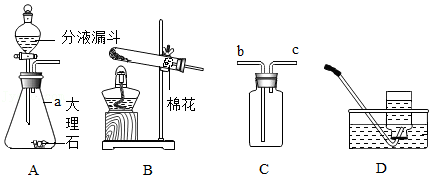
(1)仪器a的名称是 。
(2)用装置A制取CO2,分液漏斗中盛装的药品是 ;用装置C收集CO2,气体应从导管口 (填“b”或“c”)通入。
(3)用装置B制取O2,检查装置气密性的操作是 ,试管中反应的化学方程式为 。
(4)某同学在学习氮肥时,查阅资料:
①氨气极易溶于水,其水溶液称为氨水;
②氨水在浓度大或受热时易分解放出氨气。
实验室用生石灰和浓氨水能快速制取氨气的原因是 ;制得的氨气 (填“能”或“不能”)用装置D收集。
我国将力争2060年前实现碳中和。CO2的捕捉是减少碳排放的措施之一。
(1)一种利用NaOH溶液捕捉回收CO2的过程如图所示。
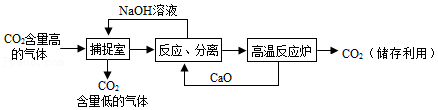
①捕捉室中NaOH溶液常喷成雾状,优点是 。
②“反应分离“环节发生的复分解反应是 (写化学方程式)。
③“反应分离”环节分离物质采用的方法是 。
④CO2用途广泛,写出一种用途: 。
(2)CaO固体也可以捕捉回收CO2。研究表明CaC2O4•H2O热分解制得的CaO疏松多孔,具有良好的CO2捕捉性能。取1.46g CaC2O4•H2O进行加热,固体质量随温度变化如图。
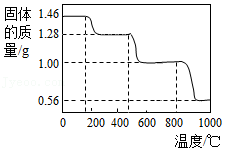
①写出400~600℃范围内分解反应的化学方程式: (CaC2O4•H2O的相对分子质量:146)。
②据图分析,CaO捕捉CO2的反应温度应 (填“高于”或“低于”)800℃。
A、B、C、D、E为初中化学常见的物质,其中A、C为金属单质,E为非金属单质,如图是它们之间的相互转化关系。请回答:
(1)反应①的基本反应类型是 。
(2)写出反应②的化学方程式 。
(3)E的化学式是 ,产生无色气体E的原因是 。
(4)金属C在 的条件下容易生锈;保护金属资源的有效途径是 (只写一条)。

新型高导热镁合金常用作电动汽车和消费电子产品的散热器。请根据如图回答有关问题。

(1)由图1可知,镁的相对原子质量为 。
(2)图2为镁离子的结构示意图,则x的数值为 ,表示镁离子的符号为 。
(3)以化合价为纵坐标、物质类别为横坐标所绘制的图叫价类二维图。图3为镁的价类二维图,B处的物质类别是 。MgO中镁元素与氧元素的质量比为 。价类二维图中的物质在一定条件下可以相互转化,例如金属镁和水发生反应可以生成A和一种单质,则该反应的化学方程式为 。
为解决能源与环境问题,有学者提出如图1所示的含碳物质转化的技术路线。
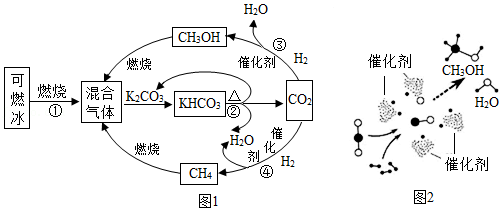
(1)“可燃冰”中甲烷完全燃烧的化学方程为 。
(2)反应②属于 (填基本类型)。
(3)反应④中,参加反应的CO2和生成的CH4的分子数目之比为 。
(4)我国学者开发促进反应③的一种新型催化剂,催化过程微观示意图如图2。该过程的中间产物 (填化学式)、氧和氢进一步作用生成甲醇(CH3OH)和水。
(5)该技术路线有利用于实现 (填标号)。
A.碳循环利用
B.减少碳排放
C.减少白色污染
如图为我国古代“布灰种盐”生产海盐的部分场景,其过程为“烧草为灰,布在滩场,然后以海水渍之,俟晒结浮白,扫而复淋”。
(1)“晒结浮白”是指海水浸渍的草灰经日晒后出现白色海盐颗粒的过程,化学上称之为 。
(2)经过多次“扫而复淋”,提高卤水浓度获得“上等卤水”(氯化钠的质量分数为15%),用于煎炼海盐。
①1000g“上等卤水”蒸干后,可得到氯化钠的质量约为 g。
②从燃料利用角度分析,用获得的“上等卤水”而不直接用海水煎炼海盐的原因是 。
③将“上等卤水”在100℃恒温蒸发至刚有晶体析出,所得溶液的组成为:150g溶液中含水 100g、NaCl 39.8g、MgCl2 7.65g及其他成分2.55g。将150g此溶液降温至20℃,有 g NaCl析出(溶解度见表)。此时, (填“有”或“没有”)MgCl2析出,原因是 。
温度/℃ |
20 |
60 |
100 |
|
溶解度/g |
NaCl |
36.0 |
37.3 |
39.8 |
MgCl2 |
54.8 |
61.3 |
73.0 |
|

“嫦娥五号”月球采样返回,“天问一号”成功抵达火星,标志着我国航天事业取得突破性进展。
(1)月壤含CaAl2Si2O8以及可作为核聚变燃料的氦﹣3等物质。
①CaAl2Si2O8中,Si、O两种元素的质量比为 。
②如图为氦元素在元素周期表中的部分信息。氦﹣3原子的质子数与中子数之和为3,则其中子数为 ,核外电子数为 。
(2)着陆器上的仪器可探测水。若月球上存在大量的水,可利用光催化分解水技术得到氧气,对人类在月球上活动意义重大,该反应的化学方程式为 。
(3)火星拥有丰富的金属矿物和二氧化碳等资源。火星低层大气的主要成分如下表。
气体成分 |
CO2 |
N2 |
Ar |
O2 |
其他 |
体积分数/% |
95.32 |
2.7 |
1.6 |
0.13 |
0.25 |
①为鉴别一瓶模拟“火星低层大气”组成的气体和一瓶空气,可采用的化学方法是 。
②若为满足人类未来在火星上生活,下列研究设想不合理的是 。
A.将CO2转化为O2,提高O2含量
B.将CO2分解转化为N2,提高N2含量
C.寻找水的存在和开发水循环技术
D.利用火星上的金属矿物冶炼金属
高纯CO可用于半导体领域某些芯片的刻蚀,利用甲酸(HCOOH)制取高纯CO的主要流程如图:

(1)甲酸中碳元素和氧元素的质量比为 。
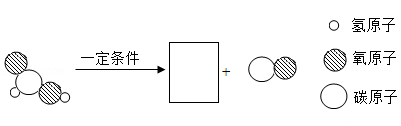
(2)反应塔中甲酸分解的微现示意图如图,在方框中补全另一种产物的微粒图示 。
(3)反应塔中发生副反应产生微量CO2。洗涤器中加入NaOH溶液的目的是中和未反应的甲酸蒸气,并除去CO2,NaOH与CO2反应的化学方程式为 。
真空热还原法生产钙的主要转化过程如图:

(1)石灰石的主要成分是 。
(2)Ⅱ中反应有两种产物,固体X一定含有氧元素和铝元素,从元素守恒角度说明理由 。
(3)装置Ⅲ中发生的是 (填“物理”或“化学”)变化。
阅读下面科普短文。
碳元素是人类接触和利用最早的元素之一。由碳元素组成的单质可分为无定形碳、过液态碳和晶形碳三大类,如图1。

石墨是制铅笔芯的原料之一,在16世纪被发现后,曾被误认为是含铅的物质。直到18世纪,化学家将石墨与KNO3共熔后产生CO2,才确定了它是含碳的物质。
碳纤维既有碳材料的固有本质特性,又有纺织纤维的柔软可加工性,综合性能优异。目前,我国已形成碳纤维生产、碳纤维复合材料成型,应用等产业链,碳纤维复合材料应用领域分布如图2。
科学界不断研发出新型碳材料,碳气凝胶就是其中一种。碳气凝胶具有优良的吸附性能,在环境净化中发挥重要作用。我国科研人员在不同温度下制备了三种碳气凝胶样品,比较其对CO2的选择性吸附性能。他们在不同压强下测定了上述样品对混合气体中CO2吸附的选择性值,实验结果如图3。图中选择性值越高,表明碳气凝胶对CO2的选择性吸附性能越好。
随着科学技术的发展,碳材料的潜能不断被激发,应用领域越来越广泛。
依据文章内容回答下列问题:
(1)金刚石属于 (填序号)。
A.无定形碳
B.过渡态碳
C.晶形碳
(2)石墨与KNO3共熔,能发生如下反应,配平该反应的化学方程式:5C+4KNO3
K2O+ N2↑+ CO2↑。
(3)由图2可知,我国碳纤维复合材料应用占比最高的领域是 。
(4)判断下列说法是否正确(填“对”或“错”)。
①石墨是一种含铅的物质 。
②碳材料其有广阔的应用和发展前景 。
(5)对比图3中三条曲线,得到的实验结论是 。
天然气是常见的化石燃料。
(1)做饭时,若燃气灶的火焰呈现黄色或橙色,锅底出现黑色,应将炉具的进风口调 (填"大"或"小")。
(2)含160g甲烷的天然气充分燃烧,生成二氧化碳的质量是多少克?(根据化学方程式进行计算)
硝酸钾的溶解度曲线如图所示。回答下列问题:
(1)30℃时,硝酸钾的溶解度是 g。
(2)60℃时,在100g水中加入60g硝酸钾固体,充分搅拌,所得溶液是 (填"饱和"或"不饱和")溶液。
(3)将(2)中所得的溶液从60℃降温至30℃,可析出硝酸钾晶体 g,此时溶液的溶质质量分数 45.8%(填">""<"或"=")。

A是目前世界年产量最高的金属,根据如图回答下列问题:
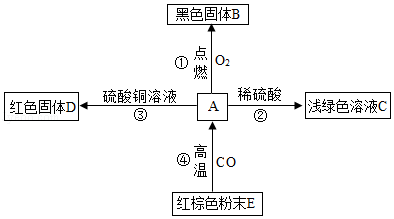
(1)B的名称是 。
(2)溶液C中溶质的化学式为 。
(3)D可用于制 ,③可证明铁的金属活动性比铜 (填"强"或"弱")。
(4)②的基本反应类型是 。
(5)④的化学方程式为 。
试题篮
()