X、Y、Z、W、E五种短周期元素在元素周期表的位置如图。其中W的原子序数是Y的2倍。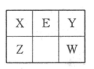
(1)能证明X、Z两元素非金属性强弱的离子方程式为
(2)一定条件下,在恒容容器中,充人一定量的WY2 (g)和XY (g),发生反应: 时,各物质的平衡浓度如下表:
时,各物质的平衡浓度如下表: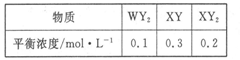
①若温度升高到 T2℃时,反应的平衡常数为6.64,则该反应的逆反应为______反应(填“吸热”或“放热”)。
②其他条件不变,若该反应在恒压条件下进行,平衡时XY的转化率a2______a1(T1℃时的转化率)(填“<”“>”“=”)
(3)室温下,Mg(OH)2饱和溶液______(填“能”或“不能”)使石蕊试液变蓝,通过计算说明原因(已知: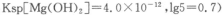 。答
。答
(4)化学反应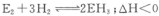 在工业生产中有重要的地位,若要提高E2的转化率,可采取的措施是______(填字母代号)
在工业生产中有重要的地位,若要提高E2的转化率,可采取的措施是______(填字母代号)
a.升高温度 b.加催化剂 c.增加H2的浓度 d.分离出EH3
一定条件下,1mol E2与3molH2在密闭容器中反应达到平衡,E2的转化率为25%且放出23.lkJ能量,则该条件下反应的热化学反应方程式为____________________.
(5)电化学降解法可用于治理水中硝酸盐的污染,其原理如图所示。其中B为电源的______极,其电极反应式为______。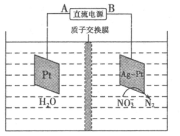








 粤公网安备 44130202000953号
粤公网安备 44130202000953号