现有一含NaCl杂质的Na2CO3样品,取13.9g样品溶于水,配成104.4g溶液,此溶液与100g某浓度的盐酸恰好完全反应,得到200g溶液。请计算:
(1)生成的二氧化碳的质量为 g;
(2)所得溶液中NaCl的质量分数(写出计算步骤)。
在一个密闭容器中放入X、Y、Z、M四种物质,使之在一定条件下发生化学反应。一段时间后,测得有关数据如下表:
物质 |
X |
Y |
Z |
M |
反应前的质量/g |
20 |
5 |
3 |
28 |
反应后的质量/g |
待测值 |
30 |
3 |
8 |
关于此反应的认识不正确的是( )
A.物质Z可能是该反应的催化剂
B.该反应一定是化合反应
C.参加反应的Y、M的质量比为5:4
D.待测值为13
我国历史悠久,“四大发明”闻名世界,其中“火药”是“四大发明”之一。黑火药爆炸的化学方程式为:S+2KNO3+3C═K2S+X↑+3CO2↑,其中X的化学式为( )
A.N2 B.NO2 C.NOD.SO2
现有等质量甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中化合价均为+2价)。则下列说法中错误的是( )

A.金属活动性:乙>甲>丙
B.生成氢气的质量:甲>乙>丙
C.相对原子质量:乙>丙>甲
D.消耗硫酸的质量:甲>乙>丙
阅读下面关于“水果打蜡”的科普短文。
农科院的专家给夏橙打上一种食用蜡﹣﹣蜂蜡。目的是为了防腐保鲜,减少维生素C的流失。蜂蜡的主要成分C46H92
O2,是由十六烷酸(C16H32O2)与三十烷醇(C30H62O)形成的脂,人体接触少量食用蜡不会产生危害。但是,用工业蜡(主要成分可表示为CxHy)处理水果,对人体会造成伤害。蜂蜡遇热会熔化,把打了蜂蜡的水果放到热水中,水中浮起一层蜡,因此打蜂蜡的水果可用热水清洗。
依据短文内容,回答下列问题:
(1)十六烷酸(C16H32O2)由 种元素组成,夏橙中的维生素C (填“是”或“不是”)人类营养物质。
(2)依据短文内容归纳蜂蜡的物理性质 。
(3)十六烷酸(C16H32O2)和三十烷醇(C30H62O)反应生成蜂蜡(C46H92O2)和另一种物质X,X的化学式为 。
(4)请配平工业蜡在氧气中完全燃烧的化学方程式:4CxHy+ O2 4xCO2+2yH2O
4xCO2+2yH2O
NSR技术通过BaO和Ba(NO3)2的相互转化实现NOx(氮氧化物)的储存和还原,能有效降低柴油发动机在空气过量条件下的NOx排放。其工作原理如图所示。
(1)还原时还原尾气可以是CO、H2等,存在如下反应:5CO+Ba(NO3)2═N2+X+5CO2
①反应中,碳元素的化合价 (填“升高”或“降低”)。
②X的化学式是 。
(2)储存时,部分NO发生反应的化学方程式为 ;吸收NOx(如NO、NO2)的物质是 。
(3)NO气体通过NSR技术转化为N2的总反应方程式是 。

一氧化碳与氢气在一定条件下发生反应的微观示意图如图:
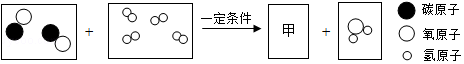
下列分析不正确的是( )
A.该反应前后分子的种类发生了改变
B.物质甲由碳、氢、氧三种原子构成
C.该反应的反应物和生成物中共有2种氧化物
D.物质甲中碳、氢、氧元素质量比为12:3:8
30g某有机物M在氧气中完全燃烧,生成44gCO2和18gH2O,下列说法不正确的是( )
A.M含有C、H、O三种元素
B.M中氧元素的质量分数约为53.3%
C.完全燃烧时,M与消耗O2的质量比为15:16
D.3.0gM在2.4gO2氧气中燃烧生成2.4gCO、1.2CO2和1.8gH2O
对于复分解反应,X+2NaOH═2Y+Cu(OH)2↓,下列分析中正确的是( )
A.X一定是CuCl2B.Y可能是H2O
C.相对分子质量大小:X>YD.Y可能是Na2SO4
宋代著名的医学家宋慈编写的《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理之一是:4Ag+2H2S+O2=2X(黑色)+2H2O下列说法中正确的是( )
A.X为Ag2S
B.金属活动性:Ag>Cu
C.反应中H2S和O2的质量比为17:16
D.反应前后,银元素、氧元素的化合价均没有改变
在点燃条件下,A和B反应生成C和D,反应前后变化的微观示意图如图所示。

根据上述信息可得出( )
A.该反应不满足质量守恒定律
B.原子在化学反应中不可再分
C.该反应的类型是化合反应
D.反应前后分子不发生改变
(1)以粗盐为原料生产自来水消毒剂ClO2的某步反应化学方程式为:2NaClO3+4HCl=2C1O2↑+Cl2↑+2X+2H2O,则X的化学式为 。
(2)过氧化钙(CaO2)是一种对环境友好的多功能无机化合物,与水反应生成一种碱并放出能使带火星的木条复燃的气体。该反应的化学方程式为 。
(3)某同学在处理含有H2SO4和CuSO4的混合物废液时,加入一定量烧碱溶液并充分反应后,有蓝色沉淀生成,过滤,滤液呈蓝色。则上述过程中生成沉淀的化学方程式为 ,滤液中一定存在的溶质是 。
将10g镁、铝的金属混合物加入到一定质量的稀硫酸中,恰好完全反应后,经测定溶液质量增加了9g,将反应后的溶液蒸干,得到固体的质量为( )
A.19gB.50gC.58gD.63g
试题篮
()