下列关于氨气的说法正确的是
| A.氨气既能用浓硫酸干燥也能用无水CaCl2干燥 |
| B.NH3是电解质,所以氨水能导电 |
| C.用水吸收NH3用如图装置可防止倒吸 |
| D.NH3可以使干燥的红色石蕊试纸变蓝 |
某稀硫酸和稀硝酸的混合溶液中c(SO42-)+c(NO3-)="2.5" mol•L-1.取200mL该混合酸,则能溶解铜的最大质量为( )
| A.12.8g | B.19.2g | C.32.0g | D.38.4g |
某固体混合物可能含有Al、(NH4)2SO4、MgCl2、AlCl3、FeCl2、NaCl中的一种或几种,现对该混合物做如下实验,所得现象和有关数据如图(气体体积已换算成标准状况下体积):下列说法不正确的是( )
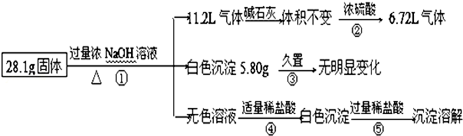
| A.混合物中一定不存在FeCl2和NaCl |
| B.反应④的离子方程式为:AlO2﹣+H++H2O=Al(OH)3↓ |
| C.混合物中一定含有Al、(NH4)2SO4、MgCl2三种物质,无法判断是否含有AlCl3 |
| D.白色沉淀5.80g是Mg(OH)2 |
2007年诺贝尔化学奖授予德国化学家Gerhard Ertl,以表彰他在表面化学领域研究所取得的开拓性成就。某反应在Pd/Al2O3/Ba催化剂表面吸附与解吸作用的机理如下图所示(图中HC表示碳氢化合物,nitrate指硝酸盐),该机理研究是指

| A.汽车尾气催化转化机理 | B.钢铁生锈机理 |
| C.合成氨工业催化氧化机理 | D.氢氧燃烧电池电极反应机理 |
硝酸是一种重要的化工原料,工业上一般以氨气为原料来制备硝酸。请回答:
(1)氨气催化氧化的化学方程式为______________________。
(2)氨气若在纯氧中燃烧,则发生反应为4NH3+3O2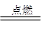 2N2+6H2O,科学家利用此原理,设计成氨气-氧气燃料电池,则通入氨气的电极是________(填“正极”或“负极”);碱性条件下,该电极发生反应的电极反应式为______________________。
2N2+6H2O,科学家利用此原理,设计成氨气-氧气燃料电池,则通入氨气的电极是________(填“正极”或“负极”);碱性条件下,该电极发生反应的电极反应式为______________________。
(3)纳米级Cu2O具有优良的催化性能,制取Cu2O的方法有:
①加热条件下用液态肼(N2H4)还原新制Cu(OH)2制备纳米级Cu2O,同时放出N2.该制法的化学方程式为______________________。
②用阴离子交换膜控制电解液中OH-的浓度制备纳米Cu2O,反应为2Cu+H2O Cu2O+H2↑,如图所示.该电解池的阳极反应式为______________________。
Cu2O+H2↑,如图所示.该电解池的阳极反应式为______________________。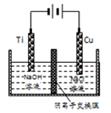
高氯酸铵(NH4ClO4)和铝粉常用作火箭推进剂的固体燃料。高温时,NH4ClO4的分解反应是:2NH4ClO4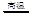 N2↑+4H2O↑+Cl2↑+2O2↑,下列有关NH4ClO4的分解及保存方法说法不合理的是
N2↑+4H2O↑+Cl2↑+2O2↑,下列有关NH4ClO4的分解及保存方法说法不合理的是
| A.点燃铝粉可以引发NH4ClO4分解 |
| B.NH4ClO4迅速分解时可能会引发爆炸 |
| C.NH4ClO4应低温通风保存,远离火种、热源 |
| D.0.5 mol NH4ClO4分解时产生的气体体积是44.8 L |
某学生利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。

A B C D E F
请回答下列问题:
(1)B装置的名称是________________;E装置的作用____________________。
(2)写出F中发生反应的离子反应方程式 。
(3)上述制氨为快速制氨,实验室常用氯化铵和氢氧化钙制备,其化学方程式为: 。
(4)装置A的烧瓶中装有生石灰,随着浓氨水的滴入,氨气产生的原因是_________。
(5)通入C装置的两根导管左边较长、右边较短,目的是_____________________________。
(6)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一。请写出反应的化学方程式:___________________________。当有a mol氯气参加反应时,转移的电子总数为b个,则阿伏加德罗常数为(用含a、b的代数式表示)________________。
根据下列有关实验得出的结论一定正确的是
| 选项 |
方法 |
结论 |
| A |
实验室制氢气,向稀H2SO4中滴加少量Cu(NO3)2溶液 |
可以加快制备氢气的反应速率 |
| B |
向Fe(NO3)2溶液中滴入用硫酸酸化的H2O2溶液, 则溶液变黄 |
氧化性:H2O2>Fe3+ |
| C |
相同温度下,等质量的大理石与等体积、等浓度的盐酸反应 |
反应速率: 粉状大理石>块状大理石 |
| D |
吸热反应“TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g)”在一定条件下可自发进行 |
则该反应的△S<0 |
硝酸是氧化性酸,其本质是NO3-有氧化性,某课外实验小组进行了下列有关NO3-氧化性的探究(实验均在通风橱中完成)。
(1)实验Ⅰ中,铝片作________(填“正”或“负”)极。液面上方产生红棕色气体的化学方程式是________。
(2)实验Ⅱ中电流计指针先偏向右边后偏向左边的原因是________。

查阅资料:活泼金属与1 mol·L-1稀硝酸反应有H2和NH4+生成,NH4+生成的原理是产生H2的过程中NO3-被还原。
(3)用上图装置进行实验Ⅲ:溶液X为1 mol·L-1稀硝酸溶液,观察到电流计指针向 右偏转。
① 反应后的溶液中含NH4+。实验室检验NH4+的方法是________。
② 生成NH4+的电极反应式是________。
(4)进一步探究碱性条件下NO3-的氧化性,进行实验Ⅳ:

① 观察到A中有NH3生成,B中无明显现象。A、B产生不同现象的解释是________。
②A中生成NH3的离子方程式是________。
(5)将铝粉加入到NaNO3溶液中无明显现象,结合实验Ⅲ和Ⅳ说明理由____________。
下图是用点滴板探究氨气的性质。实验时向NaOH固体上滴几滴浓氨水后,立即用培养皿罩住整个点滴板。下列对实验现象的解释正确的是

| 选项 |
实验现象 |
解释 |
| A |
红色石蕊试纸变蓝 |
NH3极易溶于水 |
| B |
浓硫酸附近无白烟 |
NH3与浓硫酸不发生反应 |
| C |
氯化铝溶液变浑浊 |
NH3与AlCl3溶液反应:Al3++3OH–→Al(OH)3↓ |
| D |
浓盐酸附近有白烟 |
NH3与挥发出的HCl反应:NH3+HCl→NH4Cl |
用右图所示装置进行下列实验,实验结果与预测的现象不一致的是

| |
①中的物质 |
②中的物质 |
预测①的现象 |
| A |
酚酞溶液 |
浓盐酸 |
无明显现象 |
| B |
淀粉KI溶液 |
浓硝酸 |
无明显现象 |
| C |
AlCl3溶液 |
浓氨水 |
有白色沉淀 |
| D |
湿润红纸条 |
饱和氯水 |
红纸条褪色 |
空气污染已成为人类社会面临的重大威胁。下列气体不属于大气污染物的是
| A.NO | B.CO2 | C.SO2 | D.NO2 |
试题篮
()