下列推断合理的是()
| A. |
明矾[

|
B. |
金刚石是自然界中硬度最大的物质,不可能与氧气发生反应

|
C. |
浓

|
D. |
将
|
关于浓度均为0.1 的三种溶液:①氨水、②盐酸、③氯化铵溶液,下列说法不正确的是()
| A. |
|
| B. |
水电离出的 |
| C. |
①和②等体积混合后的溶液: |
| D. |
①和③等体积混合后的溶液: |
下列叙述正确的是()
| A. |
0.1 |
| B. |
|
| C. |
|
| D. |
在 |
25 ℃时,浓度均为0.2的
和
溶液中,下列判断不正确的是()

| A. |
均存在电离平衡和水解平衡 |
| B. |
存在的粒子种类相同 |
| C. |
|
| D. |
分别加入 |
已知:25°C时,,
。下列说法正确的是()

| A. |
25°C时,饱和 |
| B. |
25°C时,在 |
| C. |
25°C时, |
| D. |
25°C时,在 |
将电解质分为强、弱电解质的依据是
| A.在一定条件下的电离程度 | B.属于离子化合物还是共价化合物 |
| C.熔融状态下是否完全电离 | D.溶于水后的导电能力是强还是弱 |
今有室温下四种溶液,有关叙述不正确的是
| |
① |
② |
③ |
④ |
| pH |
11 |
11 |
3 |
3 |
| 溶液 |
氨水 |
氢氧化钠溶液 |
醋酸 |
盐酸 |
A.①、②中分别加入适量的氯化铵晶体后,两溶液的pH均减小
B.分别加水稀释10倍,四种溶液的pH:①>②>④>③
C.①、④两溶液等体积混合,所得溶液中c(Cl-)>c(NH4+)>c(OH-)>c(H+)
D.VaL④与VbL②溶液混合后,若混合后溶液pH=4,设混合溶液体积变化忽略不计,则Va∶Vb=11∶9
A、B、C、 D、 E五种溶液分别是NaOH、NH3·H2O、CH3COOH、HCl、NH4HSO4中的一种。常温下进行下列实验:
①将1L pH=3的A溶液分别与0.001mol·L-1 xL B溶液、0.001mol·L-1 yL D溶液充分反应至中性,x、y大小关系为:y<x;
②浓度均为0.1mol·L-1A和E溶液,pH:A<E;
③浓度均为0.1mol·L-1C与D溶液等体积混合,溶液呈酸性。回答下列问题:
(1)E是 溶液。
(2) 用水稀释0.1 mol·L-1B时,溶液中随着水量的增加而减小的是 (填写序号) 。
①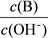 ②
②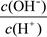 ③c(H+)
③c(H+)
④ OH-的物质的量 ⑤ c(H+)和c(OH-)的乘积
(3)OH-浓度相同的等体积的两份溶液A和E,分别与锌粉反应,若最后仅有一份溶液中存在锌粉,且放出氢气的质量相同,下列说法正确的是 (填写序号) 。
①反应所需要的时间E>A ②开始反应时的速率A>E
③参加反应的锌粉物质的量A=E ④反应过程的平均速率 E>A
⑤A溶液里有锌粉剩余 ⑥E溶液里有锌粉剩余
(4)室温下,将pH=1的A溶液aL与pH=12的D溶液bL混合,所得混合液的pH=3,设混合溶液体积变化忽略不计,则a:b= 。
(5)0.1 mol·L-1C溶液中各种离子浓度由大到小的顺序是:
。
试题篮
()