 与稀盐酸反应(放热反应)生成
与稀盐酸反应(放热反应)生成 的量与反应时间的关系如下图所示.下列结论不正确的是( )
的量与反应时间的关系如下图所示.下列结论不正确的是( )
| A.反应开始2分钟内平均反应速率最大 |
| B.反应4分钟后平均反应速率最小 |
| C.反应开始4分钟内温度对反应速率的影响比浓度大 |
D.反应在第2min到第4min间生成 的平均反应速率为 的平均反应速率为 |
某探究小组用与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用
浓度为1.00
·
、2.00
·
,大理石有细颗粒与粗颗粒两种规格,实验温度为298
、308
,每次实验
的用量为25.0
、大理石用量为10.00
。
(1)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
| 实验编号 |
大理石规格 |
实验目的 |
||
| ① |
298 |
粗颗粒 |
2.00 |
(Ⅰ)实验①和②探究 (Ⅱ)实验①和探究温度对该反应速率的影响; (Ⅲ)实验①和探究大理石规格(粗、细)对该反应速率的影响;) |
| ② |
||||
| ③ |
||||
| ④ |
(2)实验①中质量随时间变化的关系见下图:
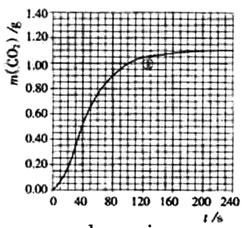
依据反应方程式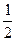
+
=
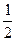
+
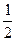
↑+
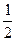
,计算实验①在70-90
范围内
的平均反应速率(忽略溶液体积变化,写出计算过程)。
(3)请在答题卡的框图中,画出实验②、③和④中质量随时间变化关系的预期结果示意图。
实验室利用Zn和稀HCl反应制取H2,下列措施中,不能提高化学反应速率的是( )
| A.增大盐酸的浓度 | B.给反应液加热 |
| C.向溶液中加入少量硫酸铜溶液 | D.向溶液中加入醋酸钠晶体 |
某温度下,在一容积可变的容器中,反应2A(g)+B(s) 2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol和4mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是( )
2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol和4mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是( )
A.均减半
B.均加倍
C.均增加1mol
D.均减少1mol
反应2X(气)+Y(气) 2Z(气)(正反应为放热反应),在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量[n(z)]与反应时间(t)的关系如图所示。下列判断正确的是( )
2Z(气)(正反应为放热反应),在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量[n(z)]与反应时间(t)的关系如图所示。下列判断正确的是( ) 
| A.T1<T2,P1<P2 |
| B.T1<T2,P1>P2 |
| C.T1>T2,P1>P2 |
| D.T1>T2,P1<P2 |
在一密闭容器中,反应aA(气)=bB(气)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%则( )
| A.平衡向正反应方向移动了 |
| B.物质A的转化率减少了 |
| C.物质B的质量分数增加了 |
| D.a>b |
可逆反应:3A(气) 3B(?)+C(?)(正反应为吸热反应)随着温度升高,气体平均相对分子质量有变小趋势,则下列判断正确的是( )
3B(?)+C(?)(正反应为吸热反应)随着温度升高,气体平均相对分子质量有变小趋势,则下列判断正确的是( )
| A.B和C可能都是固体 |
| B.B和C一定都是气体 |
| C.若C为固体,则B一定是气体 |
| D.B和C可能都是气体 |
100mL6mol/L H2SO4跟过量锌粉反应,一定温度如下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量的( )
| A.碳酸钠固体 |
| B.醋酸钠固体 |
| C.硫酸钾溶液 |
| D.硫酸铵固体 |
反应2X(g)+Y(g) 2Z(g)(正反应放热),在不同温度(T1和T2)及压强(p1和p2)下,产物Z的物质的量(n2)与反应时间(t)的关系如图10所示。下述判断正确的是( )。
2Z(g)(正反应放热),在不同温度(T1和T2)及压强(p1和p2)下,产物Z的物质的量(n2)与反应时间(t)的关系如图10所示。下述判断正确的是( )。
| A.T1<T2,p1<p2 |
| B.T1<T2,p1>p2 |
| C.T1>T2,p1>p2 |
| D.T1>T2,p1<p2 |
对于可逆反应mA(g)+nB(s) pC(g)+qD(g)反应过程中,其他条件不变时,产物D的质量分数D%与温度T或压强p的关系如图所示,请判断下列说法正确的是( )。
pC(g)+qD(g)反应过程中,其他条件不变时,产物D的质量分数D%与温度T或压强p的关系如图所示,请判断下列说法正确的是( )。
| A.降温,化学平衡向正反应方向移动 |
| B.使用催化剂可使D%有所增加 |
| C.化学方程式中气体的化学计量数m<p+q |
| D.B的颗粒越小,正反应速率越快,有利于平衡向正反应方向移动 |
图1表示mA(g)+nB(g) pC(g)+qD(g)+Q,在不同温度下经过一定时间混合体系中C的质量分数与温度T的关系;图2表示在一定条件下达到平衡(v正=v逆)后t时刻改变影响平衡的另一个条件重新建立新平衡的反应过程,判断该反应是( )。
pC(g)+qD(g)+Q,在不同温度下经过一定时间混合体系中C的质量分数与温度T的关系;图2表示在一定条件下达到平衡(v正=v逆)后t时刻改变影响平衡的另一个条件重新建立新平衡的反应过程,判断该反应是( )。
 |
 |
| 图1 曲线图 |
图2 曲线图 |
| A.m+n>p+qQ>0 |
| B.m+n>p+qQ<0 |
| C.m+n<p+qQ>0 |
| D.m+n<p+qQ<0 |
某化学反应2A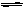 B+D在四种不同条件下进行,B、D起始浓度的起始浓度都为零,反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度的起始浓度都为零,反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
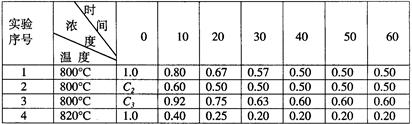
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20分钟时间内平均速率为 mol·L-1·min-1
(2)在实验2,A的初始浓度c2= mol·L-1,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是 。
(3)设实验3的反应速率为V3,实验1的反应速率为V1,则V3 V1(填>、=、<=),且c3 1.0 mol·L-1(填>、=、<=)。
(4)比较实验4和实验1,可推测该反应是__________反应(选填吸热、放热)。理由是________________。
可逆反应A(气)+B(气) 2C(气)在固定容积的容器中进行,如果向容器中充入1mol A和1mol B,在某温度下达平衡时,C的物质的量分数为m%;若向容器中充入1molC,在同样条件下,达到平衡时,C的物质的量分数为n%,则m和n的正确关系是( )
2C(气)在固定容积的容器中进行,如果向容器中充入1mol A和1mol B,在某温度下达平衡时,C的物质的量分数为m%;若向容器中充入1molC,在同样条件下,达到平衡时,C的物质的量分数为n%,则m和n的正确关系是( )
| A.m>n |
| B.m<n |
| C.m=n |
| D.无法确定 |
二氧化氮存在下列平衡:2NO2(气) N2O4(气)(正反应为放热反应)在测定NO2的相对分子质量时,下列条件中较为适宜的是( )
N2O4(气)(正反应为放热反应)在测定NO2的相对分子质量时,下列条件中较为适宜的是( )
| A.温度130℃、压强3.03×105Pa |
| B.温度25℃、压强1.01×105Pa |
| C.温度130℃、压强5.05×104Pa |
| D.温度0℃、压强5.05×104Pa |
试题篮
()