下列化学用语正确的是
| A.氯分子的电子式:Cl:Cl |
B.水分子的电子式: |
C.氯离子的结构示意图: |
D.质量数为37的氯原子: |
下列有关物理量相应的单位表达错误的是
| A.摩尔质量:g/mol | B.气体摩尔体积:mol/L |
| C.溶解度:g/100gH2O | D.密度:g/cm3 |
下列物质(或主要成分)对应的化学式中,不正确的是
| A.小苏打NaHCO3 | B.烧碱NaOH | C.绿矾FeSO4·7H2O | D.钡餐BaCO3 |
用镁铝合金制作的窗框、卷帘门、防护栏等物品轻巧、美观、耐用。与上述这些特点无关的镁铝合金的性质是
| A.不易生锈 | B.导电性好 | C.密度小 | D.强度高 |
化合物A(C12H16O2)经碱性水解、酸化后得到B和C(C8H8O2)。C的核磁共振氢谱表明含有苯环,且苯环上有2种氢原子。B经过下列反应后得到G(C8H12O4),核磁共振氢谱显示只有一个峰。
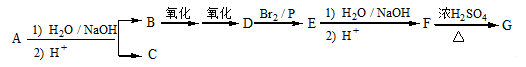
已知:
请回答下列问题:
(1)A的结构简式: 。
(2)写出F→G反应的化学方程式: ,该反应属于 (填反应类型)。
(3)写出满足下列条件的C的所有同分异构体的结构简式(至少写出3种): 。
①是苯的对位二取代化合物; ②能与FeCl3溶液发生显色反应;
③不考虑烯醇(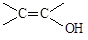 )结构。
)结构。
下列关于甲、乙、丙、丁四个图像的说法中,正确的是

| A.图甲表示向盐酸溶液中通入NH3过程中溶液导电性的变化 |
| B.由图乙可知,若除去CuSO4溶液中的Fe3+可采用向溶液中加入适量CuO至pH在4左右 |
| C.图丙表示25 ℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1氨水,溶液的pH随加入盐酸体积的变化 |
| D.图丁表示向Al2(SO4)3溶液中滴入NaOH溶液,生成Al(OH)3沉淀的量随NaOH溶液体积的变化 |
某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴、阳极,槽中盛放含铬废水,原理示意图如右图所示,下列说法中不正确的是
| A.A为电源正极 |
| B.阴极区附近溶液pH降低 |
| C.阳极区溶液中发生的氧化还原反应为Cr2O72-+6Fe2++14H+===2Cr3++6Fe3++7H2O |
| D.若不考虑气体的溶解,当收集到H2 13.44 L(标准状况)时,有0.1 mol Cr2O72-被还原 |
现有常温下的四份溶液: ① 0.01 mol/L CH3COOH ② 0.01 mol/LHCl ③pH=12的氨水 ④ pH=12的NaOH溶液,下列说法正确的是
| A.①中水的电离程度最小,③中水的电离程度最大 |
| B.将四份溶液稀释相同倍数后,溶液的pH:②﹥①,③﹥④ |
| C.将②③混合,若pH=7,则消耗溶液的体积:②﹥③ |
| D.将①、④混合,若有c(CH3COO-)﹥c(H+),则混合液一定呈碱性 |
下列说法正确的是
| A.室温某酸溶液的pH等于3,则由水电离产生的c(H+)=1×10-11mol/L |
B.对于反应X+3Y2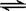 Z,增大压强使平衡向生成Z的方向移动,平衡常数增大 Z,增大压强使平衡向生成Z的方向移动,平衡常数增大 |
| C.自发反应一定是熵增大,非自发反应一定是熵减小或不变 |
| D.某温度下,向AgCl饱和溶液中加入蒸馏水,AgCl的溶解度、Ksp均增大 |
下列除去杂质的实验方法正确的是
| A.除去CO中混有的少量O2:通过灼热的Cu网后收集气体 |
| B.除去SO2中混有的CO2:可通过盛有KMnO4溶液的装置洗气 |
| C.除去FeCl3酸性溶液中少量的FeCl2:加入稍过量双氧水后放置 |
| D.除去SiO2中的Fe2O3:可加入NaOH溶液后过滤 |
有机物H是一种药物的有效成分,其合成路线如下:
根据以上信息回答下列问题:
(1)A的结构简式为________,F含有的官能团是________(填名称)。
(2)反应①的条件是________,反应②的类型是________。
(3)合成的产物H具有的性质为________ (填序号)。
| A.在水中溶解度大于苯酚 |
| B.既有酸性又有碱性 |
| C.能发生缩聚反应 |
| D.能与溴水发生加成反应 |
(4)写出B在浓碱、高压条件下水解的化学方程式________。
(5)写出符合下列条件的D的一种同分异构体________。
①苯环上只有一个侧链②能和NaOH发生中和反应③分子中无甲基
(6)已知:① 发生取代时,在羧基间位取代;②
发生取代时,在羧基间位取代;② 易发生氧化反应。以A为原料合成化合物
易发生氧化反应。以A为原料合成化合物 的设计合成路线为(其他试剂任选):(合成路线流程图示例:
的设计合成路线为(其他试剂任选):(合成路线流程图示例:  )
)
利用周期表中同族元素的相似性,可预测元素的性质。
(1)P元素的基态原子有_______个未成对电子,白磷的分子式为P4,其结构如下图所示。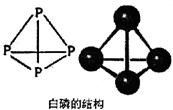
科学家目前合成了N4分子,N原子的杂化轨道类型是________,N -N键的键角为________;N4分解后能产生N2并释放出大量能量,推测其用途为________。
(2) N、P、As原子的第一电离能由大到小的顺序为________。
(3)立方氮化硼晶体的结构如下图所示:
该晶体中,B原子填充在N原子的________空隙,且占据此类空隙的比例为________ (填百分数)。
(4) N与As是同族元素,B与Ga是同族元素,立方砷化镓晶体与立方氮化硼晶体结构类似,两种晶体中熔点较高的是________;立方砷化镓晶体的晶胞边长为a pm,则其密度为________g·cm-3 (用含a的式子表示,设NA为阿伏加德罗常数的值)。
已知t ℃时的Ksp (AgC1) =1.6×10-10,Ksp (AgBr )=7.8×10-13;在t℃时,Ag2CrO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是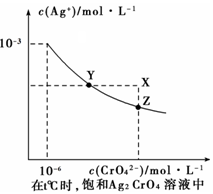
| A.t℃时,Ksp (Ag2CrO4 )=1×10-9 |
| B.t℃时,在饱和Ag2CrO4溶液中加入AgNO3可使溶液由Z点到X点 |
| C.t℃时,溶解度的大小顺序为AgC1 > Ag2CrO4>AgBr |
| D.t℃时,取一定量的KCl和KBr的混和溶液,向其中滴加AgNO3溶液,当AgCl开始沉淀时,c(C1-)/c(Br-)= Ksp (AgC1)/ Ksp (AgBr) |
试题篮
()