NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A.在标准状况下,分子总数为NA的H2和O2混合气体,其体积约为22.4L |
| B.5.6g铁与足量的氯气反应,转移电子数为0.2NA |
| C.11.2LH2O所含有的原子数为1.5NA |
| D.0.2mol/L的Na2CO3溶液中含有的Na+数为0.4NA |
欲配制1.00mol/L的NaCl溶液80mL,下列说法正确的是( )
| A.应选用100mL容量瓶 |
| B.配置之前容量瓶中残留的蒸馏水会导致浓度偏高 |
| C.定容时腐蚀刻度会导致浓度偏低 |
| D.摇匀、静置后发现凹液面低于刻度线,再加水至刻度线即可 |
下列物质对应分类不正确的是( )
| A.Na2S——钠盐 | B.H2SO4——电解质 | C.豆浆——胶体 | D.纯碱——碱 |
下列含氧酸中,酸性最弱的是
| A.HClO | B.HNO2 | C.H2CO3 | D.HIO4 |
书写热化学方程式时要注明物质的状态,其主要原因是
| A.物质的状态与反应热有关 | B.物质的状态与生成物有关 |
| C.可以具体说明反应进行的情况 | D.可以具体说明反应发生的条件 |
下列反应既是氧化还原反应,又是吸热反应的是
| A.铝片与稀硫酸的反应 | B.灼热的碳与二氧化碳反应 |
| C.甲烷在氧气中的燃烧 | D.Ba(OH)2·8H2O与NH4Cl的反应 |
下列物质不是配合物的是
| A.NH4Cl | B.Fe(SCN)3 | C.CuSO4•5H2O | D.[Ag(NH3)2]OH |
根据电子排布的特点,Cu在周期表属于
| A.s区 | B.p区 | C.d 区 | D.ds区 |
工业上将纯净干燥的氯气通入到0.5 mol·L-1 NaOH溶液中得到漂白水。
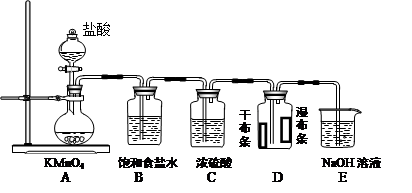
某同学想在实验室探究Cl2性质并模拟制备漂白水,上图是部分实验装置。已知KMnO4与浓盐酸反应可以制取Cl2。(注:装置D中布条为红色)
(1)配平KMnO4与盐酸反应的化学方程式:
KMnO4+ HCl(浓) = KCl + MnCl2+ Cl2↑+ H2O
(2)如果反应中转移0.5mol电子,则生成Cl2的物质的量为_______________。
(3)浓硫酸的作用是 。
(4)实验时装置D中的现象是 。
(5)装置E中发生化学反应的离子方程式为 。
(6)配制500 mL物质的量浓度为0.5 mol·L-1 NaOH溶液时,主要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒和 ,需称量的NaOH的质量是 。
NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。
(1)上述反应中氧化剂是____________。
(2)根据上述反应,鉴别NaNO2和NaCl。可选用的物质有:①水、②碘化钾淀粉试纸、③淀粉、④白酒、⑤食醋,你认为必须选用的物质有____________(填序号)。
(3)某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是____________。
| A.NaCl | B.NH4Cl | C.HNO3 | D.浓H2SO4 |
(1)0.5 mol CO2的质量为___________,其中含有__________个CO2分子,在标准状况下的体积是 。
(2)标准状况下,1.92 g某气体的体积为672 mL,则此气体的相对分子质量为____________。
(3)想一想:Ba(OH)2(固体)、CuSO4(固体)、CH3COOH(液体)这三种物质为什么可以归为一类,下列哪些物质可以和它们归为一类 (填序号)。
A 75%的酒精溶液 B 硝酸钠 C 碱石灰 D 豆浆 E 过氧化钠
(4)洁厕灵(强酸性,含盐酸)与84消毒液(碱性,含NaClO)混用可能使人中毒。请写出中毒涉及反应的离子方程式 。
下列离子方程式书写正确的是
| A.Cu与FeCl3溶液反应:Cu+ Fe3+= Cu2++ Fe2+ |
| B.碳酸钙溶于稀盐酸:CO32-+ 2H+ =H2O + CO2↑ |
| C.FeSO4溶液和NaOH溶液反应:Fe2+ + 2OH- = Fe(OH)2↓ |
| D.氯气溶于水:Cl2 + H2O = 2H+ + ClO- + Cl- |
配制一定物质的量浓度的某溶液,下列情况会使配制结果偏高的是
| A.定容摇匀后发现液面低于刻度线,再加水至刻度线 |
| B.容量瓶中原来含有少量蒸馏水 |
| C.未洗涤烧杯和玻璃棒 |
| D.定容时俯视刻度线观察液面 |
试题篮
()