含有吡喃萘醌骨架的化合物常具有抗菌、抗病毒等生物活性,一种合成该类化合物的路线如图(部分反应条件已简化):

回答下列问题:
(1)B的结构简式为_____;
(2)从F转化为G的过程中所涉及的反应类型是_____、_____;
(3)物质G所含官能团的名称为_____、_____;
(4)依据上述流程提供的信息,下列反应产物J的结构简式为_____;
(5)下列物质的酸性由大到小的顺序是_____(写标号);
①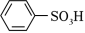 ②
② ③
③
(6)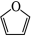 (呋喃)是一种重要的化工原料,其能够发生银镜反应的同分异构体中,除
外,还有_____种;
(呋喃)是一种重要的化工原料,其能够发生银镜反应的同分异构体中,除
外,还有_____种;
(7)甲苯与溴在 催化下发生反应,会同时生成对溴甲苯和邻溴甲苯。依据由C到D的反应信息,设计以甲苯为原料选择性合成邻溴甲苯的路线 _____(无机试剂任选)。
[化学——选修5:有机化学基础]
氟他胺G是一种可用于治疗肿瘤的药物。实验室由芳香烃A制备G的合成路线如下:
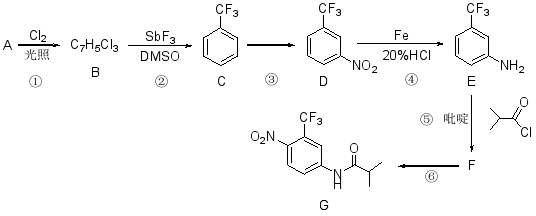
回答下列问题:
(1)A的结构简式为________。C的化学名称是________。
(2)③的反应试剂和反应条件分别是________,该反应的类型是________。
(3)⑤的反应方程式为________。吡啶是一种有机碱,其作用是________。
(4)G的分子式为________。
(5)H是G的同分异构体,其苯环上的取代基与G的相同但位置不同,则H可能的结构有________种。
(6)4-甲氧基乙酰苯胺( 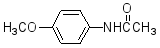 )是重要的精细化工中间体,写出由苯甲醚(
)是重要的精细化工中间体,写出由苯甲醚(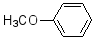 )制备4-甲氧基乙酰苯胺的合成路线________(其他试剂任选)。
)制备4-甲氧基乙酰苯胺的合成路线________(其他试剂任选)。
化合物W可用作高分子膨胀剂,一种合成路线如下:

回答下列问题
(1)A的化学名称为________。
(2)②的反应类型是________。
(3)反应④所需试剂,条件分别为________。
(4)G的分子式为________。
(5)W中含氧官能团的名称是________。
(6)写出与E互为同分异构体的酯类化合物的结构简式(核磁共振氢谱为两组峰,
峰面积比为1:1)________。
(7)苯乙酸苄酯( 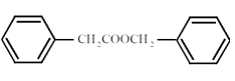 )是花香类香料,设计由苯甲醇为起始原料制备苯乙酸苄酯的合成路线________(无机试剂任选)。
)是花香类香料,设计由苯甲醇为起始原料制备苯乙酸苄酯的合成路线________(无机试剂任选)。
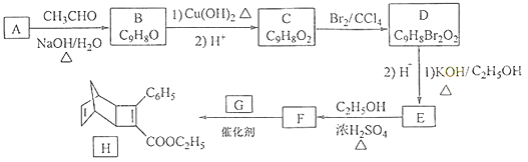
化合物H是一种有机光电材料中间体.实验室由芳香化合物A制备H的一种合成路线如下:
已知:①
② 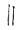 +
+ 

回答下列问题:
(1)A的化学名称为为________.
(2)由C生成D和E生成F的反应类型分别为________、________.
(3)E的结构简式为________.
(4)G为甲苯的同分异构体,由F生成H的化学方程式为________.
(5)芳香化合物X是F的同分异构体,X能与饱和碳酸氢钠溶液反应放出 , 其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为6:2:1:1,写出2种符合要求的X的结构简式________.
(6)写出用环戊烷和2﹣丁炔为原料制备化合物 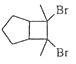 的合成路线________(其他试剂任选).
的合成路线________(其他试剂任选).
近期发现, 是继NO、CO之后第三个生命体系气体信号分子,它具有参与调解神经信号传递、舒张血管减轻高血压的功能.回答下列问题:
(1)下列事实中,不能比较氢硫酸与亚硫酸的酸性强弱的是(填标号).
| A. |
氢硫酸不能与碳酸氢钠溶液反应,而亚硫酸可以 |
| B. |
氢硫酸的导电能力低于相同浓度的亚硫酸 |
| C. |
的氢硫酸和亚硫酸的pH分别为4.5和2.1 |
| D. |
氢硫酸的还原性强于亚硫酸 |
(2)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理.

通过计算,可知系统(Ⅰ)和系统(Ⅱ)制氢的热化学方程式分别为________、________,制得等量H 2所需能量较少的是________.
(3) 与 在高温下发反应:生 .在610k时,将 与 充入2.5L的空钢瓶中,反应平衡后水的物质的量分数为0.02.
① 的平衡转化率 =________%,反应平衡常数K=________.
②在620K重复试验,平衡后水的物质的量分数为0.03, 的转化率 ________ , 该反应的△H________0.(填">""<"或"=")
③向反应器中再分别充入下列气体,能使 转化率增大的是________(填标号)
| A. |
|
B. |
|
C. |
COS |
D. |
|
水煤气变换
是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。回答下列问题:
(1)Shibata曾做过下列实验:①使纯 缓慢地通过处于 下的过量氧化钴 ,氧化钴部分被还原为金属钴 ,平衡后气体中 的物质的量分数为0.0250。
②在同一温度下用 还原 ,平衡后气体中 的物质的量分数为0.0192。
根据上述实验结果判断,还原 为 的倾向是 _________(填"大于"或"小于") 。
(2) 时,在密闭容器中将等物质的量的 和 混合,采用适当的催化剂进行反应,则平衡时体系中 的物质的量分数为_________(填标号)。
A. B. C. D. E.
(3)我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用*标注。

可知水煤气变换的 ________(填"大于""等于"或"小于")0。该历程中最大能垒(活化能) =_________ ,写出该步骤的化学方程式_______________________。
(4)Shoichi研究了 时水煤气变换中 和 分压随时间变化关系(如图所示)催化剂为氧化铁,实验初始时体系中的 和 相等、 和 相等。
计算曲线a的反应在 内的平均速率 (a)=___________ 。 时 和 随时间变化关系的曲线分别是_______、_______。 时 和 随时间变化关系曲线分别是 、 。

有机碱,例如二甲基胺(  )、苯胺(
)、苯胺( 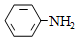 )、吡啶(
)、吡啶(  )等,在有机合成中应用很普遍,目前"有机超强碱"的研究越来越受到关注。以下为有机超强碱F的合成路线:
)等,在有机合成中应用很普遍,目前"有机超强碱"的研究越来越受到关注。以下为有机超强碱F的合成路线:

已知如下信息:
①H 2C=CH 2
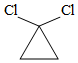
② 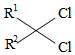 +RNH 2
+RNH 2

③苯胺与甲基吡啶互为芳香同分异构体
回答下列问题:
(1)A的化学名称为 。
(2)由B生成C的化学方程式为 。
(3)C中所含官能团的名称为 。
(4)由C生成D的反应类型为 。
(5)D的结构简式为 。
(6)E的六元环芳香同分异构体中,能与金属钠反应,且核磁共振氢谱有四组峰,峰面积之比为6:2:2:1的有 种,其中,芳香环上为二取代的结构简式为 。
羟基乙酸钠易溶于热水,微溶于冷水,不溶于醇、醚等有机溶剂。制备少量羟基乙酸钠的反应为ClCH2COOH+2NaOH→HOCH2COONa+NaCl+H2O△H<0
实验步骤如下:
步骤1:在如图所示装置的反应瓶中,加入40g氯乙酸、50mL水,搅拌。逐步加入40% NaOH溶液,在95℃继续搅拌反应2小时,反应过程中控制pH约为9。
步骤2:蒸出部分水至液面有薄膜,加少量热水,趁热过滤。滤液冷却至15℃,过滤得粗产品。
步骤3:粗产品溶解于适量热水中,加活性炭脱色,分离掉活性炭。
步骤4:将去除活性炭后的溶液加到适量乙醇中,冷却至15℃以下,结晶、过滤、干燥,得羟基乙酸钠。
(1)步骤1中,如图所示的装置中仪器A的名称是 ;逐步加入NaOH溶液的目的是 。
(2)步骤2中,蒸馏烧瓶中加入沸石或碎瓷片的目的是 。
(3)步骤3中,粗产品溶解于过量水会导致产率 ( 填“增大”或“减小”);去除活性炭的操作名称是 。
(4)步骤4中,将去除活性炭后的溶液加到适量乙醇中的目的是 。

软锰矿的主要成分为MnO2,除含有Fe2O3、MgO、Al2O3、CaO、SiO2等杂质,工业上用软锰矿制取MnSO4·H2O的流程如下: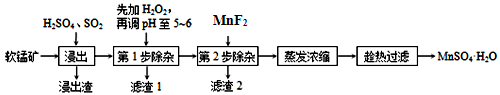
已知:①部分金属阳离子完全沉淀时的pH如下表: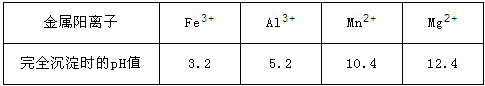
②温度高于27℃时,MnSO4晶体的溶解度随温度的升高而逐渐降低。
(1)“浸出”过程中MnO2转化为Mn2+的离子方程式为_____________。
(2)调pH至5~6的目的是___________,调pH至5~6所加的试剂可选择_________(填以下试剂的序号字母);
a.NaOHb.MgOc.CaOd.氨水
(3)第2步除杂,主要是将Ca2+、Mg2+转化为相应氟化物沉淀除去,写出MnF2除去Mg2+的离子反应方程式_________,该反应的平衡常数数值为_________。
(已知:MnF2的KSP=5.3×10-3;CaF2的KSP=1.5×10-10;MgF2的KSP=7.4×10-11)
(4)取少量MnSO4•H2O溶于水,配成溶液,测其pH发现该溶液显酸性,原因是______(用离子方程式表示),该溶液中所有离子的浓度由大到小的顺序为________。
某小组同学探究浓硫酸及其部分反应产物的化学性质,装置如下图所示(夹持装置略去)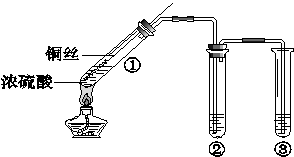
(1)试管①中反应的化学方程式是 。该反应表明浓硫酸具有 (填序号)。
a.酸性 b.强氧化性 c.还原性
(2)若试管②中的试剂为品红溶液,实验中观察到的现象是 ,说明试管①中生成的气体具有 性。
(3)若试管②中的试剂为酸化的Ba(NO3)2溶液,观察到生成不溶于硝酸的白色沉淀,说明试管①中生成的气体具有 性。
(4)试管③中的试剂为NaOH溶液,反应的离子方程式是 。
草木灰中富含钾盐,主要成分是碳酸钾,还含有少量氯化钾和硫酸钾等。现从某草木灰样品中提取钾盐,并检验其中的CO32-、SO42-和Cl-。
(1)从草木灰中提取钾盐的实验操作步骤如下,请补充完整:
① ②过滤③蒸发浓缩④冷却结晶⑤过滤。
(2)上述操作中需要用到玻璃棒的是 (填序号)。
(3)将制得的少量晶体加水溶解后,分别置于三支试管中。
①向第一支试管中加入少量稀盐酸,可观察到 ,说明溶液中存在 离子。
②向第二支试管中加入 ,可观察到 ,说明溶液中存在SO42-。③向第三支试管中先加入足量Ba(NO3)2溶液,过滤后,再向滤液中加入足量 溶液,可观察到白色沉淀,说明溶液中存在Cl-。其中,加入足量Ba(NO3)2溶液的目的是 。
(Ⅰ)实验室中盐酸的用途十分广泛,常用来制备气体。
(1)某小组同学欲配制230mL0.4mol/L盐酸,则需取用4mol/L盐酸_________mL,实验中需要用到的玻璃仪器有___________、___________、量筒、烧杯、胶头滴管。
(2)下列实验操作使配制的溶液浓度偏低的是___________。
| A.容量瓶洗涤后未干燥 |
| B.移液时,有少量溶液溅出 |
| C.定容时,加水不慎超出刻度线,又倒出一些 |
| D.量取溶液时,仰视刻度线 |
E.装入试剂瓶时,有少量溶液溅出
(Ⅱ)瑞典化学家舍勒将软锰矿(主要成分为MnO2)与浓盐酸混合加热,在世界上首先得到了氯气。已知Cl2和碱溶液在不同条件下,得到的产物不同,某兴趣小组用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。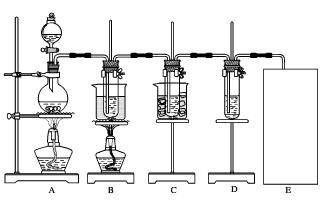
图中:A为氯气发生装置;B的试管里盛有15mL30%KOH溶液,并置于水浴中;C的试管里盛有15mL8%NaOH溶液,并置于冰水浴中;D的试管里盛有紫色石蕊试液。
请填写下列空白:
(1)制取氯气时,在圆底烧瓶里加入一定质量的二氧化锰,通过__________(填仪器名称)向圆底烧瓶中加入适量的浓盐酸。装置A中反应的离子方程式是__________________。
(2)制取氯酸钾是在装置B中进行的,装置B中制取氯酸钾的化学反应方程式是___________。该小组同学发现制得的氯酸钾产量偏低,原因是氯气中含有杂质,改进方法是_________。
(3)实验中装置D的试管中产生的现象是_______________。
(4)请在装置图方框中画出上述实验还缺少的装置,并注明试剂。
(5)该小组同学认为:SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。但是如果将SO2和Cl2同时通入到品红溶液中,则会发现褪色效果并不像该小组同学想象的那样。请你分析原因(用离子方程式表示)____________________。
某探究小组为探究氯气的性质,并用装置F制取少量“漂白液”,设计了如下实验装置。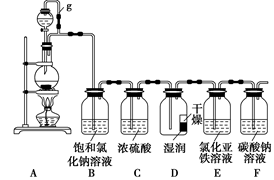
请回答下列问题:
(1)写出实验室制氯气的离子方程式: 。
(2)装置A中g管作用是___________,装置B的作用是 ,装置C的作用是 。
(3)反应一段时间后用注射器从E中抽取少量溶液,检验有Fe3+生成,请写出检验方法________。
(4)已知HCO3-的酸性弱于次氯酸,请写出少量的氯气与F中足量的碳酸钠溶液反应的化学方程式:______________________。
某小组同学用下图装置进行实验研究(a、b、c表示止水夹)。请评价或完善其方案:
(1)将装置A、C、E相连接,用MnO2和浓盐酸制取氯气,请回答:
①A中反应的离子方程式:_ 。
②E中氢氧化钠溶液的作用 。在C中加入适量的水可制得氯水.将所得氯水分成两份进行实验,其操作、现象和结论为:
| 实验序号 |
实验操作 |
现象 |
结论 |
| Ⅰ |
将氯水滴入品红溶液 |
品红溶液褪色 |
氯气有漂白性 |
| Ⅱ |
氯水中加入碳酸氢钠粉末 |
有无色气泡产生 |
氯气与水反应的产物具有酸性 |
③实验Ⅰ推出的相应结论是否合理?________,若不合理,请说明理由(若合理,无需填写)____________。
④实验Ⅱ推出相应的结论是否合理?_______,若不合理,请说明理由(若合理,无需填写)_____________。
(2)将B、D、E相连,在B中装浓硝酸和铜片,可制得NO2并进行有关实验。
①B中反应的化学方程式________________________。
②先若关闭c,当丁中充满红棕色的NO2时,再关闭止水夹a、b ,微热试管丁,丁中可观察到的实验现象 。
某课外活动小组模拟工业制备纯碱,方案如下:
(一)实验原理:NaCl+H2O+NH3+CO2═NaHCO3↓+NH4Cl
向饱和食盐水中通入足量氨气至饱和,然后通入二氧化碳,析出溶解度较小的碳酸氢钠.
(二)实验装置:所需实验药品和装置如图所示:
(三)实验步骤
(1)搭好装置,然后应该进行的操作是__________。
(2)中间的烧瓶中加入20mL饱和食盐水,并将其浸入冰水中;D中加入足量氢氧化钠固体,E中加入足量浓氨水;B中加入足量碳酸钙粉末,A中加入足量稀硫酸于(可分多次加入).仪器A的名称是__________,选择用稀硫酸而不用稀盐酸的好处是__________。
(3)先打开__________(填K1或K2),将装置A或E中的试剂慢慢加入圆底烧瓶,烧瓶中产生气体的原理是__________,大约20分钟左右时,观察到饱和食盐水上方有__________大量的白雾
现象时,再打开__________(填K1或K2),将装置A或E中的试剂慢慢加入圆底烧瓶,大约5分钟即有浑浊出现,约15分钟出现大量白色固体.
(四)纯碱制备:
(4)上述实验结束后,欲得到纯碱,将固体过滤、洗涤后,还需进行的操作是__________(不加任何其它试剂,装置任选),反应的化学方程式为__________;若将上述操作产生的气体全部通过浓硫酸,再通过足量的过氧化钠,过氧化钠增重0.28g,则制得的纯碱质量为__________g。
试题篮
()