下列实验能获得成功的是
| A.乙醇与2mol·L-1的硫酸溶液混合加热到170℃制乙烯 |
| B.苯与溴水反应制取溴苯 |
| C.要鉴别己烯中是否混有少量甲苯,最恰当的实验方法是先加足量的酸性高锰酸钾溶液,然后再加入溴水 |
| D.电石与饱和食盐水作用制乙炔 |
现有溴苯、乙醇、甲苯、己烯四种液体,只用一种试剂就可以将它们区别开,这种试剂是( )
| A.溴水 | B.食盐水 | C.NaOH溶液 | D.酸性KMnO4溶液 |
常温常压下,乙烷、乙炔和丙烯组成的混合烃64mL,与过量氧气混合并完全燃烧,除去水蒸气,恢复到原来的温度和压强,气体总体积缩小了112 mL,原混合烃中乙炔的体积分数为( )
| A.12.5% | B.25% | C.50% | D.75。 |
鉴别甲烷、乙烯、乙炔三种气体可采用的方法是( )
| A.通入溴水中,观察溴水是否褪色 |
| B.通入酸性高锰酸钾溶液中,观察颜色变化 |
| C.点燃,检验燃烧产物 |
| D.点燃,观察火焰明亮程度及产生黑烟量的多少 |
两种不同的烃CxHy和CaHb不论以什么比例混合,只要总质量一定,完全燃烧时消耗O2的质量和生成水的质量不变,下列叙述正确的是( )
| A.CxHy和CaHb分子中氢原子系数一定相等 |
| B.可能是C2H4和C3H6的混合物 |
| C.CxHy和CaHb一定是同分异构体 |
| D.CxHy和CaHb的最简式可以不同 |
实验室制备苯甲醇和苯甲酸的化学原理是
已知苯甲醛易被空气氧化,苯甲醇的沸点为205.3 ℃,苯甲酸的熔点为121.7 ℃,沸点为249 ℃,溶解度为0.34 g;乙醚的沸点为34.8 ℃,难溶于水。制备苯甲醇和苯甲酸的主要过程如下所示:
试根据上述信息,判断以下说法错误的是( )
| A.操作Ⅰ是萃取分液 |
| B.乙醚溶液中所溶解的主要成分是苯甲醇 |
| C.操作Ⅱ蒸馏所得产品甲是苯甲醇 |
| D.操作Ⅲ过滤得到产品乙是苯甲酸钾 |
在C2H2、C6H6、C2H2O2组成的混合物中,已知氧元素的质量分数为8%,则混合物中碳元素的质量分数是( )
| A.92.3% | B.87.6% | C.75% | D.84. 9% |
已知某有机物A的红外光谱和核磁共振氢谱如图所示:
下列说法中不正确的是( )
| A.由红外光谱可知,该有机物中至少有三种不同的化学键 |
| B.由核磁共振氢谱可知,该有机物分子中有三种不同的氢原子 |
| C.仅由其核磁共振氢谱无法得知其分子中的氢原子总数 |
| D.若A的化学式为C2H6O,则其结构简式为CH3—O—CH3 |
质谱法能够对有机分子进行结构分析。其方法是让极少量的(10-9 g)化合物通过质谱仪的离子化室,样品分子大量离子化,少量分子碎裂成更小的离子。如C2H6离子化可得到C2H6+、C2H5+、C2H4+……然后测定其质荷比。设H+的质荷比为β,其有机物样品的质荷比如图所示(假设离子均带一个单位正电荷,信号强度与该离子的多少有关),则该有机物可能是( )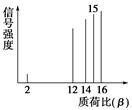
| A.甲醇(CH3OH) | B.甲烷 | C.丙烷 | D.乙烯 |
如图是一个核磁共振氢谱,请你观察图谱,分析其可能是下列物质中的( )
| A.CH3CH2CH2CH3 | B.(CH3)2CHCH3 |
| C.CH3CH2CH2OH | D.CH3CH2COOH |
某气态有机物X含C、H、O三种元素,已知下列条件,现欲确定X的分子式,所需的最少条件是( )
①X中含碳质量分数
②X中含氢质量分数
③X在标准状况下的体积
④质谱确定X的相对分子质量
⑤X的质量
A.①② B.①②④ C.①②⑤ D.③④⑤
仔细分析下列表格中烃的排列规律,判断排列在第16位烃的分子式是( )
| 1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
…… |
| C2H2 |
C2H4 |
C2H6 |
C3H4 |
C3H6 |
C3H8 |
C4H6 |
C4H8 |
C4H10 |
|
A.C6H12 B.C6H14 C.C7H12 D.C7H14
某有机物在氧气中充分燃烧,生成的CO2和H2O的物质的量之比为1∶2,下列说法正确的是( )
A.分子中C、H、O个数之比为1∶2∶3
B.分子中C、H个数之比为1∶4
C.分子中一定含有氧原子
D.此有机物的最简式为CH4
下列是除去括号内杂质的有关操作,其中正确的是( )
| A.分离苯和己烷—分液 |
| B.NO(NO2)—通过水洗、干燥后,用向下排气法收集 |
| C.乙烷(乙烯)—让气体通过盛酸性高锰酸钾溶液的洗气瓶 |
| D.乙醇(乙酸)—加足量NaOH溶液,蒸馏 |
试题篮
()