下列结论错误的是( )
①微粒半径:r(K+)>r(Al3+)>r(S2-)>r(Cl-) ②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③还原性:S2->Cl->Br->I- ④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO ⑥非金属性:O>N>P>Si
⑦金属性:Be<Mg<Ca<K
| A.① | B.①③ | C.②③④⑤⑥⑦ | D.①③⑤ |
已知1~18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同电子层结构,下列关系正确的是( )
| A.质子数:c>d | B.离子的还原性:Y2->Z- |
| C.氢化物的稳定性:H2Y>HZ | D.原子半径:X<W |
根据中学化学教材所附元素周期表判断,下列叙述不正确的是( )
| A.第16列元素的最高价氧化物的化学式为RO3 |
| B.第2列元素中一定没有非金属元素 |
| C.第15列元素的最高价氧化物对应的水化物的化学式可能为H3RO4 |
| D.某元素的离子最外层电子数与次外层相同,该元素一定位于第三周期 |
有五组同族元素的物质,在101.3kPa时测定它们的沸点( )如下表所示:
)如下表所示: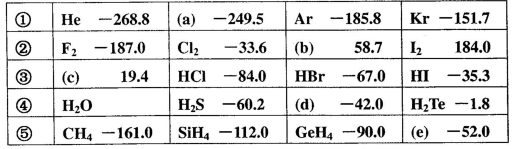
对应表中内容,下列各项中正确的是
A.a、b、c的化学式分别为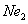 、 、 、 、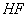 |
| B.第②组物质均有氧化性;第③组物质对应水溶液均是强酸 |
C.第④组中各化合物的稳定性顺序为: |
| D.上表中同族物质对应的氢化物的沸点,均随相对分子质量的增大而升高 |
短周期主族元素A、B、C、D的原子序数依次增大,A和B形成的气态化合物的水溶液呈碱性,B位于第VA族,A和C同主族,D原子最外层电子数与电子层数相等。下列叙述正确的是
A.原子半径:D>C>B
B.单质的还原性:D>C
C元素A、B、C的氧化物均为非金属氧化物
D.元素B、C、D的最高价氧化物对应的水化物能相互反应
下列结论是从某同学的作业本上摘录的,其中你认为肯定正确的是
①微粒半径:S2->Cl->Cl>S ②氢化物稳定性:HF>HCl>H2S>H2Se
③还原性:S2->Cl->Br->I- ④氧化性:Cl2>S>Se
⑤酸性:H2SO4>HClO4>H2SeO4 ⑥得电子能力:F>Cl>Br>I
| A.只有① | B.②④⑥ | C.①③④ | D.只有⑥ |
PM2.5细颗粒物含有的毒性物质来源之一是汽车尾气排放。通过排气管加装催化装置,可有效减少CO和NO的排放,催化装置内发生的反应为:NOx + CO N2 + CO2,下列关于此反应的说法中,错误的是( )
N2 + CO2,下列关于此反应的说法中,错误的是( )
| A.所涉及元素中原子半径: C>N>O |
| B.氧化剂与还原剂的物质的量之比为1︰1时,NOx中氮元素的化合价为+2价 |
| C.当x = 2时,每生成1mol N2,转移电子数为4mol ,N2为氧化产物 |
| D.等物质的量N2和CO2中,共价键的个数比为3︰4 |
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法正确的是( )
| A.第一电离能和电负性: Z>W>Q |
| B.元素W的最高价氧化物对应的水化物的酸性比Q的强 |
| C.离子半径X3-<Z 3+ |
| D.元素X与元素Q二者的氢化物能化合生成离子化合物 |
如下图是从元素周期表中截取下来 的,A、B、C为短周期主族元素,下列说法中正确的是( )
A.D一定是金属元素,其金属性比C强 B.C的最高价氧化物水化物显强酸性
C.B的氢化物是以分子形式存在,且分子内含极性共价键
D.E的原子序数一定是A的5倍,且原子半径比A大
X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。下列说法正确的是( )
| A.元素Y、Z、W具有相同电子层结构的离子,其半径依次增大 |
B.元素X不能与元素Y形成化合物 |
C.元素Y、R分别与元素X形成的化合物的热稳定性: |
| D.元素W、R的最高价氧化物的水化物都是强酸 |
右表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
| A.Y、Z的阴离子电子层结构都与R原子的相同 |
| B.常压下,Y单质的沸点比Z单质的沸点低 |
| C.W的氢化物的稳定性比X的氢化物的稳定性强 |
| D.Y元素的非金属性比W元素的非金属性强 |
几种短周期元素的原子半径及主要化合价如下表:
| 元素代号 |
X |
Y |
Z |
W |
| 原子半径/pm |
160 |
143 |
70 |
66 |
| 主要化合价 |
+2 |
+3 |
+5、+3、-3 |
-2 |
下列叙述正确的是( )
A.X、Y元素的金属性 X < Y
B.一定条件下,Z单质与W的常见单质直接生成ZW2
C.Y的最高价氧化物对应的水化物能溶于稀氨水
D.一定条件下,W单质可以将Z单质从其氢化物中置换出来
有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族;X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料。下列说法中,正确的是( )
| A.X、M两种元素只能形成X2M型化合物 |
| B.由于W、Z、M元素的氢化物相对分子质量依次减小,所以其沸点依次降低 |
| C.元素Y、Z、W的单质晶体属于同种类型的晶体 |
| D.元素W和M的某些单质可作为水处理中的消毒剂 |
有A、B、C、D四种元素,其中A、B、C属于同一周期,A原子最外层p能级的电子数等于次外层的电子总数;B原子最外层中有三个不成对的电子;C元素可分别与A、B、D生成RC2型化合物,其中的DC2与C3互为等电子体。下列叙述中不正确的是
A.D原子的简化电子排布式为[Ar]3s23p4
B.B、C两元素的第一电离能大小关系为B>C
C.用电子式表示AD2的形成过程为
D.由B60分子形成的晶体与A60相似,分子中总键能:B60 >A60
试题篮
()