(14分)分析下图,回答以下问题:
(1)水电解生成H2,首先要解决的问题是________________________________。
(2)氢气作为理想的“绿色能源”除了来源丰富,还有哪些优点:
①________________________________,②_____________________________。
(3)氢氧燃料电池是氢能源利用的一个重要方向,氢气在________极上发生________反应。若电解质溶液为KOH溶液,写出正负极上的电极反应:
正极________________________________,负极________________________________。
人造地球卫星用到的一种高能电池——银锌蓄电池,其电池的电极反应式为Zn+2OH--2e-=ZnO+H2O,Ag2O+H2O+2e-=2Ag+2OH-。据此判断氧化银是
| A.负极,并被氧化 |
| B.正极,并被还原 |
| C.负极,并被还原 |
| D.正极,并被氧化 |
(I)下列装置能组成原电池的是 (填序号)
(II)将CH4设计成燃料电池,装置如图所示(A、B为多孔碳棒)
① (填A或B)处电极入口通甲烷,其电极反应式为 ;
②当消耗甲烷的体积为11.2 L(标准状况下)时,则导线中转移电子数为 ,消耗KOH的物质的量为 。
镍镉(NiCd)可充电电池在现代生活中有广泛应用,它的充放电反应按下式进行:
Cd(OH)2+2Ni(OH)2  Cd+2NiO(OH)+2H2O由此可知,该电池放电时的负极材料是
Cd+2NiO(OH)+2H2O由此可知,该电池放电时的负极材料是
| A.Cd(OH)2 | B.Ni(OH)2 | C.Cd | D.NiO(OH) |
研究和开发CO2和CO的创新利用是环境保护和资源利用双赢的课题。
(1)CO可用于合成甲醇。在体积可变的密闭容器中充入4molCO和8molH2,在催化剂作用下合成甲醇:
CO(g)+2H2(g) CH3OH(g)(Ⅰ),平衡时CO的转化率与温度、压强的关系如图所示:
CH3OH(g)(Ⅰ),平衡时CO的转化率与温度、压强的关系如图所示:
①该反应正向属于________反应;(填“吸热”或放热”)。
②在0.1Mpa 、100℃的条件下,该反应达到平衡时CH3OH体积分数为 。
③在温度和容积不变的情况下,向平衡体系中再充入4molCO,8molH2,达到平衡时CO转化率_______(填“增大”,“不变”或“减小”), 平衡常数K_______(填“增大”,“不变”或“减小”)。
(2)在反应(Ⅰ)中需要用到H2做反应物,以甲烷为原料制取氢气是工业上常用的制氢方法。已知:
CH4(g)+ H2O(g)= CO(g)+3H2(g) △H="+206.2" kJ·mol-1
CH4(g)+ CO2(g)= 2CO(g)+2H2(g) △H="+247.4" kJ·mol-1
则CO和H2O(g)反应生成CO2和H2的热化学方程式为: 。
(3)CO还可以与氧气组成碱性燃料电池,电解质溶液是20%~30%的KOH溶液。则该燃料电池放电时,负极的电极反应式为_______________________________。
化学电池在通讯、交通及日常生活中有着广泛的应用。
(1)目前常用的镍(Ni)镉(Cd)电池,其电池总反应可以表示为:
Cd+2NiO(OH)+2H2O 2Ni(OH)2+Cd(OH)2
2Ni(OH)2+Cd(OH)2
已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸,负极材料是 ,以下说法中正确的是 (填字母代号)
| A.①③ | B.②④ | C.①④ | D.②③ |
①以上反应是可逆反应 ②充电时镍元素被氧化
③电子由正极经电解质溶液流向负极 ④放电时电能转变为化学能
(2)写出放电时正极电极反应:
氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题:
(1)氮元素原子的L层电子数为 ;肼的结构式:
(2)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为 ;
(3)肼可作为火箭发动机的燃料,与氧化剂N2O4(l)反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)= N2O4(1) △H1= -195kJ·mol-1
②N2H4(1) + O2(g)= N2(g) + 2H2O(g) △H2= -534.2kJ·mol-1
写出N2H4(1)和N2O4(1) 反应生成N2和水蒸气的热化学方程式 ;
(4)肼一空气燃料电池是一种具有高效,环境友好的碱性电池,,该电池放电时,负极的反应式为 。
利用生活中常见的材料可以进行很多科学实验,甚至制作出一些有实际应用价值的装置来,下图就是一个用废旧材料制作的可用于驱动玩具的电池的示意图.该电池工作时,有关说法正确的是
| A.铝罐将逐渐被腐蚀 |
| B.炭粒和炭棒上发生的反应为:O2+4e-===2O2- |
| C.炭棒应与玩具电机的负极相连 |
| D.该电池工作一段时间后炭棒和炭粒的质量会减轻 |
二甲醚是一种绿色、可再生的新能源。下图是绿色电源“二甲醚燃料电池”的工作原理示意图(a、b均为多孔性Pt电极)。该电池工作时,下列说法不正确的是
| A.a电极为该电池负极 |
| B.电池工作时,燃料电池内部H+从a电极移向b电极 |
| C.电池工作时,a电极反应式:CH3OCH3—12e-+3H2O═ 2CO2↑+12H+ |
| D.O2在b电极上得电子,电极反应式:O2+4e-+2H2O═ 4OH- |
氢氧燃料电池已用于航天飞机,以30%KOH溶液为电解质溶液的这种电池在使用时的电极反应如下:2H2 + 4OH— - 4e— ="=" 4H2O O2 + 2H2O + 4e— ="=" 4OH—
据此作出判断,下列说法中错误的是
| A.H2在负极发生氧化反应 |
| B.供电时总反应为:2H2 + O2 ="=" 2H2O |
| C.产物为无污染的水,属于环境友好电池 |
| D.燃料电池的能量转化率可达100% |
下列关于充电电池的叙述,不正确的是
| A.充电电池的化学反应原理是氧化还原反应 |
| B.充电电池可以无限制地反复放电、充电 |
| C.充电是使放电时的氧化还原反应逆向进行 |
| D.较长时间不使用电器时,最好从电器中取出电池,并妥善存放。 |
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述不正确的是
3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述不正确的是
| A.放电时负极反应为:3Zn-6e-+6OH-====3Zn(OH)2 |
B.充电时阳极反应为:Fe(OH)3-3e-+5OH- FeO42- +4H2O FeO42- +4H2O |
| C.放电时每转移3 mol电子,正极有1 mol K2FeO4被还原 |
| D.充电时阴极溶液的碱性减弱 |
绿色电源“二甲醚-氧气燃料电池”的工作原理如下图,所示下列说法正确的是
| A.氧气应从c处通入,电极Y上发生的反应为:O2+4e-+2H2O = 4OH- |
| B.电池在放电过程中,电极X周围溶液的pH增大 |
| C.二甲醚应从b处加入,电极X上发生的反应为:(CH3)2O -12e-+3H2O=2CO2+12H+ |
| D.当该电池向外电路提供2 mol电子时消耗O2约为22.4 L |
下列说法正确的是
| A.铅蓄电池在放电过程中,负极质量减小,正极质量增加 |
B.原子核内有10个中子的氧原子 |
| C.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极 |
| D.新制饱和氯水在光照下有气泡产生,其主要成分是氯气 |
铅蓄电池的反应原理为:2PbSO4+2H2O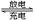 Pb+PbO2+2H2SO4,下列叙述中,正确的是
Pb+PbO2+2H2SO4,下列叙述中,正确的是
| A.PbSO4的氧化性比PbO2的强、还原性比Pb的强 |
| B.放电时,PbO2为氧化剂、做负极,Pb为还原剂、做正极 |
| C.放电时,当有2 mol H2SO4反应时,会有1.204×1024个电子从铅电极流出 |
| D.充电时,PbSO4既被氧化又被还原,Pb是阳极产物之一 |
试题篮
()