可以将反应Zn+Br2 = ZnBr2设计成蓄电池,下列4个电极反应①Br2 + 2e-= 2Br-
②2Br- - 2e-= Br2 ③Zn – 2e-= Zn2+ ④Zn2+ + 2e-= Zn其中表示充电时的阳极反应和放电时的负极反应的分别是( )
| A.②和③ | B.②和① | C.③和① | D.④和① |
碱性电池具有容量大,放电电流大的特点,因而得到广泛应用。锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn+2MnO2+2H2O=Zn(OH)2+2MnOOH,下列说法错误的是( )
| A.电池工作时,锌失去电子 |
| B.电池正极的电极反应式为:2MnO2+2H2O+2e-=2MnOOH+2OH- |
| C.电池工作时,电子由正极通过外电路流向负极 |
| D.外电路中每通过0.2 mol 电子,锌的质量理论上减少6.5 g |
已知蓄电池在充电时作电解池,放电时作原电池,铅蓄电池上的两个接线柱,一个接线柱旁标有“+”,另一个接线柱旁标有“—”,关于标有“+”的接线柱,下列说法中正确的是
| A.充电时作阳极,放电时作负极 |
| B.充电时作阳极,放电时作正极 |
| C.充电时作阴极,放电时作负极 |
| D.充电时作阴极,放电时放正极 |
LiAl/FeS电池是一种正在开发的车载电池,该电池中正极的电极反应式为:
2Li++FeS+2e-→Li2S+Fe ,有关该电池的下列说法中,正确的是( )
| A.负极的电极反应式为Al-3e-―→Al3+ |
| B.该电池的总反应式为2Li+FeS===Li2S+Fe |
| C.LiAl在电池中作为负极材料,该材料中Li的化合价为+1 |
| D.充电时,阴极发生的电极反应式为Li2S+Fe-2e-===2Li++FeS |
据国外媒体报道,iPhone5在电池方面有所改进,它将配备NEC自主研发的ORB超薄有机游离基电池,单次充电仅需30秒.该电池的一极为一种有机高分子的游离基(用R表示)和石墨粉及粘结剂的复合物,另一极是锂,分隔材料为某种聚烯烃,电解质为LiPF6溶解于某种有机碳酸酯溶剂中,高分子游离基在空气中十分稳定,在电池充电时被氧化成阳离子,而电池放电时又被还原成游离基.下列有关说法不正确的是( )
| A.放电时,该电池是将化学能转化为电能 | B.放电时,负极发生的反应是Li-e-═Li+ |
| C.充电时,Rx+由阴极向阳极移动 | D.充电时,阳极发生的反应是R-xe-═Rx+ |
废电池造成污染的问题日益受到关注。下列有关电池的说法正确的是( )
| A.构成原电池的正极和负极必须是两种不同的金属 |
| B.弱电解质在水中的电离程度很小,不能用作电池的电解质溶液 |
| C.原电池是将化学能完全转变为电能的装置 |
| D.回收废旧电池,可防止汞、镉和铅等重金属对土壤和水源的污染 |
利用如图所示原电池可测量空气中Cl2含量,其中电解质是Ag+可以自由移动的固体物质。下列分析不正确的是
| A.电子经外电路流向Pt电极 |
| B.电池工作时,电解质中Ag+数目减少 |
| C.正极反应:Cl2+2e—+2Ag+ = 2AgCl |
| D.空气中c(Cl2)越大,Ag极消耗速率越快 |
根据题意完成下列方程式
(1)写出实验室制备氨气的化学方程式 ;
(2)写出实验室制备Cl2的离子方程式 ;
(3)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3和KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为 ;K2FeO4-Zn可组成碱电池,电池总反应式为:2Fe O42-+8H2O+3Zn=2Fe(OH)3+3Zn(OH)2+4OH-。写出该电池的正极反应式 ;
Al-AgO电池可用作水下动力电源,其原理如图所示。该电池反应的化学方程式为:2Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O,则下列说法正确的是
| A.当电极上析出0.54 g Ag时,电路中转移的电子为0.01 mol |
B.该隔膜是阳离子交换膜 |
| C.Al电极的反应式为:Al-3e-+3OH-=Al(OH)3 |
| D.正极的电极反应式为:AgO+2e-+2H+=Ag+H2O |
(1)可以将氧化还原反应2H2+O2=2H2O设计成原电池,若KOH溶液作电解质溶液,则正极反应式为 。若把H2改为甲烷,KOH溶液作电解质溶液,则负极反应式为 。
(2)酸性锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围是有碳粉,二氧化锰,氯化锌和氯化铵等组成的填充物,该电池在放电过程产生MnOOH。该电池的正极反应式为 ,负极反应式为 ,电池反应的离子方程式为: 。
锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列叙述正确的是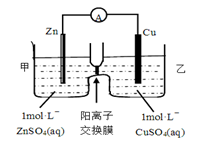
| A.铜电极上发生氧化反应 |
| B.电池工作一段时间后,甲池的c(SO42-)减小 |
| C.电池工作一段时间后,乙池溶液的总质量增加 |
| D.阴阳离子离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡 |
铁镍蓄电池又称爱迪生电池,放电时的总反应为:Fe+Ni2O3+3H2O=Fe(OH)2+2Ni(OH)2。下列有关该电池的说法不正确的是
| A.电池的电解液为碱性溶液,正极为Ni2O3、负极为Fe |
| B.电池放电时,负极反应为Fe+2OH--2e-=Fe(OH)2 |
| C.电池充电时,阳极反应为2Ni(OH)2+2OH--2e-=Ni2O3+3H2O |
| D.电池充电过程中,阴极附近溶液的pH降低 |
金属-硫电池价格低廉,使用寿命较长,能量密度高,因而在电池研究领域得到广泛关注。最近,我国科研工作者研究了一种能在室温下工作的新型Na-S电池。该电池放电过程的总反应方程式如下:nS + 2Na = Na2Sn
注:能量密度指单位质量的电极材料可输出的电能,以W·h·kg-1为计量单位。
则下列说法不正确的是( )
| A.该电池中用固态金属Na为负极,S单质作为正极,但S单质须负载在导电材料上 |
| B.该电池的电解质必须具备室温下传导Na+的能力,但不宜用NaOH溶液作为电解液 |
| C.n值越大则该电池的能量密度越高 |
| D.该电池充电过程中阳极的电极反应式:Na2Sn-2e-=2Na++ nS,故充电时Na+从阳极向阴极迁移 |
燃料电池是一种利用能源物质的新的形式,比如我们可用熔融的K2CO3作电解质,惰性材料作电极,一极通CH2=CH2,另一极通O2、CO2下列说法中不正确的是( )
| A.通入乙烯的一极为正极 |
| B.正极发生的电极反应为:3O2+6CO2+12e-=6CO32- |
| C.负极发生的电极反应为:CH2=CH2+6CO32--12e-=8CO2+2H2O |
| D.电池的总反应式为:CH2=CH2+3O2=2CO2+2H2O |
试题篮
()