“神州”六号飞船上使用是氢氧燃料电池,其电池总反应式为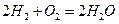
试完成下列问题:
(1) 若电解溶液为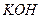 溶液,则电极反应式为:
溶液,则电极反应式为:
负极:
正极:
(2)如果把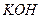 改为稀硫酸做导电物质,则电极反应式为:
改为稀硫酸做导电物质,则电极反应式为:
负极:
正极:
(3)如果把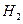 改为
改为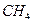 ,
,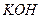 溶液作导电物质,则电极反应式为:
溶液作导电物质,则电极反应式为:
负极:
正极:
被称之为“软电池”的纸质电池,采用一个薄层纸片作为传导体,在其一边镀锌,而在其另一边镀二氧化锰。在纸内是离子“流过”水和氧化锌组成的电解液。电池总反应为:Zn + 2 MnO2十H2O =" ZnO" + 2MnO (OH)。下列说法正确的是
| A.该电池的正极为锌 |
| B.电池正极反应式为: 2MnO2 + 2e-+ 2H2O =" 2MnO" (OH)十2OH- |
| C.当 0.l mol Zn 完全溶解时,流经电解液的电子个数为 1.204×l023 |
| D.该电池反应中二氧化锰起催化作用 |
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:
Zn(s)+2MnO2+H2O(l)====Zn(OH)2(s)+Mn2O3(s)
下列说法错误的是( )
| A.电池工作时,锌失去电子 |
| B.电池正极的电极反应式为:2MnO2+H2O(l)+2e-====Mn2O3(s)+2OH-(aq) |
| C.电池工作时,电子由正极通过外电路流向负极 |
| D.外电路中每通过0.2 mol电子,锌的质量理论上减小了6.5 g |
铁——镍蓄电池充电放电时发生的反应为:


 ,关于此蓄电池的下列说法中不正确的是( )
,关于此蓄电池的下列说法中不正确的是( )
| A.放电时Fe为负极 |
B.充电时阴极的电极反应式为: |
C.放电时 的反应为: 的反应为: |
| D.蓄电池的电极必须浸在碱性电解质溶液中 |
实验室用铅蓄电池作电源电解饱和食盐水制氯气,已知铅蓄电池放电时发生如下反应:
负极:
正极:
今若制得Cl2O.050mol,这时电池内消耗的H2SO4的物质的量至少是
| A.O.O25mol | B.O.O5Omol |
| C.O.1Omol | D.0.2Omol |
我国首创以铝—空气—海水电池作为能源的新型的海水标志灯,以海水为电解质溶液,靠空气中的氧气使铝不断氧化而产生电流,只要把灯放入海水数分钟,就会发出耀眼的白光。则电源的负极材料是 ,负极反应为 ;正极材料是 ,正极反应为 。
试题篮
()