下列物质中,按只有氧化性、只有还原性、既有氧化性又有还原性的顺序排列的一组是( )
| A.F2、K、HCl | B.Cl2、Al、H2 |
| C.NO2、Na、Br2 | D.O2、SO2、H2O |
“服用维生素C可使食物中的三价铁离子变成二价铁离子”这句话说明
| A.维生素C本身被还原 | B.维生素C具有还原性 |
| C.维生素C具有氧化性 | D.维生素C发生了还原反应 |
氢化钙中的氢元素为-1价,它可用做生氢剂,反应的化学方程式是:
CaH2+2H2O==Ca(OH)2+2H2↑。该反应中,水的作用是. ( )
| A.溶剂 | B.还原剂 | C.氧化剂 | D.既是还原剂又是氧化剂 |
氢硫酸在空气中有如此反应:2H2S+O2==2S↓+2 H2O,下列不正确的是( )
| A.属于置换反应 | B.还原性:H2O> H2S |
| C.氧化性:O2> S | D.酸性:H2S> H2O |
常温下,H2O2溶液中滴加少量FeSO4溶液,可发生如下反应:2Fe2++H2O2+2H+=2Fe3++2H2O,下列说法正确的是( )
| A.Fe2+得电子 | B.H2O2被氧化 |
| C.H2O2的氧化性比Fe3+强 | D.H2O既不是氧化产物也不是还原产物 |
已知反应①2BrO3- + Cl2 =Br2 +2ClO3-②5Cl2 + I2 +6H2O=2HIO3 +10HCl
③ClO3- +5Cl-+6H+=3Cl2 +3H2O,下列物质氧化能力强弱顺序正确的是( )
| A.ClO3->BrO3->IO3->Cl2 | B.BrO3->Cl2>C1O3->IO3- |
| C.BrO3->ClO3->Cl2>IO3- | D.Cl2>BrO3->C1O3->IO3- |
下列各反应中,水作为还原剂的是( )
A.2H2+O2 2H2O 2H2O |
B.SO3+H2O==H2SO4 |
| C.2F2+2H2O==4HF+O2 | D.2Na+2H2O==2NaOH+H2 ↑ |
金属镍有广泛的用途。粗镍中含有少量Fe、Cu、Pt等杂质,可用电解法制备高纯度的镍(用NiSO4作电解质溶液)。已知:氧化性Fe2+<Ni2+<Cu2+,下列叙述正确的是
| A.阳极发生还原反应,其电极反应式:Ni2+2e=Ni |
| B.电解过程中,阳极质量的减少与阴极质量的增加相等 |
| C.电解后,溶液中存在的金属阳离子只有Fe2+ |
| D.电解后,可以从电解槽底部的阳极泥中回收Cu和Pt |
常温下,在下列溶液中发生如下反应: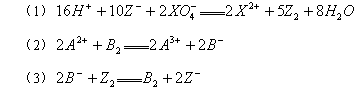
由此判断,下列说法错误的是
A.溶液中不可能发生反应 |
| B.Z2元素在(1)(3)反应中均做还原剂 |
C.氧化性由强到弱顺序是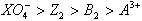 |
| D.X2+是XO4还原产物 |
制备单质硅时,主要化学反应如下
①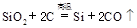 ②
② ③
③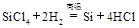 下列对上述三个反应的叙述中,不正确的是( )
下列对上述三个反应的叙述中,不正确的是( )
| A.①③为置换反应 | B.①②③均为氧化还原反应 |
| C.②为化合反应 | D.三个反应的反应物中硅元素均被氧化 |
试题篮
()