已知有如下反应:①2Fe3++2I-===2Fe2++I2 ②2Fe2++Br2===2Fe3++2Br-
③2Fe(CN)+I2===2Fe(CN)+2I-,试判断氧化性强弱顺序正确的是
| A.Fe3+>Br2>I2>Fe(CN) |
| B.Br2>I2>Fe3+>Fe(CN) |
| C.Br2>Fe3+>I2>Fe(CN) |
| D.Fe(CN)>Fe3+>Br2>I2 |
已知有如下反应:①2BrO3-+Cl2=Br2+2ClO3-,②ClO3-+5Cl-+6H+=3Cl2+3H2O,③2FeCl3+2KI=2FeCl2+2KCl+I2,④2FeCl2+Cl2=2FeCl3。下列各微粒氧化能力由强到弱的顺序正确的是
| A.ClO3->BrO3->Cl2>Fe3+>I2 | B.BrO3->Cl2>ClO3->I2>Fe3+ |
C.BrO3->ClO3->Cl2>Fe3+>I2 | D.BrO3->ClO3->Fe3+>Cl2>I2 |
常温下,在溶液中可发生以下反应:
①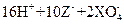 ===
===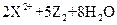 ,
,
②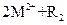 ===
=== ,③
,③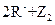 ===
=== ,
,
由此判断下列说法错误的是( )
A.还原性强弱顺序为: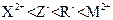
B.Z元素在反应①中被氧化,在③中被还原
C.常温下可发生反应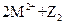 ===
===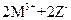
D氧化性强弱顺序为: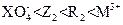
赤铜矿的成分是Cu2O,辉铜矿的成分是Cu2S,将赤铜矿与辉铜矿混合加热有以下反应:Cu2S + 2Cu2O 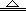 6Cu + SO2↑。对于该反应的下列说法正确的是
6Cu + SO2↑。对于该反应的下列说法正确的是
| A.该反应中的氧化剂只有Cu2O | B.Cu2O在反应中既是氧化剂又是还原剂 |
| C.Cu既是氧化产物又是还原产物 | D.氧化产物与还原产物的物质的量之比为1:6 |
常温下,分别在溶液中发生如下反应:(1)16H+ + 10Z- + 2XO4- ="=" 2X2++ 5Z2↑+ 8H2O,(2)2A2+ + B2==2A3++ 2B-,(3)2B- + Z2== B2 + 2Z-。由此判断下列说法错误的是
| A.反应Z2+2A2+="=" 2A3++2Z-能发生 |
| B.氧化性由强到弱的顺序是XO4-、Z2、B2、A3+ |
| C.还原性由强到弱的顺序是 A 2+、B-、Z-、X2+ |
| D.Z元素在(1)、(3)反应中均被还原 |
已知下面六句话:①A氧化B,②B氧化A,③A被B氧化,④B被A氧化,⑤A被B还原,⑥B被A还原。其中和第一句话的意思相同的是
| A.②③ | B.②④ | C.⑤⑥ | D.④⑤ |
在常温下,发生下列反应:①16H++10Z-+2XO4-→2X2++5Z2+8H2O;②2A2++B2→2A3++2B-;③2B-+Z2→B2+2Z-。根据上述反应,判断下列结论中错误的是 ( )
| A.溶液中可发生:Z2+2A2+→2A3++2Z- |
| B.Z2在①、③反应中为还原剂 |
| C.氧化性强弱的顺序为:XO4->Z2>B2>A3+ |
| D.X2+是XO4-的还原产物 |
下列物质在空气中久置会发生变质,且在变质过程中,既有氧化还原反应发生,又有非氧化还原反应发生的是
| A.苛性钠溶液 | B.漂白粉 | C.氯水 | D.生石灰 |
已知I-、Fe2+、SO2、Cl-、和H2O2均有还原性,它们在酸性溶液中还原性的顺序为SO2>I->Fe2+>H2O2>Cl-,则下列反应不可能发生的是
| A.2Fe 3+ + SO2 + 2H2O = 2 Fe 2+ + SO42- + 4H+ |
| B.I2 + SO2 + 2H2O= H2SO4 + 2HI |
| C.2 Fe 2+ + I2=2Fe 3+ + 2I- |
| D.H2O2 + SO2=H2SO4 |
在一种酸性溶液中存在NO3-、I-、Cl-、Fe3+中的一种或几种离子,向该溶液中加入溴水,溴单质被还原,由此可推知该 溶液中( )
溶液中( )
A 一定含有I-,不能确定是否含有Cl- B 一定含有NO3-
C 不含有Fe3+,可能含有NO3- D 一定含有I-、NO3-和Cl-
试题篮
()